Propriedades coligativas,energia potencial e força iônica
Análises Físico-Químicas
1 O que são as propriedades coligativas
Propriedades coligativas são aquelas que percebemos quando um soluto não volátil é adicionado a um solvente. A intensidade com que essas propriedades aparecem depende apenas do número de partículas do soluto na solução, mas não depende da natureza do soluto.
Solutos não voláteis podem ser moleculares ou iônicos. Um exemplo de soluto molecular não volátil é o açúcar (sacarose - C12H22O11) que vemos na forma de cristais brancos, porque milhares e milhares de moléculas estão bem ligadas, formando esses cristais.
Mas quando dissolvemos o açúcar na água, suas moléculas se separam e se isolam, então não podemos vê-las, mas as moléculas C12H22O11 se dissolvem na água lá.
Um exemplo de soluto não volátil iônico é o sal (cloreto de sódio – NaCl), cujas fórmulas unitárias estão também unidas, formando aglomerados iônicos de estrutura geométrica bem definida, que são chamados de retículos cristalinos. Mas ao ser colocado em água, o sal reage com as moléculas dela, tendo os seus íons separados (ocorre uma dissociação iônica). Assim, os íons Na+ e Cl- ficam dispersos na água e também não são visíveis a olho nu.
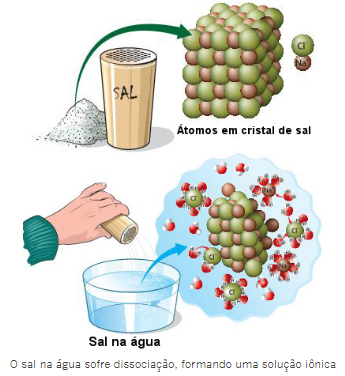
Assim, essas partículas (moléculas ou íons) que ficam dispersas no solvente, que geralmente é a água, são as responsáveis por mudanças em determinadas propriedades do solvente.
As quatro propriedades coligativas são:
* Tonoscopia ou tonometria: O efeito tonoscópico é a diminuição da pressão de vapor de um líquido quando um soluto não volátil é adicionado a ele.
Quando preparamos uma mistura de água e açúcar, por exemplo, as moléculas de açúcar dissolvem-se porque são polares como as moléculas de água. Elas interagem umas com as outras por meio de forças intermoleculares, o que dificulta que as moléculas de água da superfície do líquido passem para o estado de vapor e escapem do solvente.
O abaixamento relativo da pressão máxima de vapor é representado pela relação&&DeltaP/P2 e pode ser calculado por meio da fórmula:

* Ebulioscopia ou ebuliometria: O efeito ebulioscópico é o aumento do ponto de ebulição de um líquido quando adicionamos um soluto não volátil a ele.
Por exemplo, quando temos água fervendo, ou seja, que já atingiu o seu ponto de ebulição (100 ºC ao nível do mar), e adicionamos açúcar, a água para de ferver na hora, ou seja, a temperatura de ebulição aumentou. Isso acontece pelo mesmo motivo mencionado para o efeito tonoscópico, isto é, a interação entre as moléculas do solvente e do soluto dificulta que a molécula passe para o estado de vapor, por isso, é necessário adicionar mais energia na forma de calor para que a solução entre em ebulição.
O aumento do ponto de ebulição pode ser calculado por meio da fórmula:

Crioscopia ou crometria: O efeito crioscópico é a diminuição do ponto de congelamento de um líquido quando um soluto não volátil é adicionado a ele.
Por exemplo, em lugares frios, as águas dos mares formam uma camada de gelo somente na superfície, porque ela é formada somente por água. Já a parte líquida que fica abaixo do gelo não se congela porque, além de o gelo ser um isolante térmico natural, essa água possui vários sais dissolvidos que diminuem o ponto de congelamento.
Em países que nevam, há o risco de congelamento da água dos radiadores usados para refrigerar os motores. Por isso, há alguns produtos comerciais (aditivos) que são adicionados com a finalidade de diminuir o ponto de congelamento da água e evitar o seu congelamento. Um exemplo de anticongelante usado com essa finalidade é o etilenoglicol (C6H6O2), que, se estiver em uma proporção de 50%, tem a capacidade de abaixar o ponto de fusão da mistura até cerca de -35 ºC.
A diminuição do ponto de congelamento pode ser calculado por meio da fórmula:

Osmoscopia: O fenômeno da osmose ocorre quando colocamos um solvente puro e uma solução (ou duas soluções com concentrações diferentes) separados por uma membrana semipermeável e ocorre a passagem de solvente pela membrana no sentido do solvente para a solução (ou da solução menos concentrada para a mais concentrada).
Por exemplo, se colocarmos ameixas secas em água, com o tempo, notaremos que as ameixas incharão. Isso ocorre porque a pele da ameixa seca funciona como uma membrana semipermeável e o solvente (água) passa por ela e vai para o interior da ameixa.

A pressão osmótica (π) pode ser calculada por meio da fórmula:

Quando adicionamos açúcar na água que está fervendo, ela para de ferver. Isso é explicado pela ebulioscopia, uma propriedade coligativa

2 Energia Potencial
O que é energia potencial?
Energia potencial é uma forma de energia que pode ser armazenada nos corpos e que depende do tipo de interação e da posição que o corpo apresenta em relação à sua vizinhança. Na Física, existem basicamente duas formas de energia potencial mecânica: energia potencial gravitacional e energia potencial elástica.
A energia potencial armazenada por qualquer objeto sujeito a forças conservativas é definida pela posição do objeto e independe do caminho tomado por ele. São chamadas de forças conservativas todas as forças capazes de armazenar energias que podem ser acessadas em momentos posteriores, como a força elástica ou a força gravitacional.
Além disso, é necessário que as forças conservativas sejam capazes de transformar uma energia em outras formas de energia. Um exemplo de energia potencial é a energia potencial gravitacional, que independe da trajetória tomada pelo corpo. Para essa forma de energia, são consideradas somente as posições final e inicial do corpo.
Trabalho e energia potencial
Quando a energia potencial de um corpo sofre acréscimos ou decréscimos em seu módulo sob a ação exclusiva de forças conservativas, dizemos que essas forças realizaram trabalho sobre ele.
O trabalho é o fenômeno físico responsável pela transformação de uma forma de energia em outra por meio da aplicação de uma força. No caso em que um corpo é abandonado de uma certa altura, a força peso realiza trabalho sobre ele, transformando sua energia potencial gravitacional em energia cinética, por exemplo.
Unidade de medida da energia potencial
A unidade física utilizada para energia potencial no Sistema Internacional de Unidades é o joule (J): 1 joule equivale à quantidade de energia necessária para elevarmos a um metro (1,0 m) de altura um peso igual a 1 Newton (1,0 N).
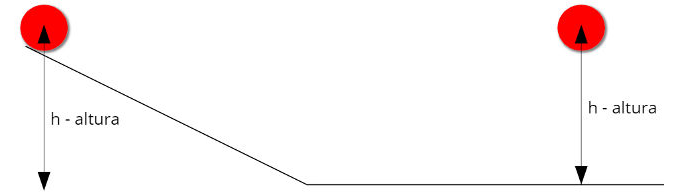
Olhe a figura acima.Nela, temos dois corpos que estão prestes a cair de uma mesma altura. A mudança na energia potencial gravitacional que cada um deles sofrerá é exatamente a mesma, uma vez que a força peso, responsável pelo movimento de queda dos corpos, é uma força conservativa. Apesar de o corpo à esquerda percorrer um caminho maior, a diferença de altura dos corpos em relação ao solo é a mesma.
Um exemplo de força não conservativa é a força de atrito. Se houvesse atrito na situação ilustrada na figura acima, ele não seria exatamente o mesmo para os dois casos, uma vez que a distância percorrida por um dos corpos é maior que a distância percorrida pelo outro. Logo, o atrito é uma força não conservativa e não é capaz de armazenar energia em forma de energia potencial.
O que é energia potencial gravitacional?
Energia potencial gravitacional é a energia relacionada à altura de um corpo em relação ao solo. Trata-se de uma grandeza escalar, definida unicamente pelo seu módulo, medido em joules (J). A energia potencial gravitacional é definida por meio da seguinte equação:

Como a energia potencial é escalar, ela pode ser definida em relação a qualquer referencial. Por exemplo: um corpo que se encontra na cobertura de um prédio tem uma grande energia potencial gravitacional em relação à rua, entretanto, sua energia potencial relativa àquela cobertura é nula.
O que é energia potencial elástica?
Energia potencial elástica é uma forma de energia relacionada à compressão ou elongação de um corpo que tende a voltar ao seu formato original, como molas e elásticos.
Quando algum corpo tem tendência a voltar à sua posição de equilíbrio em razão de uma força restauradora, assim como uma mola esticada ou comprimida, dizemos que ele é capaz de armazenar energia em forma de energia potencial elástica.
A energia potencial elástica, assim como todas as outras formas de energia potencial, também é escalar. Dessa forma, o caminho tomado pelo corpo não afeta o módulo de sua energia potencial, que é afetado somente pela diferença entre as posições final e inicial do corpo. Por exemplo: um corpo elástico, quando esticado ou comprimido em dois centímetros, apresentará a mesma quantidade de energia potencial elástica para ambos os casos.
Podemos calcular a energia potencial elástica de um corpo por meio da equação apresentada abaixo:

Na equação acima, k recebe o nome de constante elástica. Essa constante é uma propriedade do corpo e mede a intensidade da força necessária para deformar o corpo em um metro. Já a variável x mede a deformação do corpo em metros. Se o corpo estiver em seu tamanho original, sua deformação será nula, de forma que x = 0. Portanto, esse corpo não apresentará qualquer energia potencial elástica.
Fórmulas de energia potencial
Para calcularmos a energia potencial gravitacional contida em um corpo, utilizamos a fórmula abaixo:

Podemos calcular o módulo da energia potencial elástica de um corpo por meio da fórmula abaixo:

Um exemplo sobre energia potencial
Confira abaixo um exemplo de aplicação das fórmulas de energia potencial gravitacional e energia potencial elástica.
Calcule o módulo da energia potencial gravitacional de um corpo de massa igual a 4,0 kg que se encontra em uma altura de 50,0 cm em relação ao solo. Adote g = 10 m/s².
Resolução:
Para calcularmos o módulo da energia potencial gravitacional desse corpo, fazemos o seguinte cálculo:
Lembre-se de que é necessário que a altura esteja definida em metros (50,0 cm equivalem a 0,5 m).

3 Força Iônica
A força iônica de uma solução é uma medida de sua concentração de íons. Os compostos iônicos, quando dissolvidos em água, se dissociam em íons. A concentração total de eletrólitos na solução afeta propriedades importantes, como a dissociação e a solubilidade de vários sais. Uma das principais características determinadas pelos íons dissolvidos em uma solução é sua força iônica.
Quantificando a força iônica
A força iônica, I, de uma solução é função da concentração de todos os íons presentes naquela solução.
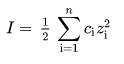

Como nas soluções não-ideais on volumes não se comportam de maneira rigorosamente aditiva, é frequentemente preferível trabalhar com a molalidade (mol/kg{H²O}) ao invés da molaridade (mol/L). Neste caso, a força iônica é definida como:
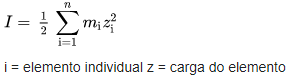
Exemplo:

A importância da força iônica

Durante as titulações, são utilizados meios de alta força iônica para a determinação de constantes de equilíbrio, com a finalidade de minimizar a alteração no coeficiente de atividade dos solutos a baixas concentrações. A água procedente de fontes naturais, têm sempre um valor de força iônica diferente de zero, devido à presença de sais dissolvidos.