Estado sólido e Função de Gibbs
Análises Físico-Químicas
1 Estado sólido da matéria
O estado sólido é um estado da matéria, cujas características são ter volume e forma definidos, isto é, a matéria resiste à deformação. Dentro de um sólido, os átomos ou as moléculas estão relativamente próximos, ou "rígidos". Mas isto não evita que o sólido se deforme ou comprima. Na fase sólida da matéria, os átomos têm uma ordenação espacial fixa, mas uma vez que toda a matéria tem alguma energia cinética, até os átomos do sólido mais rígido movem-se ligeiramente, num movimento "invisível".Os sólidos quando submetidos a altas temperaturas, passam para a fase líquida quando alcançam o ponto de fusão, que é variável dependendo do material e através da sublimação é possível que passem direto para a fase de vapor.Além disso, as forças de coesão (agrupamento) são maiores que as forças de repulsão em suas moléculas. As partículas possuem apenas energia cinética vibracional, apenas vibram em posições fixas, definidas.
O gelo é um exemplo sendo o estado sólido da água

Algumas das propriedades dos sólidos :
Fragilidade: O sólido frágil rompe-se com facilidade sem antes deforma-se e uma de suas característica é romper bruscamente, a fragilidade também é o oposto da ductilidade.
Exemplo: A grafite é um material frágil.
Dureza: O sólido duro apresenta resistência a ter sua superfície riscada. A dureza pode ser medida pela Escala de Mohs.
Exemplo: As pedras preciosas são materiais de grande dureza.
Resistência: O sólido resistente é capaz de suportar a ação de forças intensas sem romper-se.
Exemplo: O ferro e outros metais são materiais resistentes a esforços externos.
Elasticidade: O sólido elástico deforma-se e recupera a forma original quando a força que produziu a deformação é retirada.
Exemplo: A borracha é um material elástico
Flexibilidade: O sólido flexível dobra-se sem romper-se.
Exemplo: Algodão, lã, náilon e outras fibras têxteis são materiais flexíveis.
Ductilidade: O sólido dúctil estende-se com facilidade, formando fios. A ductilidade é o oposto da fragilidade.
Exemplo: O ouro é bastante dúctil.
A plasticidade descreve a deformação de um material submetido as forças aplicadas.
Os sólidos são classificados em cristalinos ou amorfos.
Sólidos cristalinos
Com exceção do mercúrio, os metais são caracterizados por estarem em estado sólido à temperatura ambiente,de modo que os sais e a maioria dos minerais são cristais. Cristais como sal e quartzo são conhecidos pelos seres humanos há vários séculos, mas apenas no século 20, que foram interpretados como arranjos regulares de átomos. Em 1912, raios-X foram usados para confirmar que cada cristal é um arranjo tridimensional ordenado. As medidas mostraram que os átomos de um cristal estavam muito próximos, com a distância entre eles aproximadamente o comprimento dos raios-X.
Materiais cujos constituintes são dispostos em um padrão regular são conhecidos como cristais.Em sólidos cristalinos, as partículas (átomos, moléculas ou íons) estão em um padrão de regularidade ordenada, repetitivas. Há muitas estruturas cristalinas diferentes, e da mesma substância pode ter mais de uma estrutura (ou fase sólida), por exemplo, o gelo tem quinze estruturas cristalinas conhecidas, ou quinze fases sólida, que existem em várias temperaturas e pressões.
Uma das características dos sólidos é a organização das moléculas que compõem o material, pois estão de forma organizada, logo, outros materiais como o vidros, plásticos e outros, que não possuem essa organização, são denominados sólidos amorfos.
Cristais de insulina

No estado sólido, a distância média de separação entre os átomos, ou moléculas, que formam a amostra é comparável aos seus diâmetros. Neste caso, a intensidade da interação entre os átomos, ou moléculas é da mesma ordem de grandeza que a intensidade da interação que mantém unidos os átomos em moléculas isoladas.
Uma base para classificar os sólidos cristalinos é a natureza das forças que mantêm o ordenação da rede cristalina. A energia de coesão em um cristal depende das forças de ligação dominantes entre esses átomos, ou moléculas. A classificação dos sólidos cristalinos são: sólidos cristalinos iônicos, sólidos cristalinos covalentes, sólidos cristalinos moleculares e sólidos cristalinos metálicos.
Sólidos cristalinos iônicos: Nos sólidos iônicos a rede cristalina é formada por íons positivos e negativos. Por causa das forças eletrostáticas relativamente intensas entre os íons, os sólidos iônicos são geralmente duros, frágeis e têm um elevado ponto de fusão. Por não terem elétrons livres, sua condutividade elétrica é muito baixa.Os sólidos iônicos podem ser solúveis, ou mesmo, muito solúveis, pois, por exemplo, em contato com a água, os íons dispersam-se no líquido.
Posuem energia de vibração da rede menor que a dos sólidos covalentes. Os exemplos deste tipo de sólidos são o cloreto de sódio (NaCl) e o cloreto de césio (CsCl).
Sólidos cristalinos covalentes: Nos sólidos covalentes ocorre o compartilhamento de pares de elétrons de valência entre os átomos, formando ligações covalentes. Cada elétron está ligado de forma que não há elétrons livres. Por isso esses sólidos possuem baixa condutividade elétrica. Esses sólidos também possuem a característica de serem duros e difíceis de deformar.As energias de vibração da rede são elevadas, da mesma forma são as frequências geradas. Um exemplo típico deste tipo de sólidos é o diamante.
Sólidos cristalinos moleculares: Esses sólidos são constituídos por moléculas apolares, ou seja, os elétrons encontram-se emparelhados e não formam ligações covalentes, suas moléculas estão ligadas pelas forças de Van der Waals. Esses sólidos possuem baixa condutividade elétrica,são altamente compressíveis e deformáveis e apresentam um ponto de fusão baixo, porque as ligações intermoleculares que unem as suas moléculas são relativamente frágeis, quebrando-se com alguma facilidade.
Sólidos cristalinos metálicos: São formados a partir de átomos com alguns elétrons fracamente ligados nas camadas mais externas, que passam a se mover por todo o sólido. Um sólido cristalino metálico é constituído por uma rede ordenada de íons positivos que são mantidos juntos por uma espécie de gás de elétrons livres. A mobilidade dos elétrons de valência que constituem esse gás de elétrons torna esses metais bons condutores de eletricidade.Os sólidos metálicos são opacos, visto que os referidos eletrões livres absorvem os fotões das radiações eletromagnéticas do visível.
Aos sólidos que são organizados em um único cristal, esses são denominados monocristais e aos agregados em muitos cristais, são denominados policristais.
Sólidos amorfos
São aqueles não possuem uma ordenação interna uniforme, carecem de um rede de cristalização, aliás, sua estrutura interior se assemelha mais aos líquidos, com disposição interna em grande parte aleatória. Os sólidos amorfos são por exemplo, os plásticos, os vidros, os sabões, as parafinas e muitos outros compostos orgânicos e inorgânicos.Em muitos amorfos as partículas possuem uma liberdade para vaguear pelo material. Isso é evidenciado, por exemplo, na elasticidade da borracha, na tendência do vidro fluir quando sujeito a tensões por longos períodos de tempo.
Algumas das aplicações dos vidros e dos materiais plásticos derivam de sua qualidade de serem facilmente moldáveis quando submetidos a aumentos de temperatura.Podem ser encontrados exemplos de sólidos amorfos nos três grupos de materiais (metálicos, cerâmicos e poliméricos), embora esses três grupos tenham uma maior propensão a serem cristalinos. Uma das formas de se obter um sólido amorfo é evitar sua cristalização durante o processo de solidificação. Em muitas substâncias é possível evitar a cristalização, por exemplo, através do rápido resfriamento.
Os metais puros tem grande são propensos à cristalização, por outro lado a solidificação ultra-rápida de diversos metais produzem metais amorfos, também denominados vidros metálicos.O primeiro metal amorfo a se ter notícia era uma liga de ouro e silício (Au75Si25) produzida pelos cientistas W. Klement (Jr.), Willens e Duwez em 1960.
A ausência de simetria fazem dos vidros metálicos excelentes materiais magnéticos. Geralmente apresentam grande resistência metálica e tenacidade. São mais resistentes a corrosões do que as ligas cristalinas tradicionais. Apresentam alta resistência elétrica e baixas perdas acústicas.
Os sólidos amorfos também são chamados de sólidos vítreos
Amostras de metal amorfo

Cristais Líquidos
Os cristais líquidos são materiais que apresentam estado da matéria compreendido entre os estados sólido e líquido, assim sendo, esses materiais apresentam características tanto da fase sólida quanto da fase líquida. Nesse estado as moléculas mantêm sua orientação, mas também se movimentam em várias direções, assim como no sólido e no líquido respectivamente. Esses materiais são constituídos na sua maioria por moléculas orgânicas anisométricas. Essas moléculas possuem dimensões bem maiores que as outras, podendo ter forma alongada ou de disco.
Existe uma variedade de substâncias que se encontram na fase sólida ou líquida. Da mesma forma existem várias substâncias de cristal líquido. De acordo com a temperatura e a natureza, os cristais líquidos podem se apresentar em diferentes fases como, por exemplo, na fase nemática. Essa fase é a que torna possível a fabricação das TVs de LCD. Dentre todas as características dos cristais líquidos, a que mais se destaca é o fato de essas substâncias serem afetadas por correntes elétricas. O cristal líquido chamado de nemático torcido, um cristal que se encontra na fase nemática, encontra-se naturalmente torcido. Ao aplicar uma corrente elétrica sobre esses cristais faz com que eles se destorçam em vários graus, dependendo da intensidade da tensão que é aplicada sobre ele. As TVs de LCD utilizam esse cristal líquido porque ele reage à passagem da corrente elétrica controlando, dessa forma, a passagem da luz.
Alguns cristais líquidos são sensíveis a pequenas variações de temperatura, de forma que através dessa variação eles podem mudar de cor. Essa propriedade é aproveitada na construção de termômetros de cristal líquido. Outras aplicações dos cristais líquidos são os suportes de copo e o display de cristal líquido (LCD). O primeiro possui uma camada que é sensível a pequenas variações de temperatura, possibilitando assim uma variedade de cores a serem observadas pelo usuário. Já o segundo é um tipo de mostrador que vem sendo muito utilizado nos aparelhos digitais no lugar dos chamados LEDs.
Polimorfismo
Polimorfismo, em química, é a propriedade de materiais sólidos poderem existir sob mais de uma forma cristalina. Pode ser encontrado em qualquer material cristalino incluindo polímeros e metais. O polimorfismo de substâncias químicas elementares é apelidado de alotropia. Opõe-se ao isomorfismo, que caracteriza materiais de constituição química diferente, mas com a mesma forma cristalina.
Estudo dos sólidos
Os físicos chamam ao estudo dos sólidos física do estado sólido Este ramo inclui o estudo de semicondutores e de supercondutividade, também tem como objetivo explicar e prever as diversas propriedades macroscópicas dos materiais cristalinos, tais como, térmicas, elétricas, magnéticas, ópticas etc. A partir da aplicação das leis da física a seus constituintes microscópicos. Os materiais densos não-cristalinos não se incluem nesse estudo, pois são considerados mais semelhantes aos líquidos. A física da matéria condensada é uma área da física cujo objeto de investigação engloba o da física do estado sólido e inclui sólidos amorfos e líquidos.Essa área de estudo parte, em geral, dos métodos e modelos desenvolvidos na física do estado sólido, modificando-os e adaptando-os de modo adequado.
A ciência dos materiais preocupa-se primariamente com propriedades dos sólidos tais como a força e transformações de fase. É largamente coincidente com a física do estado sólido.
A química do estado sólido cobre em parte ambos estes campos, mas preocupa-se principalmente com a síntese de novos materiais.
Mudança do estado físico
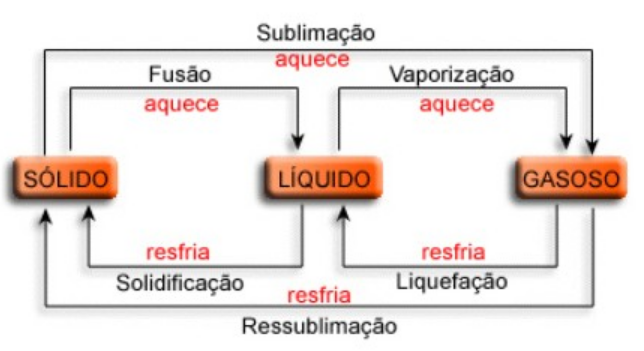
As mudanças do estado físico envolvendo o estado sólido são:
Fusão: é a passagem de uma substância do estado sólido para o estado líquido.
Solidificação: é a passagem do estado físico de uma substância do estado líquido para o estado sólido.
Sublimação: é a passagem de uma substância do sólido para o estado gasoso, esse processo só ocorre em condições adequadas de pressão e temperatura.Sublimação também pode ser a passagem direta do estado gasoso para o estado sólido,nesse caso pode ser chamada de ressublimação, ou sublimação regressiva.
2 Função de Gibbs
A energia livre de Gibbs (ΔG) é uma grandeza que foi determinada pelo físico, matemático e químico norte-americano Josiah Willard Gibbs no ano de 1883. Gibbs desenvolveu essa grandeza com o intuito de prever a espontaneidade de uma reação química.
Antes de 1883, acreditava-se que a espontaneidade de uma reação era determinada por apenas duas grandezas: a variação da entalpia (ΔH) e a variação da entropia (ΔS). A reação seria espontânea quando:
ΔH<0 (reação exotérmica): há liberação de energia
ΔS>0: o sistema reacional possui grande desorganização atômica
Porém, Gibbs descobriu que, quando uma reação química espontânea ocorre, parte da energia liberada (reação exotérmica) sempre é utilizada para reorganizar o sistema (reorganizar os átomos). Essa parte de energia depende da temperatura (T) e do nível de desorganização dos átomos (ΔS).
A partir disso, Gibbs concluiu que a entalpia (energia liberada durante a reação), a entropia e a temperatura são os fatores determinantes para prever a espontaneidade de uma reação.
Assim, podemos definir a energia livre de Gibbs (ΔG) como a energia útil de um sistema que resulta da diferença entre a entalpia e a entropia (esta multiplicada pela temperatura), o que resulta na seguinte equação matemática:
ΔG = ΔH – T. ΔS
Unidades da energia livre de Gibbs
Joule (J)
Quilojoule (KJ) - 1 KJ equivale a 1000 J
Caloria
Quilocaloria (Kcal) - 1 Kcal equivale a 1000 cal
Vale lembrar que 1 Kcal = 4,18 KJ ou 1 cal = 4,18 J.
Detalhes fundamentais sobre a energia livre de Gibbs
Como a energia livre de Gibbs é a energia que sobra após uma reação química espontânea, logo, ela é liberada. Assim sendo, uma reação só é espontânea se o resultado do ΔG for menor que 0;
A expressão da energia livre de Gibbs só é aceita se a reação estiver sendo realizada sobre pressão e temperatura constantes;
A temperatura, no cálculo da energia livre de Gibbs, sempre deve estar na unidade Kelvin;
A energia livre de Gibbs é a máxima energia que pode ser retirada de um sistema (uma reação);
Quando utilizamos a fórmula da energia livre de Gibbs, é fundamental que as variações de entalpia (ΔH) e entropia (ΔS) estejam na mesma unidade de medida.
Espontaneidade de uma reação
Podemos prever a espontaneidade de uma reação baseando-nos em diferentes condições de entalpia, entropia e temperatura da seguinte forma:
a) Quando o ΔH for positivo (maior que zero) e o ΔS for negativo (menor que 0):
ΔH =+x
ΔS = -y
Quando essas grandezas forem adicionadas à expressão matemática a seguir:
ΔG = ΔH – T. ΔS
ΔG = x - T.(-y)
ΔG = x + T.y
O resultado do ΔG será positivo e, com isso, a reação não será espontânea.
b) Quando o ΔH for positivo (maior que zero) e o ΔS for positivo (maior que 0)
ΔH =+x
ΔS = +y
Quando essas grandezas forem adicionadas à expressão matemática a seguir:
ΔG = ΔH – T. ΔS
ΔG = x - T.(+y)
ΔG = x - T.y
O resultado do ΔG será totalmente dependente da temperatura. O processo só será espontâneo se o resultado da multiplicação da temperatura pela entropia for maior que o da entalpia, o que pode ocorrer em altas temperaturas.
c) Quando o ΔH for negativo (menor que zero) e o ΔS for positivo (maior que 0)
ΔH =-x
ΔS = +y
Quando essas grandezas forem adicionadas à expressão matemática a seguir:
ΔG = ΔH – T. ΔS
ΔG = -x - T.(+y)
ΔG = -x - T.y
O resultado do ΔG será negativo e, com isso, a reação será espontânea.
d) Quando o ΔH for negativo (menor que zero) e o ΔS for negativo (menor que 0)
ΔH =-x
ΔS = -y
Quando essas grandezas forem adicionadas à expressão matemática a seguir:
ΔG = ΔH – T. ΔS
ΔG = -x - T.(-y)
ΔG = -x + T.y
O resultado do ΔG será totalmente dependente da temperatura. O processo só será espontâneo se o resultado da multiplicação da temperatura pela entropia for maior que o da entalpia, o que pode ocorrer em altas temperaturas.