Potencial Químico
Análises Físico-Químicas
1 Potencial Químico
Em termodinâmica, potencial químico de um elemento, também conhecida como a energia livre parcial molar, é uma forma de energia potencial que pode ser absorvida ou libertada durante uma Reação química. Também pode ser importante durante uma Transição de fase. O potencial químico de uma espécie numa mistura pode ser definido como a inclinação da energia livre do sistema no que diz respeito a uma alteração no número de moles de apenas aquela espécie. Assim, é uma derivada parcial da energia livre no que diz respeito à quantidade da espécie, todas as outras concentrações de espécies presentes na mistura mantendo-se constante, e a uma temperatura constante. Quando a pressão é constante, o potencial químico é a Energia livre de Gibbs molar. Em condições de Equilíbrio químico ou em fase de equilíbrio, a soma total dos potenciais químicos é zero, assim como a energia livre está no mínimo.
Numa transformação, a pressão e temperatura constantes, a energia disponível para realizar trabalho designa-se por energia livre de Gibbs, G, ou função de Gibbs. O trabalho máximo que pode ser obtido da transformação é:
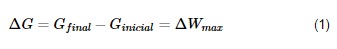
Onde ΔG é a variação da energia livre entre o estado final e inicial, e ΔWmax é o trabalho máximo que o sistema pode realizar (aparte o trabalho de expansão-compressão). Como o trabalho é feito à custa de G, a energia livre diminui, até que o sistema atinja o ponto de equilíbrio, perdendo a capacidade de produzir mais trabalho e a partir daí ΔG = 0. Dum modo geral, ΔG ≤ 0 para processos espontâneos, onde a igualdade indica o ponto de equilíbrio. Isto é, o sistema “resvala” num fosso de energia livre até atingir o fundo do fosso, ou seja, o equilíbrio. É claro que uma transformação pode ou não produzir trabalho, dependendo do modo como seja executada. Por exemplo, a reação de oxi-redução:
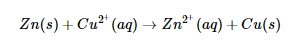
Pode realizar-se numa célula eletroquímica ou misturando diretamente os reagentes. Em ambos os casos ΔG ≤ 0, mas no primeiro é obtido trabalho elétrico, enquanto no outro a energia livre degrada-se em energia térmica (“calor”) sem a realização de trabalho. Na realidade, em qualquer transformação, há sempre degradação de energia (2ª lei da termodinâmica) donde ΔWmax é um limite superior praticamente inatingível.
Se o sistema tiver um único componente (gás, líquido ou sólido puros) o potencial químico, µ, é definido como a energia livre molar, a determinada pressão e temperatura:

Em que a energia livre, G, é uma função da pressão, p, da temperatura absoluta, T, e do número de moles n, ou seja, G = G (p, T, n).
Para sistemas com vários componentes, G = G (p, T, n¹, n², ...ni, ...), e o potencial químico de cada componente define-se como a energia livre molar parcial:
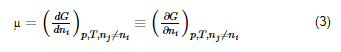
Que é a taxa de variação da energia livre causada por uma variação do número de moles do componente i, mantendo constantes a pressão, temperatura e o número de moles das outras espécies, isto é, a derivada parcial de G em ordem a ni.
Das propriedades físicas de G, pode estabelecer-se a expressão:
Que se reduz à definição (2) para um único componente.
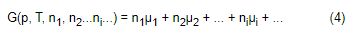
Equilíbrio de fases
Quando duas fases estão em equilíbrio os seus potenciais químicos, pressões e temperaturas são iguais. Suponhamos um líquido puro (l) e o seu vapor (v) num recipiente fechado a determinada temperatura. Se µ(l) > µ(v), o líquido vaporiza-se e a pressão do vapor aumenta até que a pressão de equilíbrio seja atingida e a partir desse ponto µ(l) = µ(v). Pelo contrário, se µ(l) < µ(v) o vapor condensa-se e a sua pressão diminuí até ao ponto de equilíbrio, admitindo que o vapor não se esgote. Dada a relação direta entre o potencial químico do vapor e o da fase condensada, a medição das pressões de vapor de equilíbrio é um dos métodos para determinar os potencias químicos das duas fases. As pressões de vapor relacionam-se também com a tendência de escape das moléculas de líquidos e sólidos para o estado gasoso. Estas relações foram essenciais para Lewis[5] introduzir as fugacidades e atividades com base nos potenciais químicos.
Síntese do amoníaco
A reação gasosa da síntese do amoníaco decorre segundo o esquema:
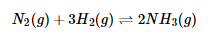
O potencial químico de NH3 é:
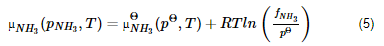
A fugacidade é uma pressão efetiva que traduz o desvio do gás real relativamente ao gás ideal; no gás ideal as forças intermoleculares são inexistentes e a fugacidade é igual à pressão. As forças atrativas tendem a congregar as moléculas diminuindo a sua tendência de escape, e as repulsivas tendem a dispersá-las aumentando essa tendência.
Se f < p, as forças dominantes são as atrativas e quando f > p as forças dominantes são as repulsivas. Se, porventura, f ≈ p, o potencial químico do gás real é aproximadamente igual ao do gás ideal à mesma pressão e temperatura. Da equação (5) conclui-se: (i) o potencial químico do amoníaco, a determinada pressão e temperatura, assim como a fugacidade, são independentes do estado padrão. Neste caso, apenas por conveniência, escolhe-se o gás ideal com pΘpΘ = 1 bar, mas podia escolher-se outro estado padrão, o que modificaria o primeiro termo do segundo membro da equação e o denominador do termo logarítmico, mas a soma dos dois termos manter-se-ia inalterada.
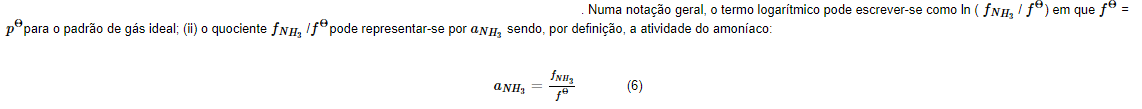
Por conseguinte, a atividade é a fugacidade relativa ao estado padrão. Se fΘ = 1 bar, como no caso presente, a atividade é numericamente igual à fugacidade, mas enquanto a fugacidade tem dimensões de pressão, a atividade é adimensional. A equação (5), como a de qualquer componente da mistura, pode ser reescrita em termos da atividade:
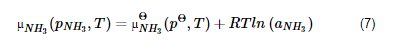
Como as equações (5) e (7) são equivalentes, utilizar uma ou outra forma é uma questão de preferência, desde que se saiba a fugacidade do estado padrão porque, segundo a definição (6), a atividade depende do estado padrão escolhido. Aliás, muitos autores utilizam apenas as expressões em termos das atividades.
Posto isto, analisemos a síntese do amoníaco, mantendo o formalismo das fugacidades. A diferença da energia livre entre o produto e os reagentes, de acordo com a expressão (4), é:
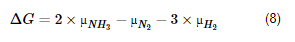
Introduzindo na equação anterior a expressão (5) e as expressões análogas para o nitrogênio e hidrogênio, deduz-se:
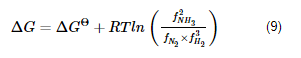

E a constante de equilíbrio da reação é:
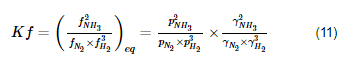


2 Ionização de ácidos
Um ácido monoprótico, HA, ioniza-se numa solução aquosa segundo a reação:
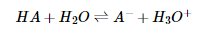
Da análise termodinâmica dos potenciais químicos, semelhante à do amoníaco, conclui-se que a definição exata da constante de equilíbrio da reação, em termos de atividades, é:
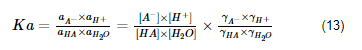


No âmbito das soluções eletrolíticas, é conveniente escolher estados padrão diferentes para o solvente e para o soluto.Já vimos que a escolha dos estados padrão é arbitária, não afetando os potenciais químicos das substâncias, numa determinada condição, e as respetivas fugacidades.

PH de soluções aquosas


3 Solubilidade
Solubilidade é a propriedade física das substâncias de se dissolverem, ou não, em um determinado líquido.Denomina-se soluto, os compostos químicos que se dissolvem em outra substância. O solvente é a substância na qual o soluto será dissolvido para formação de um novo produto.
A dissolução química é o processo de dispersão do soluto em um solvente, dando a origem a uma solução ou mistura homogênea.
Os solutos podem ser classificados em:
- Solúvel: são os solutos que se dissolvem no solvente.
- Pouco solúvel: são os solutos que apresentam dificuldade de se dissolver no solvente.
- Insolúvel: são os solutos que não se dissolvem no solvente.
Um princípio comum em solubilidade é: “semelhante dissolve semelhante”. Isso quer dizer que um soluto polar tende a se dissolver em um solvente polar. O mesmo é verdadeiro para substâncias apolares.
Veja alguns exemplos:
- Os hidrocarbonetos, apolares, apresentam pouca solubilidade em água, que é polar.
- O álcool (polar) é solúvel em água, mas não é solúvel em gasolina (apolar).
- A solubilidade dos sais é diferenciada. Eles podem ser classificados em: sal solúvel e sal praticamente insolúvel.
Coeficiente de Solubilidade
O coeficiente de solubilidade (Cs) determina a capacidade máxima do soluto que se dissolve em uma determinada quantidade de solvente. Isso, conforme as condições de temperatura.
Em resumo, o coeficiente de solubilidade é a quantidade de soluto necessária para saturar uma quantidade padrão de solvente a uma determinada condição.
Por exemplo, considere a seguinte situação:
Em um copo de água com sal (NaCl), inicialmente, o sal desaparece na água
Entretanto, se for adicionado mais sal, em determinado momento ele começará a se acumular no fundo do copo.
Isso acontece porque a água, que é o solvente, atingiu o seu limite de solubilidade e a quantidade máxima de concentração. A isso também chamamos de ponto de saturação.
O soluto que resta no fundo do recipiente e que não se dissolve é chamado de corpo de fundo ou precipitado.
Em relação ao ponto de saturação, as soluções classificam-se em três tipos:
- Solução insaturada: quando a quantidade de soluto é menor que Cs.
- Solução saturada: quando a quantidade de soluto é exatamente a mesma do Cs. É o limite de saturação.
- Solução supersaturada: quando a quantidade do soluto é maior que o Cs.
Produto de Solubilidade
Como vimos, a solubilidade representa a quantidade de soluto dissolvida em uma solução. O produto de solubilidade (Kps) é uma constante de equilíbrio diretamente relacionada com a solubilidade.
O seu cálculo permite determinar se uma solução é saturada, insaturada ou saturada com precipitado. Esse cálculo está relacionado com o equilíbrio de dissolução e a concentração de íons na solução.
Isso porque o produto da solubilidade refere-se ao equilíbrio de dissolução de substâncias iônicas.
Curva de Solubilidade
A capacidade de solubilidade química de uma substância submetida à alteração de temperatura não é linear. A variação da capacidade de solubilidade, em função da temperatura, é conhecida por curva de solubilidade.
A maioria das substâncias sólidas têm o seu coeficiente de solubilidade aumentado com o aumento da temperatura. Assim, a solubilidade de cada material ocorre de maneira proporcional, conforme a temperatura.Cada substância possui uma curva de solubilidade própria para um determinado solvente.
A variação de solubilidade é considerada linear quando não está sob influência da temperatura. Para conhecer a variação é preciso observar a curva de solubilidade.
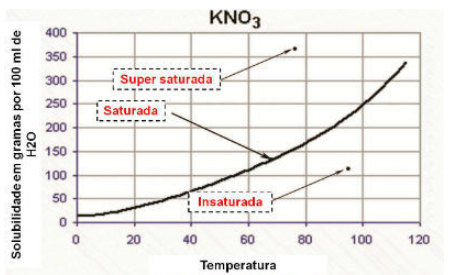
No gráfico, a curva de solubilidade demonstra que a solução é:
- Saturada: quando o ponto está sobre a curva de solubilidade.
- Insaturada: quando o ponto está abaixo da curva de solubilidade.
- Saturada homogênea: quando o ponto está acima da curva de solubilidade.
Fórmula do Coeficiente de Solubilidade
A fórmula para calcular o coeficiente de solubilidade é:
Cs = 100 . m1/m2
onde:
Cs:coeficiente de solubilidade
m1: massa do soluto
m2: massa do solvente
4 Eletrólito
Na química, o termo eletrólito refere-se genericamente a substâncias que em solução ou no estado fundido sofrem subdivisão em íons de suas moléculas. Substâncias que não se dissociam são chamadas de não-eletrólitos.
O termo "eletrólito" refere-se à capacidade de conduzir eletricidade através da intervenção de íons, uma característica peculiar dessas espécies químicas. Portanto, um eletrólito constitui o que é chamado de um condutor iónico ou, alternativamente, um condutor de uma segunda espécie. Os eletrólitos são capazes de conduzir a corrente elétrica, uma vez dissolvida em solução, precisamente por causa da presença de íons positivos e negativos gerados na solução, derivados da dissociação e ionização do eletrólito.
A condução não está ligada, neste caso, ao fluxo livre de elétrons dentro de uma estrutura cristalina, mas são os íons que se encarregam de "carregar" a corrente elétrica. Define um anfolito de um eletrólito com um comportamento anfotérico. As propriedades salientes dos eletrólitos são a condutividade iónica, as propriedades coligativas e o pH das soluções às quais dão origem.
Uma célula eletroquímica pode conter dois eletrólitos diferentes conectados eletricamente por uma ponte de sal ou por uma partição porosa; neste caso, o eletrólito em contato com o cátodo é chamado de católito, enquanto o eletrólito em contato com o ânodo é chamado anolito.
Exemplos de Eletrólitos
Quanto à natureza química, ácidos, bases e sais são eletrólitos. Do ponto de vista do estado de agregação, os eletrólitos podem ser subdivididos em:
- soluções eletrolíticas (por exemplo, ácido clorídrico e ácido sulfúrico);
- eletrólitos sólidos (por exemplo, & beta; - alumina, forma alotrópica de óxido de alumínio);
- sólidos iônicos (por exemplo, cloreto de sódio, iodeto de prata e fluoreto de cálcio);
- sais fundidos (por exemplo, nitratos alcalinos).
Eletrólitos Fortes e Fracos
Com referência a uma solução, um eletrólito forte está presente em uma única fase líquida no estado ionizado solvatado. Um eletrólito fraco é um eletrólito que só se dissocia na água parcialmente. Um eletrólito fraco tem um equilíbrio químico entre a forma molecular não dissociada e os íons que dela derivam pela dissociação. A dissociação aumenta se a solução for diluída. O grau de dissociação é um parâmetro que identifica o nível quantitativo de dissociação iónica.
Aplicações
Os eletrólitos são componentes essenciais de células eletroquímicas (incluindo células galvânicas e células eletrolíticas), onde têm a função de transportar a carga elétrica de um eletrodo para outro. Em uma célula eletroquímica, duas soluções eletrolíticas também podem estar presentes, separadas por um septo poroso ou por uma ponte de sal.
Os eletrólitos são usados dentro de capacitores particulares, chamados capacitores eletrolíticos.
Os eletrólitos também podem ser usados para realizar as operações da unidade de floculação (usado no tratamento de águas residuais) e permuta iónica (usado em amaciamento de água e em operações de cromatografia de permuta iónica).
Biologia
Os eletrólitos são essenciais para alguns processos biológicos, como a bomba de sódio e potássio. No sangue, e especificamente no plasma, está presente o sódio, potássio, fosfato, magnésio, ferro, cálcio e outros. Em medicina de diagnóstico, os parâmetros são medidos em exames de sangue com várias tecnologias, incluindo o eletrodo de membrana.