Cogumelos
Cultivo de Cogumelo e Champignon
1 Introdução
Os cogumelos comestíveis, sempre apreciados por seu valor gastronômico, vêm crescendo de importância nos últimos anos quanto à possibilidade de reciclar economicamente certos resíduos agrícolas e agro-industriais (CHANG & MILES, 1984).
Considerando também o elevado conteúdo protéico, seu cultivo tem sido apontado como uma alternativa para incrementar a oferta de proteínas, para países em desenvolvimento e com alto índice de desnutrição (CHANG & HAYES, 1980; CHANG et al., 1992; WUEST et al., 1987).
Além desses aspectos, a importância dos cogumelos também está ligada ao mercado em contínuo crescimento, aos avanços tecnológicos para melhorar a qualidade, produtividade e custo de produção, ao ainda baixo consumo “per capita” mesmo nos países mais desenvolvidos e, às ilimitadas opções de espécies que podem ser cultivadas.
As propriedades medicinais ou nutricêuticas de alguns cogumelos também vêm incrementando o seu valor agregado e, sob o ponto de vista empresarial, considera-se que o cultivo de cogumelos exige tecnologia e, portanto, constitui-se em atividade diferenciada e seletiva do ponto de vista técnico-econômico, pois, a diminuição dos custos de produção, pode representar um grande trunfo para o sucesso do empreendimento
O cultivo comercial de fungos comestíveis no Brasil restringe-se ao Agaricus bisporus, ao shiitake (Lentinula edodes) e, raramente, ao Pleurotus spp. Também são raros os relatos de pesquisas brasileiras no assunto sendo que o Instituto de Botânica de São Paulo foi um dos pioneiros, tendo criado em 1985 um Centro de Pesquisa de Cogumelos Comestíveis, em Mogi das Cruzes e, em 1986, foi criado um núcleo de ensino, pesquisa e extensão, na Faculdade de Ciências Agronômicas/UNESP, em Botucatu, denominado Módulo de Cogumelos.
Outros centros vêm surgindo em várias Universidades e Instituições de Pesquisa, tais como: UFRS, Porto Alegre, RS; UEL, Londrina, PR; UFLA – Lavras, MG; UFSC, Florianópolis, SC; EMBRAPA de Curitiba, PR e CENARGEN, Brasília, DF; UFPE, Recife, PE; e vários outros
Possivelmente pela falta de pesquisa, a produtividade brasileira de A. bisporus em Mogi das Cruzes, principal região de cultivo do Estado de São Paulo e do Brasil, ainda seja da ordem de 5 a 7 kg de cogumelos frescos/100 kg de substrato úmido (4 a 6 kg de cogumelos frescos/m2 ); na Europa, entretanto, a produtividade média do champignon é de 30 kg/ 100 kg de substrato.
Sistemas de cultivo
A escolha da tecnologia de cultivo e o preparo do substrato de cultivo dependem da espécie de cogumelo que se pretende cultivar, da disponibilidade e custo de resíduos agroindustriais e outros insumos e matérias primas e, de forma ainda mais óbvia, do custo de produção e mercado.
Basicamente, o cultivo de qualquer cogumelo pode ser realizado em condições naturais não assépticas ou sob condições axênicas isto é, com substrato submetido à esterilização e com as técnicas de cultivo assépticas até à colonização total do substrato pelo cogumelo.
Sob condições naturais não assépticas, os cogumelos podem ser cultivados em quatro grupos de substratos: em hospedeiros vivos (micorrízicos, ecologicamente dependentes e aqueles que causam doenças em essências florestais); substratos “in natura” com relação C/N maior que 100/1, tais como troncos de madeira sem qualquer preparação prévia (usados para o cultivo de shiitake, Pleurotus spp e fungos medicinais como o Ganoderma lucidum, Pycnoporus spp e outros); resíduos agroindustriais com relação C/N entre 50 e 100/1, tais como palhas pré-tratadas por compostagem curta e pasteurização severa (Pleurotus spp, Volvariela volvaceae e outros) ou apenas pasteurização severa, como no caso de cavacos de madeira obtidos pela trituração de galhos finos e/ou serragem fresca (shiitake, Auricularia sp e outros); e palhas e resíduos agroindustriais com relação C/N entre 25 e 50/ 1, com prévia compostagem (Fase I), pasteurização e condicionamento (Fase II), utilizados para o cultivo de Agaricus spp. (após o condicionamento a relação C/N estreita-se para 16 a 17/1).
Um outro padrão de substrato enriquecido com relação C/N entre 15 e 25/ 1, pode ser utilizado no sistema de cultivo de cogumelos sob condições axênicas, tais como o shimeji (Pleurotus ostreatus), o shiitake (Lentinula edodes), a Flamulina velutipes, Pholiota nameko e vários outros, incluindo quaisquer dos cogumelos normalmente cultivados sob condições naturais não assépticas.
A principal razão da utilização de substratos com estreita relação C/N no cultivo axênico é para obter-se elevadas produtividades visando cobrir os custos dos processos de esterilização e assepsia e, principalmente, para obter produções no tempo e quantidades requeridas pelo mercado consumidor, fato que às vezes não pode ser conseguido com o cultivo em condições naturais não assépticas, mormente quando se utiliza um baixo nível tecnológico de cultivo.
Preparo do composto e compostagem (Fase I)
Os cogumelos do gênero Agaricus possuem enzimas hidrolíticas da lignina (lacase), celulose e hemicelulose. Mas, deve-se fazer um parêntese para esclarecer que os cogumelos nutrem-se, e muito bem, de açúcares, mas, sob condições naturais não assépticas, se tais compostos estiverem presentes, é a microbiota mesofílica que prevalecerá no sistema e não permitirá a colonização do substrato pelo cogumelo.
Esta é a ideia pela qual, sob condições naturais, faz-se necessário o pré-tratamento do substrato pela compostagem, pasteurização e condicionamento do composto, para que se estabeleça uma microbiota responsável pela biostase favorável ao cultivo de cada cogumelo.
Na literatura se encontram diversas fórmulas de compostos os quais, de modo geral, podem ser divididos em: compostos clássicos, utilizando esterco equino, galinha e outros e, compostos sintéticos, cujas fontes de nitrogênio têm composição mais estável, possibilitando maior repetibilidade entre os ciclos de produção.
Os compostos clássicos ainda são muito utilizados pelo seu baixo custo e quando se emprega uma tecnologia de cultivo mais rústica. Desta forma, são praticamente ilimitadas as formulações dos “compostos” e, a título de exemplo, seguem alguns compostos sintéticos propostos por GIBBONS et al. (1991):
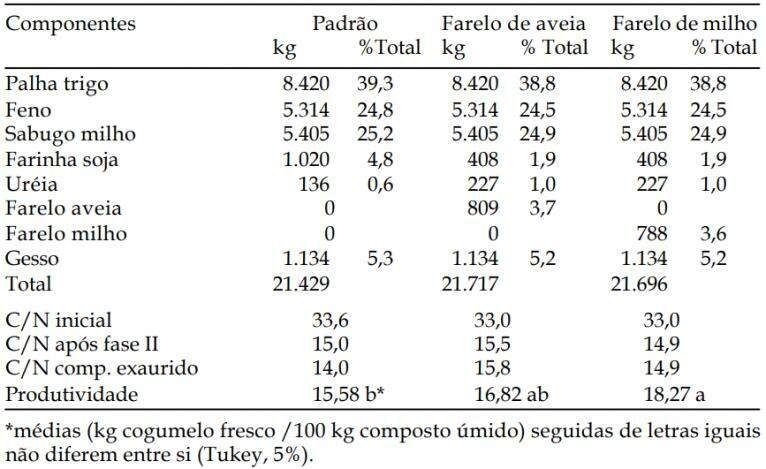
A formulação de “composto” para cultivo de cogumelos tem como primeira regra geral a escolha de materiais volumosos e fibrosos, à base de palhas de capim ou outras plantas, geralmente muito ricos em carbono (C) e pobres em nitrogênio (N) e fósforo (P).
Uma segunda regra geral para cultivo do Agaricus é que o composto deverá ser previamente corrigido com materiais concentrados em nitrogênio e fósforo, cuja composição deverá ser determinada por análises de amostras ou por consulta a valores relatados na literatura (EIRA & MINHONI, 1997), com a finalidade de atingir-se as relações C:N:P:30:1:0,2.
Usando como exemplo, considere-se os materiais na Tabela a seguir (disponíveis numa propriedade), para formular um composto para A. bisporus. Os cálculos podem ser efetuados manualmente (por tentativa) ou com auxílio de uma planilha eletrônica (MS Excel)1 , relacionada a um banco de dados com a composição de materiais concentrados e volumosos. O método leva em consideração o tipo de composto ou relação C/N a atingir, a disponibilidade e preço de materiais e a quantidade final desejada, considerando as perdas de 35% em matéria seca durante os processos de compostagem e condicionamento do composto.
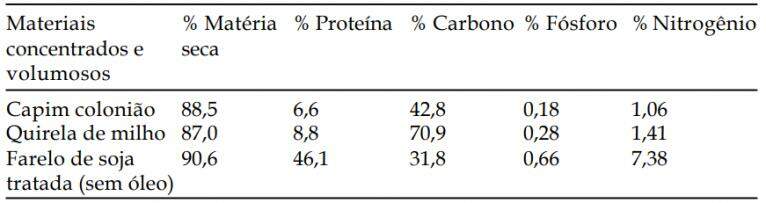
Sendo assim, para cada tonelada de capim (componente volumoso), pode-se combinar materiais concentrados e insumos visando atingir a relação C/N requerida (aproximadamente 30/1), tal como a fórmula específica transcrita na Tabela a seguir:
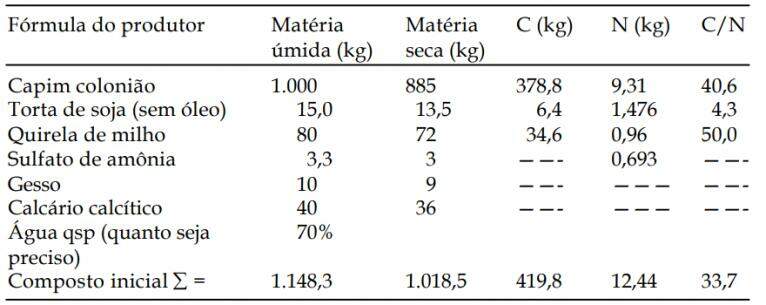
Planilha de cálculo desenvolvida no Módulo de Cogumelos, FCA/UNESP, pelo Químico Paulo Gustavo Celso (Doutorando em Biotecnologia, IQ/UNESP, Araraquara, SP e membro da equipe técnica do Módulo), 1999.
Além desses nutrientes principais, os micronutrientes K, S, Ca e alguns elementos-traço como o Mg, Mn, Zn, Bo, Co, Mo, etc, já estão presentes nos próprios componentes do composto, em quantidades que são suficientes ao metabolismo global da microbiota envolvida na compostagem (Fases I e II) e na nutrição do cogumelo (STANIER et al., 1969).
O gesso é importante para a estrutura do composto e eliminação do excesso de água e, o calcário, para garantir um efeito tampão durante a fase de produção.
De um outro lado, tecnologias de cultivo modernas vêm utilizando a suplementação do composto com materiais orgânicos concentrados em nitrogênio (VAN GRIENSVEN, 1988), como, por exemplo, o Champfood de uma companhia da Holanda2 , proposto para suplementação de substratos com relação C/N mais larga (até 50/1).
O produto é adicionado após a colonização total do substrato pelo cogumelo (a FASE III, nesta tecnologia envolve a incubação em túneis ou colonização em massa). O produto, à base de farelo de soja, é granulado e apresenta disponibilidade controlada, sendo incorporado à base de 1 a 1,4 kg/m2 de cama de cultivo (densidade de substrato entre 85 e 95 kg de substrato úmido/m2 ). Os resultados obtidos incrementaram a produtividade de A. bisporus (kg cogumelo fresco/m2 ), de acordo com a Tabela a seguir:
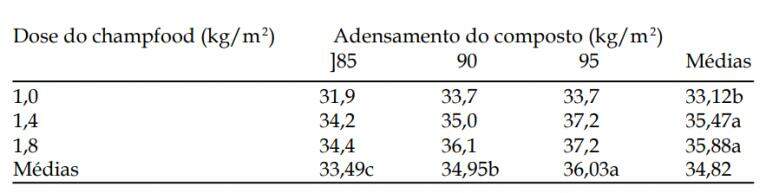
* Médias seguidas de letras iguais, não diferem estatisticamente (kg cogumelo fresco/m2 de cultivo).
Um aspecto importante é que, com a suplementação de substratos mais pobres (relação C/N inicial de até 50/1), pode-se chegar à produtividade de 34,82 kg de cogumelos frescos /m2 de cama de cultivo ou, em média, 38,7 kg de cogumelos frescos/100 kg de substrato úmido (100% maior que os resultados relatados por GIBBONS et al., 1991). Segundo VAN GRIENSVEN(1988), o farelo de soja tratado com formaldeído a 2% é um suplemento adequado a ser incorporado a compostos totalmente colonizados pelo cogumelo, à razão de 1 kg/m2 , obtendo-se produtividades de até 28 kg cogumelos frescos/m2 em relação às testemunhas (18 kg cogumelos frescos/m2 ).
Outros suplementos orgânicos com elevados teores de N (50%) vêm sendo testados e distribuídos por firmas da Europa.
Uma vez formulado o composto, monta-se a meda em camadas onde se distribui uniformemente os materiais da fórmula, que são umedecidos para iniciar-se a compostagem. Existem duas condutas na compostagem, mas que dependem da composição do substrato e regime de revolvimentos da meda.
Para substratos com relação C/N larga e/ou reviragens freqüentes a Fase I de compostagem pode ser completada entre 7 e 14 dias, processo também chamado de “short composting”. Em contraposição, substratos com relação C/N estreita e reviragens menos frequentes podem levar até 30 dias na Fase I.
Na meda de compostagem formada, desenvolvem-se atividades de comunidades microbianas, caracterizadas pela elevação de temperatura (60 a 80o C) e um desprendimento muito forte de amoníaco, resultante dos processos de mineralização do N orgânico (amonificação) que eleva o pH a índices acima de 9. Assim, a superfície da meda possui uma umidade baixa e condições máximas de aerobiose, ao passo que, na região central, as condições são parcialmente anaeróbias. Embora a maior parte do metabolismo na compostagem seja devido a fermentações, as transformações ideais ocorrem nas regiões onde predominam condições aeróbias que, impedem o estabelecimento de anaeróbios estritos, razão pela qual o composto deve ser revolvido com frequência, para que as condições sejam homogêneas em todo o material, até o final do tratamento.
Ao final da Fase I deve-se obter as seguintes características no substrato: umidade em torno de 70%; pH entre 7,5 e 8; coloração da palha de amarela a marrom, com manchas brancas de actinomicetos e outros microrganismos termófilos e uma redução no odor de amônia (STRAATSMA, 1994a e 1994b; STEINECK, 1987).
A palha também precisa perder a rigidez característica e o teor de umidade, entre 65 e 70%, pode ser medido na prática apertando-se uma porção do composto entre os dedos, sem escorrimento de água, mas tornando a palma da mão umedecida (EIRA & MINHONI, 1997).
2 Pasteurização (Fase II), inoculação e incubação (Fase III) Camada de cobertura, indução e frutificação (Fase IV)
A pasteurização para Agaricus spp nada mais é que a elevação da temperatura do composto a aproximadamente 62º C e tem a finalidade de promover o saneamento do composto, eliminando alguns microrganismos prejudiciais ao desenvolvimento do cogumelo e, concomitantemente, finalizar o processo de compostagem (condicionamento químico, físico e biológico).
As características do túnel e do processo de pasteurização encontram-se descritas em EIRA & MINHONI (1997). O pasteurizador deve possibilitar o controle da temperatura, através do sistema de ventilação, ajustando-se as proporções de reciclagem do ar quente (150 a 200 m3/t. h) e o ar novo e filtrado (10 a 40 m3/t. h), para que a temperatura eleve-se entre 60 e 65o C durante 6 a 8h e, a seguir, tenda à faixa entre 45 e 50o C, mantendo-se um regime de ventilação constante durante 5 a 7 dias (condicionamento), quando então se promove o resfriamento rápido para, a 25o C, efetuar-se a inoculação.
As características do túnel e do processo de pasteurização encontram-se descritas em EIRA & MINHONI (1997). O pasteurizador deve possibilitar o controle da temperatura, através do sistema de ventilação, ajustando-se as proporções de reciclagem do ar quente (150 a 200 m3/t. h) e o ar novo e filtrado (10 a 40 m3/t. h), para que a temperatura eleve-se entre 60 e 65o C durante 6 a 8h e, a seguir, tenda à faixa entre 45 e 50o C, mantendo-se um regime de ventilação constante durante 5 a 7 dias (condicionamento), quando então se promove o resfriamento rápido para, a 25o C, efetuar-se a inoculação.
Ao final dos processos de pasteurização e condicionamento, reduz-se a quantidade de carboidratos prontamente degradáveis, formando-se um complexo mais estável, lignina-humus; a quantidade de amônia torna-se menor que 10 ppm (mg/L); a relação C/N cai para 16; o pH altera-se para 7,5 e a umidade estabiliza-se em torno de 60 a 65% (VEDDER, 1979 e 1996).
Celso (1999), apresentou uma extensa revisão sobre a “seletividade” do composto. Num substrato “seletivo” o micélio do Agaricus crescerá de forma excludente em relação aos microrganismos competidores devido, provavelmente, à ausência de nutrientes facilmente assimiláveis como açúcares simples e aminoácidos (Eddy & Jacobs, 1976, citados por Ross & Harris, 1983a; Straatsma et al., 1989; Gerrits, 1988; Stolzer & Grabble, 1991). Quando o manejo de compostagem não transcorre corretamente, costumam aparecer, no período de colonização do Agaricus, fungos contaminantes (“weed molds”), também chamados “competidores”, que se nutrem do composto, elevam a temperatura (o Agaricus é inibido a partir de 28º C) ou produzem metabólitos tóxicos e, em consequência, reduzem o rendimento (Vijay & Gupta, 1994).
Tradicionalmente, os cultivadores associam um composto de qualidade à presença de actinomicetos, visíveis no composto na forma de micélio branco, referido como “fire fang”. VIJAY & GUPTA (1994), em trabalho de revisão sobre a microbiota do composto, citam que os actinomicetos Streptomyces e Micromonospora têm influência favorável no crescimento do Agaricus (o micélio cresce melhor e livre de contaminantes) além de estimulá-lo, pois produzem biotina, tiamina e vitaminas.
A associação entre o Agaricus e alguns fungos termófilos que se desenvolvem no final do condicionamento do composto está sendo estudada, inclusive no Brasil, com a finalidade de inoculação desses microrganismos no início da Fase II, como um trunfo na obtenção de compostos de boa qualidade (Celso, 1999).
Ross & Harris (1983a, 1983b) argumentam que alguns fungos termófilos dominam o final do processo levando ao desaparecimento da amônia, que é muito tóxica ao Agaricus, e ao declínio da termogênese. No resfriamento a 25º C para a inoculação do Agaricus, ficariam numa condição inativa ou estática, numa temperatura próxima ou abaixo da mínima de crescimento; a estrutura celular desta biomassa permaneceria intacta e seu conteúdo não assimilável, exceto para microrganismos como o Agaricus, com sistemas enzimáticos aptos à oxidação deste material.
Ross & Harris (1983a) relataram que o fungo termófilo Torula thermophila Cooney & Emerson stimulou o crescimento do Agaricus e suprimiu competidores, além de acelerar o desaparecimento da amônia. Outros microrganismos termófilos, citados por Straatsma et al.(1994a) como sendo estimuladores do micélio de Agaricus em composto esterilizado, são os seguintes: Chaetomiumthermophilum, Chaetomium sp., Malbranchea sulfurea, Myriococcum thermophilum, Stilbella thermophila, Thielavia terrestris e dois basidiomicetos não identificados.
Uma outra tecnologia que visa abreviar e reduzir as perdas durante a compostagem, é o método “ Indoor” que alia as vantagens acima citadas e vem sendo testado com sucesso, normalmente com índices de 100% de eficiência biológica, desde meados da década de 80 em países europeus e na Austrália. A tecnologia é emergente e reúnem as Fases I e II convencionais num único sistema de 6-7 dias, num mesmo túnel. Entre as fases do processo, é introduzido um “ativador biológico” apropriado, que influencia diretamente a Fase II e, consequentemente, o rendimento.
Dependendo do nível tecnológico, a inoculação pode ser feita manualmente em sacos de polietileno perfurados (furos de ½” distanciados 20 cm) ou em caixas de cultivo ou ainda em camas dispostas em prateleiras. A “semente” é utilizada à razão de 1 a 2% da massa de composto em base úmida.
O desenvolvimento do micélio ocorre dentro de um prazo variável, de acordo com o tipo de inóculo, qualidade do composto e condições da câmara de cultivo, mas, de maneira geral, oscila entre 14 e 21 dias, quando fica nítida a ocorrência de uma teia branca, lembrando um emaranhado de fios de seda sobre a superfície do composto, momento em que se procede à cobertura do substrato colonizado com solo ou outros materiais (“casing”).
Modernamente, a Fase III ou “corrida do micélio”, que também é efetuada em massa sob condições de temperatura e aeração controladas em túneis de cultivo (Van Griensven, 1988), similares aos túneis de pasteurização, com reciclagem, resfriamento (temperatura controlada entre 24 e 25º C) e renovação do ar (cerca de 2 a 3 vezes o seu volume por dia, uma vez que nesta fase os teores de CO2 permanecem muito elevados).
A camada de cobertura é um dos principais fatores para incrementar a produtividade, qualidade e uniformidade na colheita do “champignon” (Amsing & Gerrits, 1991). A função da cobertura com solo ou, preferencialmente com turfa, ainda não se encontra perfeitamente esclarecida, mas são apontadas as seguintes finalidades (Fermor, 1993): prevenir a secagem excessiva do composto; oferecer um sustentáculo para a formação dos basidiocarpos; permitir a irrigação da cama, sem que o composto seja umedecido em excesso; fornecer alguns nutrientes ao cogumelo, como por exemplo, elementos-traço; induzir o micélio fúngico a frutificar por uma ação de resfriamento, devido à evaporação de água na superfície.
Modernamente, utiliza-se uma mistura de turfa negra ou “black peat” e turfa fibrosa marrom ou “brown peat”, neutralizada com carbonato de cálcio ou calcário calcítico. A camada de cobertura deverá ser submetida a processos de pasteurização ou desinfecção com vapor ou formol para evitar nematóides e outros problemas da fungicultura.
A presença de bactérias na camada de cobertura é essencial para a indução da frutificação do cogumelo (Rainey , 1990). Dentre essas bactérias, a Pseudomonas putidaparece promover a remoção de compostos auto-inibitórios produzidos pelo cogumelo, facilitando a frutificação.
Existem várias técnicas utilizadas para o aumento da produtividade que se relacionam ao manejo da camada de cobertura. Uma técnica usada na Europa, com significativo aumento e uniformidade de produção, consiste na inoculação da cobertura com composto colonizado com a mesma semente que inoculou o substrato de produção, processo este conhecido como “ spawned casing” (Gupta et al., 1989; Gupta et al., 1993; Maccanna, 1983).
Outra técnica é o “ruffling”, que consiste na mistura da camada de cobertura já parcialmente colonizada com um pouco do composto colonizado imediatamente abaixo com o auxílio de escarificador (Maccanna, 1983). Há ainda o “ranking” que consiste em remexer a cobertura já colonizada para que esta se fracione em torrões (Bononi et al., 1995). Após utilizar estas técnicas é preciso esperar mais alguns dias para que o micélio se recomponha e, então, deve-se aumentar a ventilação e reduzir a temperatura para a indução dos primórdios.
No Brasil, a expansão do cultivo do “champignon” não foi acompanhada pelo desenvolvimento tecnológico e, consequentemente, continua-se com baixa produtividade. As principais razões são a má qualidade do composto, da camada de cobertura (geralmente solo) e a rusticidade das instalações de cultivo que agravam a incidência de pragas e doenças, pois as câmaras de cultivo não são climatizadas (Figueiredo & Mucci, 1985; Fletcher, 1986).
As mais modernas instalações possuem câmaras totalmente climatizadas (controle independente da temperatura, UR, teor de CO2 e de O2 , nível de aeração e reciclagem do ar), controladas por softwares e hardwares que comandam as unidades de manejo do ar, em cada Fase de cultivo. Algumas “fazendas de cogumelos” na Holanda possuem colheita mecânica, fato que exige o mais elevado índice de tecnologia em todas as demais fases do cultivo que precedem a colheita (Vedder, 1979 e1996; Van Griensven, 1988).