Anemia: definição, epidemiologia, fisiopatologia, classificação e tratamento
Noções Básicas em Auxiliar de Laboratório de Hematologia Clínica
1 Definição de Anemia:
A anemia é uma condição patológica em que ocorre diminuição da massa de hemoglobina e da massa eritrocitária. A redução da concentração de hemoglobina (Hb), em si, não define a anemia, pois esse achado pode ocorrer em situações fisiológicas, como a que se observa a partir do segundo trimestre da gestação, principalmente por volta da 24ª semana, atribuída à hemodiluição. Ainda assim, para fins práticos, a concentração da hemoglobina (ou o hematócrito) é o parâmetro laboratorial mais utilizado para definir o quadro de anemia.
A primeira etapa na avaliação do paciente é estabelecer se ele de fato tem anemia. A Organização Mundial da Saúde (OMS) define anemia como a concentração de Hb inferior a 12 g/dL para mulheres pré-menopausa e inferior a 13,0 g/dL para homens e para mulheres na fase pós-menopausa, ambos os valores considerados para o nível do mar.
A recomendação de adotar o valor de 13,0 g/dL como limite inferior para homens motivou muitas críticas, que o consideraram muito baixo1. Esses autores propõem limite inferior de 13,7 g/dL para homens caucasianos com idade entre 20 e 59 anos e de 13,2 g/dL para aqueles com 60 anos ou mais; e de 12,2 g/dL para mulheres com 20 anos ou mais. Para afrodescendentes adultos, os valores dos limites inferiores recomendados são de 12,9 g/dL (20-59 anos) e de 12,7 g/dL (≥ 60 anos) para homens e de 11,5 g/dL para mulheres com mais de 20 anos. A possível explicação para o estabelecimento de valores ligeiramente inferiores para afrodescendentes é a alta prevalência nessa população da talassemia α. Ademais, como se pode observar, aceitam-se valores mais baixos de concentração da Hb para homens mais idosos, mas não para mulheres. A explicação para esse fenômeno advém da constatação de que homens idosos apresentam leve queda da concentração da Hb com a idade avançada, que chega a aproximadamente 1,0 g/dL nos octogenários, queda essa atribuída à redução dos níveis de testosterona observada no homem idoso.
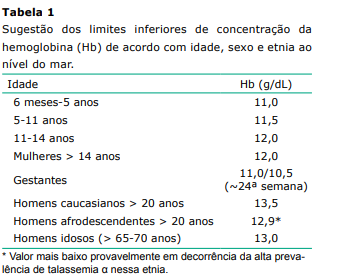
Os parâmetros da normalidade da concentração da Hb em crianças e em adolescentes também diferem daqueles observados nos adultos. Por exemplo, entre os 6 meses e os 5 anos, o limite inferior é de 11,0 g/dL; entre 6 e 11 anos, de 11,5 g/dL; entre 12 e 14 anos, de 12,0 g/dL, valor que se mantém para as mulheres a partir de então. Para os adolescentes do sexo masculino, o limite inferior é mais difícil de determinar diante da variabilidade dos níveis de testosterona para cada idade até o final da adolescência (Tabela 1).
A altitude é importante fator de influência nos níveis de concentração da Hb, especialmente nas regiões de colonização relativamente recente, como nos Andes e nas Montanhas Rochosas da América do Norte. A aclimatação recente se dá por aumento da concentração da Hb, enquanto a aclimatação de longo termo (ex. região do Himalaia) é essencialmente de caráter genético, sem aumento da concentração da Hb. Os níveis de O2 no sangue arterial não se alteram significativamente até a altitude de aproximadamente 2.500 m, a partir da qual ocorre a sua redução linear à medida que aumenta a altitude. Nos Andes, população que vive em altitude de 3.500-4.000 m apresenta Hb de aproximadamente 4,0 g/dL mais alta que a observada em indivíduos que habitam ao nível do mar ou na mesma altitude no Himalaia, região de colonização mais antiga. Isto posto, é de difícil determinação os limites da normalidade da concentração de Hb nas diferentes altitudes, até porque, nos dias atuais, há grande mobilidade das pessoas entre as diversas regiões, eventualmente em diferentes altitudes, cujo impacto na concentração de Hb é ainda em grande parte desconhecido.
Além da idade, do sexo e da altitude, outros fatores também podem influenciar os níveis de concentração da Hb, como o tabagismo, a idade gestacional e o índice de massa corporal.
2 Epidemiologia:
A prevalência da anemia varia de acordo com a região e com a situação econômica dos diferentes países. Por exemplo, a anemia falciforme e a talassemia β são mais prevalentes na África equatorial e na bacia do Mediterrâneo, respectivamente, mas também são encontradas em países como o Brasil, que receberam imigrantes dessas regiões.
Segundo estimativa da OMS, a anemia acometia, entre 1993 e 2005, aproximadamente um quarto da população mundial, o que correspondia então a 1,62 bilhão de pessoas afetadas, sendo a maioria crianças com menos de quatro anos. Publicação recente mostrou decréscimo da prevalência de anemia entre 1990 e 2010 de 40,2% para 32,9% da população mundial, especialmente nos homens. As regiões mais afetadas pela anemia foram o Sudeste da Ásia e a África subsaariana. A deficiência de ferro foi sua principal causa, e as crianças com menos de 5 anos eram as mais afetadas. Malária, esquistossomose e insuficiência renal crônica foram as causas de anemia cuja prevalência mais aumentou nesse período.
No Brasil, os dados são incompletos. Estudo realizado em 1.111 crianças, de 6 meses a 10 anos, em cidade do interior do Acre, mostrou prevalência de anemia em 13,6%, de anemia ferropriva em 10,3% e de deficiência de ferro em 45,4% dos indivíduos6. Dois estudos em populações indígenas mostraram anemia em 62,3% e 80,6% das crianças das tribos terena (Mato Grosso do Sul)7 e suruí (Rondônia/Mato Grosso)8, respectivamente. Um estudo mais abrangente do Ministério da Saúde mostrou que 20,9% de 3.499 crianças com menos de 5 anos de idade e 29,4% de 5.698 mulheres apresentavam anemia (Hb < 11,0 g/dL e Hb < 12,0 g/dL para crianças e para mulheres, respectivamente). A Região Nordeste foi a que apresentou maior prevalência de anemia nas crianças (25,5%) e nas mulheres (39,1%)9. Outra publicação recente, entretanto, mostrou prevalência de apenas 2,2% de anemia (Hb < 11,5 g/dL) em crianças de 8 a 12 anos de idade na região metropolitana de Curitiba (PR), o que põe em relevo as diferenças regionais num país heterogêneo como o Brasil.
No caso da anemia falciforme, a doença monogênica mais comum no Brasil, observa-se distribuição heterogênea, a depender da composição étnica da população de cada região. A maior prevalência da HbS é observada na população do Nordeste (10%), enquanto a menor, na população da Região Sul do país (2%). Estima-se o nascimento de uma criança com anemia falciforme para cada 1.000 a 3.000 nascimentos, o que perfaz um total de aproximadamente 3.500 casos novos por ano. Aproximadamente dez anos atrás, o número de pacientes com anemia falciforme era estimado em 25.000 a 30.000.
3 Fisiopatologia:
Cada tipo de anemia tem suas caraterísticas fisiopatológicas específicas, cuja explanação foge do escopo deste artigo. Entretanto, vale a pena discutir aspectos fisiopatológicos comuns a todos os tipos de anemia. A hemoglobina é a proteína que transporta o oxigênio dos pulmões aos tecidos. A captação e a liberação do oxigênio pela hemoglobina são influenciadas por: temperatura, pH, concentração de CO2 e quantidade de 2,3-DPG. A curva de dissociação da oxi-hemoglobina mostra a correlação da saturação de O2 com a pressão parcial de O2 e o conteúdo de Hb12. Redução da massa de hemoglobina pode acarretar diminuição significativa da capacidade de transporte de O2 e de sua liberação para os tecidos, que se torna mais evidente em condições de aumento súbito da demanda. A queda da concentração da Hb leva à mobilização pelo organismo de mecanismos compensatórios, tais como, aumento do débito cardíaco, redistribuição do fluxo sanguíneo para órgãos vitais, aumento do influxo de líquido do espaço extravascular para o intravascular, entre outros, mecanismos esses acionados de maneira menos efetiva nos indivíduos idosos ou debilitados.
Estudos em animais mostraram as alterações fisiológicas que ocorrem quando anemia dilucional isovolêmica é provocada de maneira controlada. Por exemplo, estudo em camundongos mostrou que começavam a ocorrer óbitos apenas quando a concentração de Hb caía a níveis inferiores a 5,0 g/dL e atingia 100% dos animais quando a Hb era inferior a 2,0 g/dL. Resultados semelhantes foram observados em porcos e babuínos13. Em humanos previamente saudáveis submetidos a anemia dilucional isovolêmica, não se observaram sinais de hipóxia tecidual com Hb de 5,0 g/dL. É importante enfatizar que os animais e os humanos submetidos a anemia induzida eram todos saudáveis e foram mantidos em repouso. Portanto, não se podem extrapolar as conclusões obtidas em condições clinicamente controladas para a situação que ocorre, por exemplo, no trauma cirúrgico, em que seriam de esperar demandas fisiológicas adicionais, possivelmente mais difíceis de atender com Hb de 5,0 g/dL.
Alguns estudos observacionais feitos nos EUA mostraram as consequências da anemia pós-operatória em pacientes que recusaram a transfusão de hemácias por crença religiosa (testemunhas de Jeová). Os dois mais importantes revelaram baixa morbimortalidade para a faixa de Hb entre 7,0-8,0 g/dL, mas que aumenta progressivamente à medida que diminui a concentração de Hb, sendo de 2,0 a 2,5 vezes para cada grama a menos de Hb, atingindo mortalidade de 100% a mortalidade no grupo de indivíduos com Hb menor ou igual a 2,0 g/dL. A capacidade de tolerar relativamente bem concentrações de Hb de 7,0-8,0 g/dL serviram de guia para a delineação de projetos de pesquisa clínica em que se adotaram gatilhos transfusionais mais ou menos restritivos em situações clínicas específicas.
4 Classificação da Anemia:
A anemia pode ser classificada em aguda e crônica, quanto ao tempo de instalação; decorrente da diminuição da produção (hipoproliferativa) ou do aumento da destruição dos eritrócitos (perda ou hemólise), quanto à causa e em normocítica/normocrômica, macrocítica e microcítica/hipocrômica, quanto ao volume corpuscular médio (VCM) (Tabela 2). Essa última maneira de classificar as anemias confere a vantagem prática de guiar o médico com respeito à investigação de sua causa, até porque, além do quadro clínico, o médico em geral dispõe, numa fase inicial, do hemograma, com os valores hematimétricos e as contagens de células das outras séries (leucócitos e plaquetas), o que também é útil para estabelecer o diagnóstico.

5 Manifestações Clínicas e Diagnóstico:
As manifestações clínicas da anemia são variáveis e dependem da etiologia, da gravidade, da velocidade de instalação, das eventuais comorbidades e dos mecanismos compensatórios que o paciente foi capaz de mobilizar. As queixas mais comumente observadas são astenia, dispneia e palpitações, especialmente aos esforços, que se acentuam à medida que a anemia se intensifica. Também são relativamente comuns queixas de tontura, cefaleia, zumbidos, claudicação intermitente e angina pectoris nos pacientes com doença arterial aterosclerótica. Queixas específicas também podem ocorrer em diferentes tipos de anemia, por exemplo, a perversão do apetite (pica) na anemia ferropriva e queixas neurológicas na anemia por deficiência de cobalamina.
Ao exame físico, o paciente, em geral encontra-se pálido. Pode-se ainda observar hipotrofia das papilas da língua nas anemias ferropriva e megaloblástica, edema maleolar, entre outros sinais. A icterícia e a esplenomegalia são sinais sugestivos de anemia hemolítica ou de anemia megaloblástica. Outros achados podem sugerir síndromes de falência ou infiltração da medula óssea (MO), como a presença de petéquias e a febre.
Dentre os exames a ser solicitados, o hemograma é o mais importante, pois ele permite classificar a anemia de acordo com sua a intensidade e com o volume corpuscular médico (VCM) das hemácias, além de mostrar as contagens de leucócitos, assim como a sua morfologia (ex. pleocariócitos e bastonetes gigantes nas anemias megaloblásticas), e de plaquetas (reduzida na falência ou infiltração da MO e na anemia megaloblástica, entre outras). A contagem de reticulócitos também é importante, pelo menos para o diagnóstico, pois contribui para definir a magnitude da eritropoese, ou seja, se se trata de causa de origem central (anemia hipoproliferativa-reticulocitopenia) ou de destruição ou perda de eritrócitos (reticulocitose). Outros exames também podem ser úteis, como o aumento da concentração sérica da bilirrubina não conjugada (indireta) e da desidrogenase lática nas anemias hemolíticas e nas anemias megaloblásticas (a última também está elevada nas leucemias agudas).
O diagnóstico das anemias carenciais não costuma apresentar dificuldade na maioria dos casos. Na anemia ferropriva, observa-se redução da saturação da transferrina e da concentração da ferritina sérica. Na anemia da doença inflamatória crônica, a saturação da transferrina também é baixa, mas vem comumente associada ao aumento da concentração da ferritina sérica (também pode estar normal) (Tabela 5). Nas anemias megaloblásticas, as concentrações de cobalamina (vitamina B12) ou de ácido fólico estão comumente reduzidas. Contudo, na anemia megaloblástica por deficiência de cobalamina, seus níveis séricos podem estar dentro da faixa de normalidade, que é muito ampla, mas, em geral, próximos de seu limite inferior (200-300 pg/ mL). Nesses casos, concentração elevada da homocisteína (também elevada na deficiência de folato, na insuficiência renal e no hipotireoidismo) e do ácido metilmalônico (sensível, mas pouco acessível na prática clínica) podem contribuir para definir o diagnóstico de carência de vitamina B12. Pode-se ainda dosar a cobalamina ativa, ligada à transcobalamina (holotranscobalamina), que é a que de fato importa (é inativa quando ligada à haptocorrina), cujo resultado é mais fidedigno da sua deficiência. Entretanto, a dosagem da forma ativa também é pouco acessível na prática clínica. A deficiência de folato também pode cursar com nível sérico normal desse nutriente. A sua dosagem nas hemácias é mais fidedigna da deficiência de folato, apesar de não ser tão automatizável quando a sua dosagem no soro, e, por isso, menos reprodutível de um laboratório a outro. Esse também é um exame pouco disponível na prática clínica.
Além dos exames mencionados, outros também podem ser necessários, a depender da hipótese diagnóstica, por exemplo, a análise do aspirado e biópsia de MO para o diagnóstico da anemia aplástica ou da leucemia aguda; os exames de imagem (esplenomegalia), etc.
6 Tipos mais prevalentes de anemia:
Anemia ferropriva
A anemia ferropriva (AF) é a condição mais exacerbada da deficiência de ferro, que a precede e a suplanta em prevalência. A rigor, a deficiência de ferro afeta todo o organismo, não apenas a eritropoese e o transporte de oxigênio, uma vez que o ferro é constituinte de todas as células e tecidos, como, por exemplo, os músculos, cuja proteína mioglobina também contém o grupo heme.
A AF, como mencionado anteriormente, é a mais prevalente das anemias, e afeta mais de um bilhão de pessoas em todo o mundo. Na AF, ocorre uma série de mecanismos compensatórios da anemia, desde os cardiovasculares, comuns a todo tipo de anemia, até os mais específicos, como a redução da síntese do hormônio hepcidina, que resulta em aumento da absorção de ferro, que tem lugar no duodeno. A maioria dos casos de AF decorre de perda aumentada de sangue ou da demanda aumentada por ferro, observada na infância, especialmente nos lactentes prematuros, na adolescência e na gestação. Nos adultos, presume-se que a AF decorra de perda de sangue, especialmente na menstruação. Nos homens e nas mulheres após a menopausa, é recomendável investigar sangramento por trato gastrointestinal, que pode ser oculto e assintomático.
Causas de AF, ou de deficiência de ferro muito observadas nas duas últimas décadas são o uso prolongado de inibidores da bomba de prótons e a cirurgia bariátrica, que podem acarretar má absorção do ferro. Não é comum a deficiência por falta de ingestão desse metal, exceto em crianças em regime alimentar restrito ao leite por períodos prolongados, pois o leite é relativamente pobre em ferro. Em resumo, a AF é sempre decorrente de uma condição clínica subjacente, que deve ser investigada (Tabela 3).

O quadro clínico já foi descrito acima e, em essência, não difere do de outros tipos de anemia, com a exceção da perversão do apetite, como também já foi mencionado. O diagnóstico é relativamente fácil na maioria dos casos. O grau de anemia é variável, mas pode ser intenso; as características morfológicas são de anemia microcítica e hipocrômica, exceto quando leve, em que o VCM pode estar dentro da faixa de normalidade, em geral, mais próximo do limite inferior. A série leucocitária não costuma estar alterada, no entanto, percentagem significativa (~30%) dos pacientes apresenta plaquetose ou concentração de plaquetas próxima do limite superior da normalidade, especialmente quando a AF decorrer de sangramento. O ferro sérico está diminuído ou normal e a transferrina costuma estar aumentada, o que resulta em saturação reduzida da transferrina (< 15%); a ferritina sérica está reduzida, mas pode estar dentro da faixa de normalidade em caso de a AF estar associada ou ser secundária à anemia da doença inflamatória (Tabela 4).
Outro diagnóstico diferencial é com a talassemia menor. Entretanto, essa condição não costuma acarretar queixas, e cursa com microcitose e hipocromia acentuadas, desproporcionais ao grau de anemia, que é leve, por causa da elevada concentração de hemácias, às vezes, acima da faixa da normalidade. Além disso, indivíduos com talassemia menor costumam ter níveis relativamente elevados (> 100 ng/mL) de ferritina sérica, com saturação normal ou pouco elevada da transferrina (Tabela 4). A medida do grau de anisocitose (RDW, do inglês red cell distribution width) em geral mostra valores dentro ou próximos da normalidade, o que não costuma ocorrer na AF, por exemplo.
O tratamento padrão é a suplementação de sal de ferro por via oral, na dose de 50-200 mg/dia de ferro elementar (o ferro elementar corresponde a 20% da massa do sulfato ferroso) para indivíduos adultos. Em caso de intolerância ao sal de ferro oral ou por suposta ou confirmada má absorção, pode-se administrar ferro por via parenteral (sacarato de hidróxido férrico ou carboximaltose férrica). A suplementação de ferro deve ser feita até a normalização da concentração de Hb e das reservas de ferro (ferritina).
Anemia da doença inflamatória
A anemia da doença inflamatória (ADI), também conhecida como anemia da doença crônica, é a segunda mais prevalente nos pacientes com anemia (a primeira é a anemia ferropriva) e a primeira em pacientes internados ou com doença crônica. A ADI ocorre em doenças que causam ativação imune e inflamação, tais como infecção crônica, doenças autoimunes e câncer. Mais recentemente, outras condições clínicas também foram identificadas como causadoras da ADI, como a doença renal crônica, a insuficiência cardíaca congestiva, a doença pulmonar crônica e a obesidade (Tabela 4).

A fisiopatologia da ADI envolve pelo menos três mecanismos principais:
1) restrição à mobilização do ferro de seus depósitos, principalmente nos macrófagos, mas que também diminuem a sua absorção intestinal;
2) supressão da eritropoese pelos mediadores da inflamação e, por fim,
3) redução da sobrevida das hemácias. O primeiro mecanismo envolve incremento da produção da interleucina (IL)-6, entre outros, que estimula os hepatócitos a aumentar a produção da hepcidina, o principal regulador da homeostase do ferro. A hepcidina liga-se à ferroportina (única “porta” conhecida pela qual as moléculas de ferro podem ser transportadas do interior dos macrófagos e dos enterócitos para a circulação, onde se ligam à transferrina), o que leva à sua internalização e degradação, de modo que o ferro fica aprisionado em seus locais de depósito e, portanto, menos disponível para a eritropoese.
O segundo mecanismo decorre da redução da produção da eritropoetina (EPO), assim como da redução da resposta à sua ação. Por fim, o terceiro mecanismo, mas menos importante que os dois anteriores, é a redução da sobrevida dos eritrócitos, atribuída a eritrofagocitose aumentada, tanto pelos macrófagos do fígado quanto do baço.
O diagnóstico da ADI às vezes é dificultado por sua concomitância com a deficiência de ferro, ou de outro nutriente, com a hemorragia, ou pelo fato de o fenômeno inflamatório não ser evidente.
Os sintomas e sinais são similares aos das outras anemias, entretanto, é comum haver no quadro clínico características específicas da doença de base, por exemplo, artrite (artrite reumatoide), linfadenomegalia (linfoma, tuberculose), etc. Laboratorialmente, a anemia da ADI se caracteriza por ser leve a moderada (Hb ≥ 8,5-9,0 g/dL) e normocítica (VCM: 80-100 fL) e normocrômica. Observam- -se ainda hipoferremia, hipotransferrinemia (saturação da transferrina < 20%) e hiperferritinemia (a ferritina é proteína de fase aguda, de modo que seus níveis séricos aumentam na inflamação) (Tabela 5).
Além disso, observam-se com frequência aumento da velocidade de hemossedimentação, dos níveis séricos da proteína C reativa e do fibrinogênio e aumento policlonal das gamaglobulinas. Além desses exames, é importante investigar a causa da anemia, que pode não ser evidente num primeiro momento. Então, recomenda-se avaliar as funções renal, hepática e tireoidiana (o hipotireoidismo é causa de anemia leve a moderada) e dosar a vitamina D, que exerce regulação negativa sobre a produção de hepcidina, de modo que indivíduos com hipovitaminose D podem apresentar anemia, em geral de leve intensidade. A dosagem da hepcidina, cuja concentração sérica estaria elevada, não é realizada na prática clínica.
O tratamento da ADI é principalmente o tratamento da doença de base. Eventualmente, pode ser útil o uso da eritropoetina, especialmente em pacientes idosos e com comorbidade que torne mais difícil ou impossível ao paciente mobilizar os mecanismos compensatórios da anemia, como, por exemplo, a insuficiência cardíaca. Entretanto, o uso da eritropoetina pode acarretar complicações como hipertensão arterial e levar a aumento do risco de trombose. A administração de composto de ferro também pode trazer benefício, mesmo com valores de ferritina dentro da faixa de normalidade e mesmo sem o aumento da concentração de Hb, como já foi descrito.
A transfusão de hemácias raramente é necessária, até porque a concentração de Hb não costuma ser muito baixa no paciente com ADI. Sua indicação deve se limitar a situações emergenciais.

Anemia na gestação
A anemia na gestação é um conhecido problema de saúde pública, pois acomete mais de 50% das gestantes na África, 40% na Ásia, 30% na América Latina, 18,7% na Europa e 6% na América do Norte21. Durante a gestação, ocorre o fenômeno da hemodiluição, decorrente do aumento da volemia plasmática de até 50%, enquanto o aumento da massa eritrocitária chega a aproximadamente 25%, o que explica queda da concentração de Hb. Por isso, adota-se valor mais baixo de concentração de Hb (10,5-11,0 g/dL) como limite inferior da normalidade (Tabela 1 presente nos capítulos anteriores).
Das causas de anemia na gestação, a mais comum é a deficiência de ferro. A gestação requer uma quantidade adicional de ferro de mais de 1.000 mg, dos quais 350 mg para o feto e a placenta, 500 mg para a expansão da massa eritrocitária e 250 para as perdas do parto, aproximadamente. A necessidade diária de ferro aumenta de 0,8 mg no início da gestação para 7,5 mg no terceiro trimestre, o que supera a absorção diária (1-5 mg). Portanto, as gestantes têm de mobilizar ferro de suas reservas, que, quando não são suficientes, resultam em anemia. As pacientes sob maior risco são as multigestas, as que tiveram gestação menos de um ano antes, as adolescentes, as vegetarianas e as que têm história de perdas menstruais aumentadas.
A anemia ferropriva no início da gestação, além dos efeitos diretos sobre a gestante, está associada a maior risco de parto prematuro e de neonato com déficit ponderal ao nascimento. Portanto, seu diagnóstico e tratamento precoces devem fazer parte de programa de seguimento pré-natal. O tratamento da anemia ferropriva em gestante não difere do propugnado para outro tipo de paciente, exceto o de não se recomendar a administração de composto de ferro parenteral no primeiro trimestre da gestação. Sugere-se iniciar a suplementação de sal de ferro (ex. sulfato ferroso) por via oral (mais barato e mais seguro), 50-200 mg/dia de ferro elementar, mesmo com a concentração de Hb dentro da faixa de normalidade, quando a ferritina estiver em níveis inferiores a 30 ng/mL, ou quando seu nível estiver entre 30-100 ng/mL na vigência de anemia, especialmente se microcítica (é improvável a anemia ferropriva com ferritina ≥ 100 ng/mL). A ingestão do sal de ferro de estômago vazio ou associado a vitamina C aumenta a sua absorção. No entanto, uma dificuldade que ocorre mais frequentemente na gestante é a maior intolerância ao sal de ferro oral (náusea, constipação, diarreia, dispepsia, gosto metálico). Nessa situação, pode ser útil sugerir a ingestão do sal de ferro em dias alternados, ou mesmo com maior intermitência, reduzir a dose diária ou prescrever apresentação líquida, até que se possa administrar o medicamento por via parenteral, a partir do segundo trimestre da gestação. Depois de iniciado o tratamento por via oral, é importante monitorar periodicamente a sua eficácia, por exemplo, 2 a 4 semanas depois do seu início, inclusive para mudar a via de administração de oral para parenteral caso não se tenha observado aumento da concentração de Hb.
Além da deficiência de ferro, também podem ocorrer durante a gestação outras deficiências de nutrientes, como a do ácido fólico e a da cobalamina (vitamina B12), entretanto, em menor frequência, especialmente a última. A anemia por deficiência de folato tem se tornado menos frequente que antes em razão da suplementação desse nutriente no início, ou mesmo antes, da gestação, para evitar má-formação em tubo neural do feto. Para esse fim, ou para tratar a anemia, basta administrar 1 mg/dia de folato, dose mais que suficiente para compensar as necessidades aumentadas da gestação. A deficiência de cobalamina pode ser tratada com a suplementação oral desse nutriente. Pacientes com problema que interfira com a absorção, no íleo terminal, de vitamina B12, por exemplo, aqueles submetidos a cirurgia bariátrica, devem receber a suplementação por via sublingual ou intramuscular (IM). A dose mais comumente recomendada é de 1.000 µg IM/ dia por 5-7 dias, depois, a mesma dose uma ou duas vezes por semana, e, por fim, uma vez ao mês, indefinidamente em caso de persistência da causa da deficiência.
Anemia da doença renal
A anemia é complicação que acomete a maioria dos indivíduos com insuficiência renal crônica (IRC) em estágio avançado e, nesses pacientes, estaria associada a piora da qualidade de vida e a risco aumentado de desenvolvimento de doença cardiovasculare de morte. Sua instalação é gradual e piora à medida que piora a função renal. Segundo estudo de McClellan et al., a percentagem de pacientes anêmicos aumentou de 26,7% para 75,5% quando a taxa de filtração glomerular diminuiu de ≥ 60 mL/min/1,73 m2 para < 15 mL/min/1,73 m2. A principal causa da anemia da IRC é a produção reduzida da eritropoetina-EPO (90% da EPO é sintetizada nos rins e 10%, no fígado), um hormônio (PM 30 kDa) que promove a sobrevida dos progenitores eritropoéticos, assim como a sua diferenciação. Outros fatores também contribuem para a anemia da IRC, como a inflamação, o sangramento, a deficiência de ferro e a redução da sobrevida média das hemácias.
Antes do advento dos agentes estimuladores da eritropoese (AEEs), a anemia da IRC era tratada com suplementação de ferro, com a administração de andrógenos e com a transfusão de hemácias. A partir dos anos 1990, o uso difundido da EPO e, posteriormente, de outros AEEs, como a darbepoetina alfa, revolucionou o tratamento da anemia da IRC, reduzindo muito a necessidade de transfundir hemácias. Sugere-se considerar o uso de AEE quando a Hb for inferior a 9,0-10,0 g/dL. Entretanto, o ímpeto de indicar um AEE arrefeceu um pouco quando se observaram alguns efeitos adversos associados ao seu uso, como hipertensão arterial, crise convulsiva e trombose no local de acesso vascular. Inicialmente, presumia-se que o ideal seria usar dose de AEE que normalizasse a concentração de Hb, entretanto, estudos clínicos subsequentes mostraram que a normalização da Hb, ou as doses mais altas do AEE necessárias para tal finalidade, poderia ser deletéria. A partir de então, estudos bem controlados tiveram por objetivo avaliar a adequação de visar a alvo terapêutico de Hb relativamente alto (± 13,0 g/dL) em contraposição a alvo subnormal (± 11,0 g/dL). Dois dos mais importantes estudos que mostraram os riscos do uso da EPO estão brevemente descritos abaixo. Besarab et al. incluíram 1.233 pacientes com cardiopatia (insuficiência cardíaca congestiva-ICC ou doença coronariana isquêmica) em hemodiálise, divididos em dois grupos, em que em um deles o objetivo era de atingir hematócrito (Ht) de 42% (n= 618), enquanto no outro, o objetivo era de atingir Ht de 30% (n= 615). Os desfechos primários eram o tempo para o óbito ou o primeiro episódio não-fatal de infarto agudo do miocárdio.
O grupo Ht 42% apresentou maior taxa de complicação, inclusive de trombose venosa que a observada no grupo Ht 30%, o que permitiu concluir que não se deve buscar atingir valor normal de Ht em pacientes cardiopatas com anemia da IRC. Outro estudo importante mostrou resultados semelhantes. Foram incluídos 1.432 pacientes com IRC que receberam dose de EPO para atingir Hb de 13,5 g/dL em um grupo (n= 715) e Hb de 11,3 g/dL no outro (n= 717). O grupo Hb 13,5 g/dL apresentou maior risco de complicação (infarto do miocárdio, hospitalização por ICC e acidente vascular encefálico por isquemia-AVEi) (RR: 1,34, 1,03-1,74; IC de 95%; P= 0,03) que o observado no grupo com Hb de 11,3 g/dL. Em razão desses achados, recomenda-se atualmente usar uma dose de EPO, ou de outro AEE, suficiente para atingir concentração de Hb de 10,0 a 12,0 g/dL, uma faixa que proporciona bom controle dos sinais e sintomas da anemia, e com menor risco de complicações cardiovasculares que aquele associado a valores mais elevados de Hb.
Por fim, a darbepoetina alfa também foi testada para avaliar seus benefícios e seus riscos, nesse caso, em pacientes com IRC associada ao diabetes mellitus tipo II, sem a necessidade de diálise e com anemia moderada. Foram incluídos 4.038 pacientes no estudo, 2.012 para receber a darbepoetina alfa e 2.026 para receber placebo. As conclusões foram que o uso da darbepoetina alfa não reduziu o risco de morte, de eventos cardiovasculares ou de piora da função renal, e foi associado a maior risco de AVEi. Seu único benefício foi o de reduzir o número de pacientes que requereram transfusão de hemácias (297 vs 496; P < 0,001). Além dos AEEs, há outra classe de agentes biológicos, cuja ação não é dirigida ao receptor da EPO, que poderá talvez trazer maiores benefícios que os AEEs, que são os estabilizadores do fator induzível pela hipóxia (HIF, do inglês hypoxia-inducible fator). No entanto, seu uso ainda não é difundido e seus efeitos adversos não são plenamente conhecidos.
Uma parcela dos pacientes não apresenta aumento da Hb com o uso de AEE, o que é denominado de resistência ao AEE. Há mais de uma maneira de definir a resistência ao uso de AEE; uma delas, do European Best Practice Guidelines, considera resistência quando há falha em atingir Hb de 11,0-12,0 g/dL a despeito da dose de 300 U/kg/semana de EPO ou de 1,5 µg/kg/semana de darbepoetina alfa. São várias as causas de resistência ao uso de AEE, entre as quais encontram- -se deficiências de ferro, de vitamina B12 ou de folato, sangramento, infecção e doença inflamatória concomitante. Pacientes com resposta inadequada ao AEE apresentam pior prognóstico.
Além do uso dos AEEs, é importante manter em níveis adequados as reservas de ferro, que, no caso, significa manter concentração de ferritina acima de 200 ng/mL em pacientes em hemodiálise, ou acima de 100 ng/mL em pacientes em tratamento conservador, além de saturação da transferrina ≥ 20%. Recomenda-se suspender a administração de ferro quando ferritina ≥ 500 ng/mL. A via preferida de administração de ferro é a parenteral, uma vez que sal de ferro por via oral é pouco ou nada absorvido em razão dos elevados níveis de hepcidina encontrados em pacientes com IRC.
Anemia no idoso
O indivíduo idoso (≥ 65 anos) apresenta maior prevalência das anemias carenciais (ferro, vitamina B12 e folato), da anemia da doença inflamatória e das anemias clonais (síndrome mielodisplásica). Mas, comumente sofre de anemia de causa mal definida, em geral, uma associação de dois ou mais fatores. Gaskell et al., numa revisão sistemática, observaram que um total de 17% (3-50%) dos idosos apresentavam anemia, sendo 12% (3-25%) em estudos na comunidade, 47% (31-50%) em lar de idosos e 40% (40-72%) em pacientes hospitalizados. No Brasil, um estudo mostrou anemia em 18,6% (20,8% em homens e 17,6% em mulheres) dos idosos e aumento da prevalência com o aumento da idade.
Em língua inglesa, é comum o uso do termo “inflammaging” para definir a anemia da inflamação crônica do idoso, associada à diminuição da eritropoese observada nessa idade, decorrente da queda da produção de andrógeno e da senescência do compartimento celular dos precursores da eritropoese. As citocinas inflamatórias IL-6, IL-1 e o fator de necrose tumoral α (TNF-α) estão em níveis comumente aumentados no idoso, mesmo sem uma doença inflamatória evidente33. Além disso, o idoso tem menor reserva funcional de órgãos e, portanto, menor capacidade de mobilizar os mecanismos compensatórios à anemia, o que o torna particularmente vulnerável aos seus efeitos. Então, é comum o paciente se apresentar em estado de fragilidade física, deprimido e com declínio cognitivo.
Uma das explicações para a anemia do idoso é um maior número de eritrócitos em processo de morte celular (eriptose). Ela se caracteriza por maior expressão na face exterior da membrana citoplasmática da fosfatidilserina.
O tratamento da anemia do idoso requer investigação da causa da anemia, por exemplo, a deficiência de ferro. A reposição de ferro é recomendada quando se acredita que possa haver uma deficiência desse metal, mesmo que parcialmente camuflada pelo substrato inflamatório. Nesses casos, a reposição oral de ferro deve ser pouco ou nada eficaz, em razão dos níveis elevados da hepcidina, que impedem a sua absorção. Então, preconiza-se a administração de ferro por via parenteral. A transfusão de hemácias não costuma ser necessária, entretanto, em razão da menor reserva funcional de órgãos, pode ser necessário indicar a transfusão com níveis mais elevados de Hb, se o paciente apresentar sintomas ou sinais atribuíveis à anemia. Gregersen et al. mostraram os benefícios associados a estratégia de transfusão mais liberal (Hb ≤ 11,3 g/dL vs Hb ≤ 9,7 g/dL) em pacientes idosos e frágeis submetidos a cirurgia para fratura de quadril.
Tratamento Transfusional:
Há, basicamente, duas indicações de transfundir hemácias: diminuir a hipóxia causada pela anemia e suprimir a eritropoese anormal, como na anemia falciforme com complicação, por exemplo, acidente vascular encefálico isquêmico, em que se preconiza a redução da HbS para níveis inferiores a 30-40%.
A indicação de transfundir hemácias para reduzir ou prevenir a hipóxia depende de vários fatores, como: o grau da anemia (dado pela concentração da Hb); a sua gravidade (repercussão da anemia em paciente específico); o diagnóstico, por exemplo, pacientes com talassemia maior requerem transfusões periódicas de hemácias por toda a vida, mesmo quando assintomáticos e com níveis de Hb relativamente altos (9,0-10,0 g/dL); a presença de comorbidades que podem favorecer ou desfavorecer a indicação de transfusão, assim como influir na dose transfusional (pacientes idosos podem não tolerar doses mais altas de transfusão), entre outros. Portanto, não há um valor de concentração de Hb abaixo do qual a transfusão de hemácias esteja automaticamente indicada. Cada paciente apresenta necessidades específicas. No entanto, a adoção de gatilhos transfusionais é justificável para pacientes com quadro clínico relativamente homogêneo, como, por exemplo, o observado em cirurgia de revascularização miocárdica ou em unidades de tratamento de onco-hematologia.
A dose transfusional depende de tudo o que foi exposto acima, mas também dos objetivos da transfusão. Por exemplo, a transfusão na talassemia maior, ou na anemia falciforme, visa a atingir um objetivo numérico de concentração de Hb, o que requer um cálculo preciso da dose de hemácias a transfundir. No entanto, o objetivo mais frequente é de melhorar clinicamente um paciente com descompensação cardiovascular decorrente da anemia, ou por ela agravada. Nesse caso, a dose não visa a atingir um objetivo numérico de Hb, mas sim, a melhora clínica que pode se dar eventualmente com a transfusão de um único concentrado de hemácias (200-250 mL de hemácias). Em regra, a transfusão de uma unidade de concentrado de hemácias eleva a concentração de Hb de 1,0-1,5 g/dL num paciente com 70 kg (volemia de 5.000 mL).
7 Benefícios da Anemia:
A anemia é uma óbvia condição patológica, entretanto, em algumas situações específicas, é possível presumir que anemia leve ou moderada possa trazer benefícios. Por exemplo, a inflamação crônica cursa com aumento do risco de complicações trombóticas, por várias razões, entre elas o aumento da viscosidade sanguínea. A redução da massa eritrocitária (anemia) comumente observada na doença inflamatória contrapor- -se-ia então a esse fenômeno. De fato, aumento forçado da concentração de Hb com o uso de AEEs leva ao risco aumentado de trombose, possivelmente não apenas pelo aumento da concentração da Hb, mas também por ações não eritropoéticas dos AEEs. Essa constatação foi determinante para a adoção atual de alvo mais baixo de Hb (~11,0 g/dL), tanto para a anemia da IRC quanto para a decorrente de doença inflamatória que nos anos iniciais do uso de AEE.
Outra vantagem observada é a menor mortalidade por malária por Plasmodium falciparum em pacientes com anemia ferropriva, o que talvez também seja verdade para outros tipos de infecção.
Por fim, não um benefício propriamente dito, a detecção de anemia indica a necessidade de investigar a sua causa, o que pode favorecer o diagnóstico mais precoce, por exemplo, de doenças neoplásicas, ou seja, a anemia pode ser o primeiro, e por tempo variável o único sinal de doença grave ainda oculta; por exemplo, a detecção de queda da concentração de Hb precedeu em três anos o diagnóstico de câncer de estômago ou de mieloma múltiplo, em dois anos o de câncer de cólon, de intestino delgado ou o de linfoma de Hodgkin e precedeu em um ano o diagnóstico de linfoma não Hodgkin. Além disso, a concentração de Hb é poderoso indicador de risco de morte para o idoso e de prognóstico para várias doenças, de modo que valor reduzido desse parâmetro pode sugerir condutas terapêuticas (e diagnósticas) mais vigorosas, pois faz pressupor doença de base mais avançada.