Diagnóstico da Leucemia
Noções Básicas em Auxiliar de Laboratório de Hematologia Clínica
1 Introdução do Diagnóstico de Leucemia:
A leucemia é uma proliferação neoplásica generalizada ou acúmulo de células hematopoéticas, com ou sem envolvimento do sangue periférico(22). Na maioria dos casos, as células leucêmicas extravasam para o sangue, onde podem ser vistas em grande número. Essas células também podem infiltrar o fígado, baço, linfonodos e outros tecidos.
As leucemias são classificadas de acordo com o tipo celular envolvido e o grau de maturação das células. As leucemias agudas (LA) caracterizam-se pela proliferação clonal acompanhada de bloqueio maturativo (anaplasia) variável, o que possibilita a existência de diferentes subtipos de leucemias.
Nas leucemias agudas enquadram-se as leucemias mielóides agudas (LMA). A LMA é um grupo heterogêneo de doenças clonais do tecido hematopoético, que se caracteriza pela proliferação anormal de células progenitoras da linhagem mielóide (mieloblastos), ocasionando produção insuficiente de células sangüíneas maduras normais, com consequente substituição do tecido normal.
Desse modo, a infiltração da medula é freqüentemente acompanhada de neutropenia, anemia e plaquetopenia. O processo neoplásico que dá origem ao clone leucêmico pode surgir em qualquer estágio do desenvolvimento celular, ou seja, em qualquer fase da hematopoese.
Os eventos moleculares precisos e responsáveis pela transformação leucêmica ainda não são conhecidos, entretanto o resultado final consiste na proliferação inexorável das células hematopoéticas imaturas que perderam a sua capacidade de diferenciação normal(17). No entanto, a ativação de protoncogenes e as mutações (alterações genéticas), em genes supressores que regulam o ciclo celular, parecem estar envolvidas na patogênese das leucemias, pois levam à perda dos mecanismos normais controladores da proliferação (divisão celular), diferenciação-maturação e/ou da morte celular programada (apoptose).
Na maioria dos casos, a LA surge sem motivo aparente, embora algumas vezes possam se identificar possíveis causas, como:
• radiação ionizante;
• vírus oncogênicos (human T-lymphotropic virus type I [HTLV-I] causando leucemia das células T do adulto);
• fatores genéticos e congênitos;
• algumas substâncias químicas e fármacos (como benzeno e agentes alquilantes);
• predisposição a doenças hematológicas.
A LMA é uma doença predominante em adultos mais velhos (acima de 60 anos de idade), com mais de 50% dos casos. É mais comum no sexo masculino do que no feminino, representa cerca de 15%-20% das LA da infância e 80% das dos adultos(20, 39) e apresenta um prognóstico pobre, especialmente em pacientes idosos.
Segundo o Instituto Nacional do Câncer (INCA), os índices de leucemias no Brasil mostram-se altos e estimam-se, para o ano de 2006, aproximadamente 9.500 novos casos. Muitas introspecções novas para o diagnóstico, patogênese, manifestação clínica, tratamento e prognóstico dos pacientes com LMA refletem a heterogeneidade da doença, uma vez que o prognóstico entre subgrupos de pacientes com LMA pode variar consideravelmente. Com base nesses dados, tornam-se de grande importância clínica os avanços laboratoriais ocorridos no diagnóstico das leucemias nos últimos anos.
2 Classificação da Leucemia:
As leucemias são classificadas com base no tipo celular envolvido e no estado de maturidade das células leucêmicas. Assim, as LA caracterizam-se pela presença de células muito imaturas (denominadas blastos) e por evolução rapidamente fatal em pacientes não-tratados.
Os primeiros sistemas de classificação das LA eram baseados somente em investigações citomorfológicas e citoquímicas. A morfologia ainda representa um modelo central, mas foi incorporada em sistemas de classificações atuais, como imunofenotipagem para um delineamento mais preciso da linhagem hematopoética, e estágio de diferenciação de leucemias em particular. Na Tabela 1 são abordadas as principais classificações das leucemias agudas.
De acordo com o sistema de classificação French-American-British (FAB), as LMA são ainda morfologicamente subclassificadas em oito tipos:
• M0: LMA sem diferenciação morfológica;
• M1: LMA com mínima diferenciação morfológica;
• M2: LMA com diferenciação (componente monocítico < 20%);
• M3: LMA promielocítica hipergranular M3 variante hipogranular;
• M4: LMA mielomonocítica (células monocíticas ≥ 20%) M4 variante;
• M5: LMA monocítica (com células monocíticas ≥ 20% das células leucêmicas) M5a – LMA monoblástica (sem diferenciação, blastos ≥ 80%) M5b – LMA monocítica (com diferenciação, blastos < 80%);
• M6: eritroleucemia e variante;
• M7: LMA megacarioblástica.
Contudo, a classificação FAB está em desuso e está sendo substituída pela classificação da Organização Mundial da Saúde (OMS). A classificação da OMS apresenta recomendações atualizadas e modificadas dos critérios diagnósticos utilizados pela FAB, valorizando critérios citogenéticos.
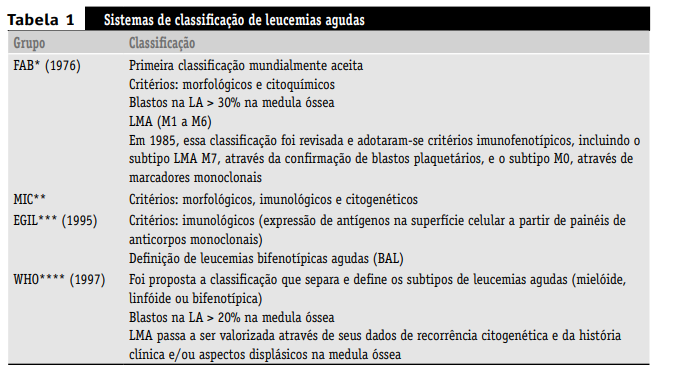
Existe também uma minoria de LA que apresenta características de ambas as linhagens (mielóide e linfóide) e, por essa razão, são designadas leucemias de linhagem mista, híbrida ou leucemia bifenotípica aguda (BAL)(10, 40). As BAL são doenças raras, responsáveis por mais de 5% das LA.
Diagnóstico Laboratorial:
Geralmente, o diagnóstico de LMA inicia-se a partir de uma suspeita clínica (Tabela 2) e se baseia na avaliação do sangue periférico e da medula óssea(4, 23, 35). Embora a morfologia continue sendo o fundamento para o diagnóstico, técnicas adicionais, incluindo imunofenotipagem, avaliação citogenética e estudos de genética molecular, tornaram-se essenciais e, em alguns casos específicos, são ferramentas complementares obrigatórias(49, 51). O uso de procedimentos diagnósticos permite a identificação do tipo celular envolvido na leucemogênese, o que é fundamental para orientar a terapêutica e determinar, até certo ponto, o prognóstico das leucemia.
As colorações citoquímicas (Tabela 3) usadas no diagnóstico e na classificação das leucemias podem ser aplicadas tanto à medula óssea quanto ao sangue periférico, auxiliando na confirmação da origem mielóide e/ou monocítica. Apesar dos progressos da imunofenotipagem, as reações citoquímicas ainda são úteis no diagnóstico das LMA.
As principais colorações em uso são fosfatase alcalina; mieloperoxidase (MPO); sudão negro B (sudan black B [SBB]); naftol AS-D; cloroacetato esterase (CAE); esterases inespecíficas, como alfa-naftil acetato esterase (ANAE); reação do ácido para-aminossalicílico (ácido periódico de Schiff [PAS]) e fosfatase ácida.
A mieloperoxidase ou SBB positiva confirma a natureza mielóide dos blastos e revela os bastonetes de Auer em aproximadamente 65% dos casos. Ela é específica para as linhagens de granulócitos, eosinófilos e monócito.
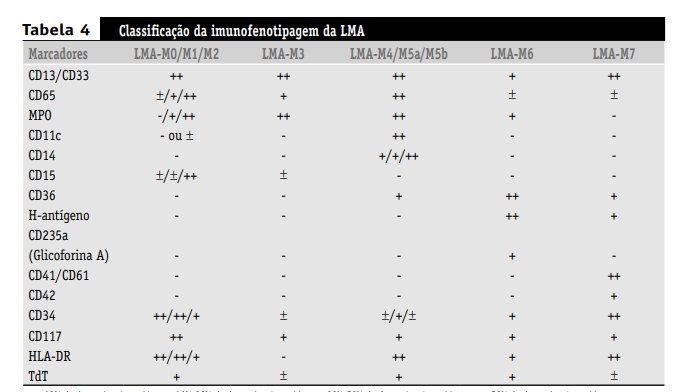
A imunofenotipagem é realizada por meio de anticorpos monoclonais marcados, que reconhecem epítopos específicos de antígenos celulares. As técnicas empregadas na imunofenotipagem podem ser a citometria de fluxo ou a imunocitoquímica. A importância da imunofenotipagem reside, principalmente, no diagnóstico das LMA M0 e M7, mas também em alguns casos de M5a, além de auxiliar no diagnóstico das LMA M3, LMA M2 e LMA M1/M2, bem como ser essencial para a identificação da BAL.


A citometria de fluxo é realizada com maior freqüência para distinção entre as leucemias mielóide e linfóide, o que é de crucial importância, e na monitorização pós-tratamento da LMA para detecção de doença residual mínima(45, 49, 54, 57). Também é útil na correta identificação dos subtipos de LMA, como a LMA M0, e na diferenciação da leucemia promielocítica aguda (M3) da LMA M1/M2(8, 27).Geralmente, a imunofenotipagem é realizada em suspensões de células do sangue periférico e da medula óssea, mas, quando necessário, pode ser feita em cortes histológicos. A Tabela 4 resume os principais marcadores imunofenotípicos relacionados aos subtipos de LMA.
A citogenética e os estudos moleculares frequentemente detectam anormalidades dentro do clone leucêmico, podendo sugerir o diagnóstico e/ou o prognóstico. As aberrações citogenéticas adquiridas são detectadas em 55%-75% de pacientes recentemente diagnosticados com LMA. A análise citogenética é convencionalmente feita pela análise microscópica dos cromossomos das células da medula óssea durante a metáfase. Pode ser complementada por técnicas de hibridização in situ, particularmente a hibridização fluorescente in situ (FISH), sendo importante para confirmar a presença de rearranjos recorrentes. Atualmente, a análise citogenética tem sido considerada um instrumento diagnóstico de grande importância para determinação do fator prognóstico da LMA.
A análise de genética molecular pode se fundamentar na análise do ácido desoxirribonucléico (DNA) por meio de técnicas, como análise de Southern blot ou reação em cadeia da polimerase (PCR), ou na análise do ácido ribonucléico (RNA) por PCR da transcriptase reversa (RT-PCR) e também por PCR em tempo real (RQ-PCR). A finalidade da análise de genética molecular pode ser tanto o estabelecimento da clonalidade, pela detecção da recombinação de genes que expressam imunoglobulinas, quanto pela identificação de uma recombinação molecular característica de um determinado tipo de LMA. Além de auxiliar na classificação das LA, é útil no monitoramento da doença residual mínima após a remissão induzida pela terapia.
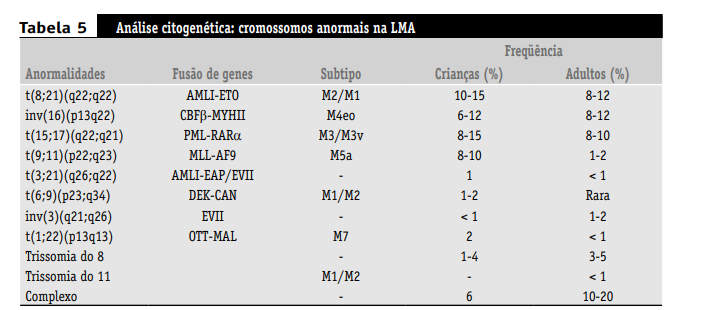
A importância da citogenética e da genética molecular na LMA para classificação e para compreensão de mecanismos patogênicos é apreciada cada vez mais no contexto clínico. As aberrações citogenéticas mais comuns observadas na LMA, e suas frequências, estão listadas na Tabela 5.
3 Disposições Finais:
Até bem pouco tempo, o diagnóstico da LMA era baseado exclusivamente na morfologia e na citoquímica do sangue e da medula óssea. Atualmente, o desenvolvimento de anticorpos monoclonais e citometria de fluxo assumiram o papel principal para a definição precisa das células blásticas de linhagem mielóide e subtipos de LMA.
Até bem pouco tempo, o diagnóstico da LMA era baseado exclusivamente na morfologia e na citoquímica do sangue e da medula óssea. Atualmente, o desenvolvimento de anticorpos monoclonais e citometria de fluxo assumiram o papel principal para a definição precisa das células blásticas de linhagem mielóide e subtipos de LMA.
Até bem pouco tempo, o diagnóstico da LMA era baseado exclusivamente na morfologia e na citoquímica do sangue e da medula óssea. Atualmente, o desenvolvimento de anticorpos monoclonais e citometria de fluxo assumiram o papel principal para a definição precisa das células blásticas de linhagem mielóide e subtipos de LMA com estudos mais aprofundados das técnicas, baseados em uma ampla combinação dos mesmos. Porém, esses estudos são caros, consomem tempo e requerem habilidade de pessoas experientes em laboratórios referenciais centralizados.
Experiências clínicas têm demonstrado a importância vital de anormalidades citogenéticas na determinação da sobrevida em pacientes com LMA. Aprimoramentos em tecnologias moleculares também estão em foco na detecção de translocações clinicamente relevantes, bem como providências de métodos sensíveis para rastrear doença residual mínima, em muitos pacientes, e para descrever a caracterização da LMA no diagnóstico e/ou durante o tratamento.
Sabe-se que o grau de evolução da LMA está significativamente relacionado ao aumento da proliferação celular clonal. Assim, a partir da análise genética, a expressão dos genes identificados na doença fornece razões para estudos futuramente preditivos para diagnóstico e intervenção terapêutica.