Farmacocinética
NOÇÕES BÁSICAS EM FARMACOLOGIA
1 Farmacocinética:
Até mesmo a mais promissora das terapias farmacológicas fracassará em estudos clínicos se o fármaco for incapaz de alcançar seu órgão-alvo em concentração suficiente para exercer efeito terapêutico. Muitas características que tornam o corpo humano resistente a danos causados por invasores estranhos e substâncias tóxicas também limitam a capacidade de os fármacos modernos combaterem os processos patológicos no paciente. O reconhecimento dos numerosos fatores que afetam a capacidade de um fármaco atuar em determinado paciente, bem como da natureza dinâmica desses fatores com o transcorrer do tempo, é de suma importância para a prática clínica da medicina.
Todos os fármacos devem satisfazer exigências mínimas para ter efetividade clínica. Um fármaco, para ser bem-sucedido, precisa atravessar as barreiras fisiológicas no corpo a fim de limitar o acesso das substâncias estranhas. A absorção dos fármacos pode ocorrer por meio de vários mecanismos desenvolvidos para explorar ou romper essas barreiras. Uma vez absorvido, o fármaco utiliza sistemas de distribuição dentro do organismo, como os vasos sanguíneos e linfáticos, para alcançar seu órgão-alvo em concentração apropriada. A capacidade do fármaco de ter acesso a seu alvo também é limitada por diversos processos que ocorrem no paciente. Estes são amplamente divididos em duas categorias: o metabolismo, em que o organismo inativa o fármaco mediante degradação enzimática (primariamente no fígado), e a excreção, em que o fármaco é eliminado do corpo (principalmente pelos rins e pelo fígado, bem como pelas fezes). Este capítulo apresenta uma visão geral dos processos farmacocinéticos de absorção, distribuição, metabolismo e excreção, com ênfase conceitual em princípios básicos que, quando aplicados a uma situação incomum, devem possibilitar ao estudante ou ao médico entender a base farmacocinética da terapia farmacológica.
Barreiras fisiológicas:
Um fármaco precisa vencer certas barreiras físicas, químicas e biológicas para alcançar seus locais de ação moleculares e celulares. O revestimento epitelial do trato gastrintestinal e de outras membranas mucosas é um tipo de barreira; são também encontradas outras barreiras após a penetração do fármaco no sangue e nos vasos linfáticos. A maioria dos fármacos deve distribuir-se do sangue para tecidos locais, processo que pode ser impedido por determinadas estruturas, como a barreira hematencefálica. Tipicamente, os fármacos abandonam o compartimento intravascular pelas vênulas pós-capilares, onde existem lacunas entre as células endoteliais através das quais o fármaco pode passar. A distribuição de um fármaco ocorre principalmente por difusão passiva, cuja velocidade é afetada por condições iônicas e celulares locais. A presente seção descreve as principais barreiras físicas, químicas e biológicas para o transporte dos fármacos no corpo, bem como as propriedades destes que afetam sua capacidade de superar tais barreiras.
Membranas biológicas:
Todas as células humanas apresentam membrana lipídica com duas camadas, as quais consistem principalmente em fosfolipídios, esteróis (sobretudo colesterol) e glicolipídios. A natureza anfifílica dos lipídios da membrana e os ambientes aquosos intra e extracelular fazem com que a membrana adote uma estrutura com um centro hidrofóbico e duas superfícies hidrofílicas. Além dos componentes lipídicos, as membranas biológicas contêm proteínas transmembrana (que as atravessam) e proteínas que só estão expostas na superfície extra ou intracelular. A dupla camada lipídica da membrana semipermeável forma uma barreira ao transporte de moléculas e tem implicações significativas para a terapia medicamentosa.
Transporte através da membrana:
O centro hidrofóbico de uma membrana biológica representa importante barreira para o transporte dos fármacos. Pequenas moléculas não polares, como os hormônios esteroides, são capazes de difundir-se facilmente através das membranas. Entretanto, a difusão passiva é ineficaz para o transporte de muitos fármacos e moléculas grandes e polares. Algumas proteínas transmembrana pertencentes à superfamília do carreador humano ligado a solutos (SLC, solutelinked carrier) – a qual inclui 43 famílias de proteínas, como as do transportador de ânions orgânicos (OAT, organic anion transporter) e do transportador de cátions orgânicos (OCT, organic cation transporter) – possibilitam o transporte de fármacos e moléculas polares através da membrana. Determinadas proteínas carreadoras transmembrana podem ser específicas para um fármaco e moléculas endógenas relacionadas; após ligação do fármaco à superfície extracelular da proteína, esta sofre mudança em sua conformação, que pode não depender de energia (difusão facilitada) ou exigir a entrada desta (transporte ativo). Essa mudança de conformação torna possível ao fármaco ligado acessar o interior da célula, onde sua molécula é liberada da proteína. De modo alternativo, alguns fármacos ligam-se a receptores específicos da superfície celular e deflagram um processo denominado endocitose, em que a membrana celular envolve a molécula para formar uma vesícula, a partir da qual o fármaco é subsequentemente liberado no interior da célula.
Difusão através da membrana:
Na ausência de outros fatores, um fármaco penetrará em uma célula até que as concentrações intra e extracelular dele sejam iguais. A velocidade de difusão depende do gradiente de concentração do fármaco através da membrana e da espessura, área e permeabilidade desta. De acordo com a lei de difusão de Fick, o fluxo efetivo de um fármaco através da membrana é:

Em que C1 e C2 são as concentrações intra e extracelular do fármaco, respectivamente. Essa definição aplica-se a uma situação ideal, em que não há fatores complicadores, como gradientes iônicos, de pH e de cargas através da membrana. Todavia, in vivo, esses fatores adicionais afetam a habilidade de um fármaco para penetrar nas células. Por exemplo, a concentração maior do fármaco fora da célula normalmente tende a favorecer sua entrada efetiva nela; porém, se tanto o interior da célula quanto o fármaco tiverem cargas negativas, é possível que essa entrada seja impedida. Ao contrário, uma célula cujo interior tem carga negativa pode favorecer a entrada de um fármaco de carga positiva.
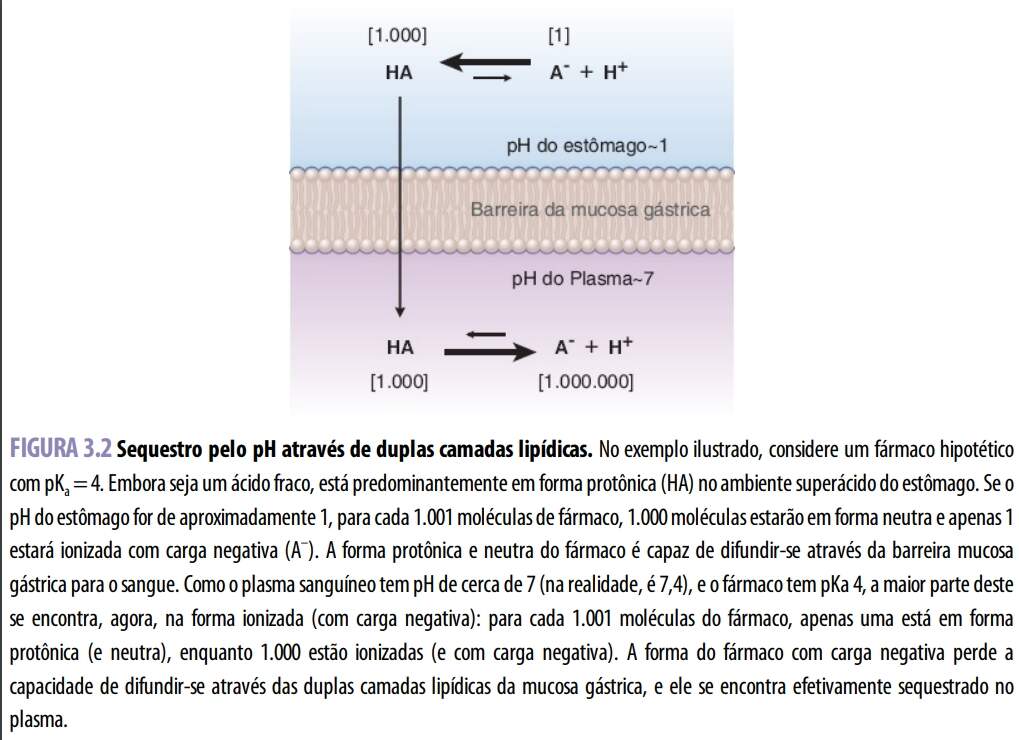
A difusão efetiva de fármacos ácidos e básicos através das membranas com dupla camada lipídica também pode ser afetada por um fenômeno associado à carga conhecido como sequestro pelo pH, que depende da constante dissociação ácida (pKa) do fármaco e do gradiente de pH através da membrana. Fármacos ácidos fracos, como fenobarbital e ácido acetilsalicílico, predominam em forma protônica, neutra, no ambiente altamente ácido do estômago. Essa forma não carregada pode atravessar as duplas camadas lipídicas da mucosa gástrica, acelerando a absorção do fármaco. A seguir, o fármaco ácido fraco adquire forma com carga elétrica negativa no ambiente mais básico do plasma, pois cede seu íon hidrogênio, e essa forma tem menor probabilidade de sofrer difusão retrógrada através da mucosa gástrica. Em seu conjunto, esses equilíbrios sequestram efetivamente o fármaco no interior do plasma.
Em termos quantitativos, a pKa de um fármaco representa o valor de pH em que metade do fármaco encontra-se em sua forma iônica. A equação de Henderson-Hasselbalch descreve a relação entre a pKa de um fármaco A ácido ou básico e o pH do meio biológico contendo esse fármaco:

Sistema nervoso central:
O sistema nervoso central (SNC) representa um desafio especial para a terapia farmacológica. Ao contrário da maioria das outras regiões anatômicas, está particularmente bem isolado de substâncias estranhas. A barreira hematencefálica utiliza junções estreitas, especializadas em impedir a difusão passiva da maioria dos fármacos da circulação sistêmica para a circulação cerebral. Por conseguinte, os fármacos destinados a atuar no SNC devem ser suficientemente pequenos e hidrofóbicos para atravessar com facilidade as membranas biológicas, ou devem utilizar as proteínas de transporte existentes na barreira hematencefálica para penetrar nas estruturas centrais. Os fármacos hidrofílicos que não conseguem ligar-se a proteínas de transporte facilitado ou ativo na barreira hematencefálica são incapazes de penetrar no SNC. É possível transpor a barreira hematencefálica utilizando infusão intratecal do fármaco, em que este é diretamente liberado no líquido cefalorraquidiano (LCR). Embora essa abordagem possa ser empregada no tratamento da meningite infecciosa ou carcinomatosa, a via intratecal não é prática para fármacos que precisam ser regularmente administrados ao paciente.
Absorção:
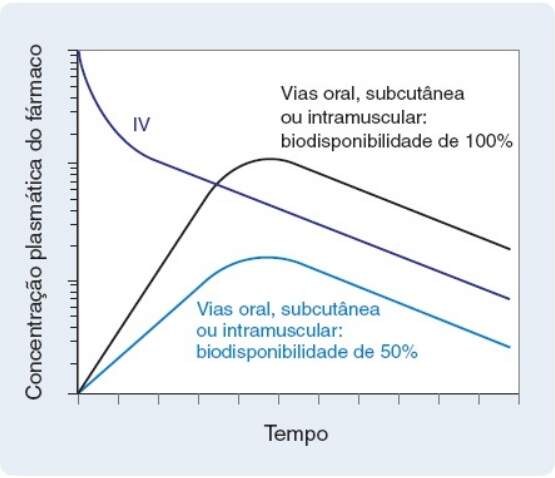
O corpo humano apresenta obstáculos excepcionais à invasão de microrganismos. O tegumento tem uma camada externa queratinizada e defensinas no epitélio. As membranas mucosas são protegidas por depuração mucociliar na traqueia, secreção de lisozima nos ductos lacrimais, secreção ácida no estômago e básica no duodeno. Esses mecanismos inespecíficos de defesa constituem barreiras para a absorção de fármacos e podem limitar sua chegada a certos órgãos-alvo. A biodisponibilidade, ou a fração do fármaco administrado que alcança a circulação sistêmica, dependerá da via de administração do fármaco, de sua forma química e de certos fatores específicos do paciente – como transportadores e enzimas gastrintestinais e hepáticos. Em termos quantitativos, a biodisponibilidade é definida da seguinte maneira:

Essa definição de biodisponibilidade baseia-se no fato importante de que a maioria dos fármacos alcança seus sítios de ação moleculares e celulares diretamente a partir da circulação sistêmica. Os fármacos de administração intravenosa são injetados diretamente na circulação sistêmica; para estes, a quantidade administrada equivale à quantidade que alcança a circulação, e sua biodisponibilidade é, por definição, igual a 1. Em contrapartida, a absorção gastrintestinal incompleta e o metabolismo hepático de “primeira passagem” (ver adiante) tipicamente fazem com que a biodisponibilidade de um fármaco de administração oral seja menor que 1.
Vias de administração e seus fundamentos:
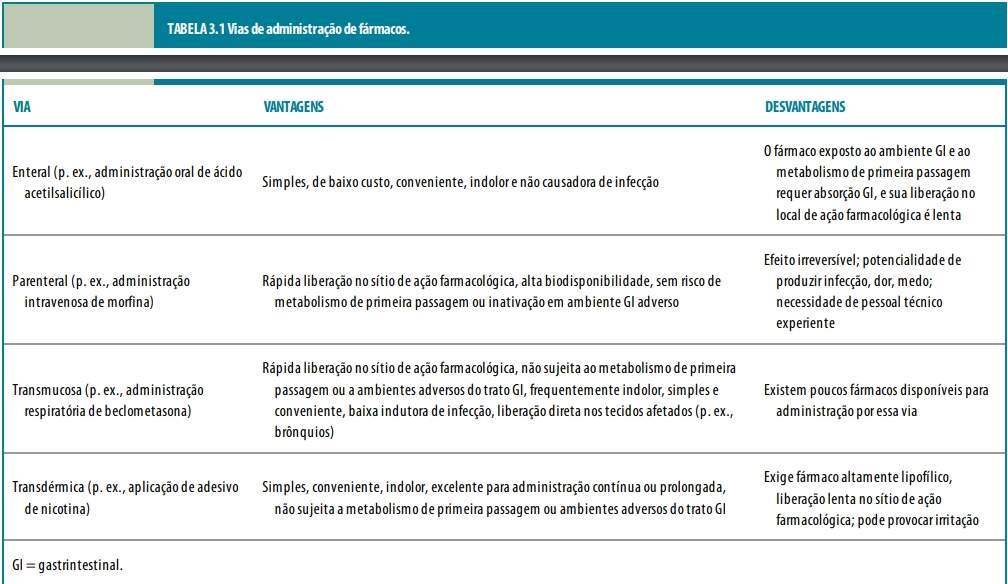
Novos fármacos são planejados e testados em forma posológica administrada por uma via específica. As vias de administração são escolhidas para tirar proveito das moléculas de transporte e de outros mecanismos que possibilitem a entrada do fármaco nos tecidos corporais. Esta seção discute as vantagens e desvantagens da administração de fármacos pelas vias enterais (oral e retal) e parenterais (todas que não são enterais), por exemplo, as que atravessam mucosas e a transdérmica.
Enteral:
A administração enteral por via oral constitui a mais simples das vias de administração de fármacos. Porém, expõe o fármaco a ambientes ácido (estômago) e básico (duodeno) rigorosos, passíveis de limitar sua absorção. Essa via oferece muitas vantagens ao paciente: possibilita fácil e conveniente autoadministração de fármacos orais, e a deglutição tem menos tendência do que outros métodos a causar infecções sistêmicas como complicação do tratamento. Um fármaco administrado por via oral deve permanecer estável durante sua absorção pelo epitélio do trato gastrintestinal. As junções das células epiteliais gastrintestinais dificultam o transporte através do epitélio intacto. Na verdade, as substâncias ingeridas (como os fármacos) devem, em geral, atravessar a membrana celular tanto na superfície apical quanto na basal, para alcançar o sangue circulante. A eficiência desse processo é determinada pelo tamanho e pelo caráter hidrofóbico do fármaco e, algumas vezes, pela presença de carreadores por intermédio dos quais o fármaco pode entrar e/ou sair da célula. Em geral, os fármacos hidrofóbicos e neutros atravessam as membranas celulares de modo mais eficiente do que os fármacos hidrofílicos ou com carga elétrica, a não ser que a membrana contenha uma molécula carreadora que facilite a passagem das substâncias hidrofílicas.
Após atravessar o epitélio gastrintestinal, os fármacos são transportados pelo sistema porta até o fígado antes de passar para a circulação sistêmica. Enquanto a circulação porta protege o corpo dos efeitos sistêmicos de toxinas ingeridas, entregando-as ao fígado para destoxificação, esse sistema pode complicar a liberação de fármacos. Todos os fármacos administrados por via oral estão sujeitos ao metabolismo de primeira passagem no fígado. Nesse processo, as enzimas hepáticas podem inativar uma fração do fármaco ingerido. Qualquer fármaco que sofra metabolismo de primeira passagem significativo precisa ser administrado em quantidade suficiente para assegurar a presença de uma concentração efetiva na circulação sistêmica, a partir da qual possa alcançar o órgão-alvo. Fármacos administrados por vias não enterais não estão sujeitos ao metabolismo hepático de primeira passagem.
Parenteral:
A administração parenteral, que consiste na introdução direta de um fármaco na circulação sistêmica, no líquido cefalorraquidiano, em tecido vascularizado ou em outro espaço tecidual, supera imediatamente as barreiras capazes de limitar a eficiência dos fármacos administrados por via oral. A administração tecidual resulta em uma velocidade de início de ação do fármaco que difere entre os vários tecidos do corpo, dependendo da velocidade de fluxo sanguíneo para o tecido. A administração subcutânea (SC) de um fármaco no tecido adiposo pouco vascularizado resulta em início de ação mais lento do que a injeção em espaços intramusculares (IM) bem vascularizados. Os fármacos apenas solúveis em soluções oleosas são frequentemente administrados por via intramuscular. Sua introdução direta na circulação venosa [por via intravenosa (IV)] ou arterial [intra-arterial (IA)] ou no líquido cefalorraquidiano [intratecal (IT)] faz com que o fármaco alcance mais rapidamente o órgão-alvo. Diferentemente das injeções subcutâneas e intramusculares, a injeção intravenosa não é limitada na quantidade de fármaco que pode ser liberada. As infusões contínuas desse tipo também têm a vantagem de uma liberação controlada do fármaco.
A administração parenteral pode envolver várias desvantagens potenciais, incluindo maior risco de infecção e necessidade de administração por um profissional de saúde. A velocidade de início de ação dos fármacos administrados por essa via é frequentemente rápida, resultando em aumento potencial da toxicidade quando esses fármacos são administrados com muita rapidez ou em doses incorretas. Tais desvantagens devem ser confrontadas com as vantagens da administração parenteral (como velocidade de início da ação e controle da dose liberada) e a urgência da indicação da terapia farmacológica.

Membrana mucosa:
A administração de fármacos através de membranas mucosas pode proporcionar potencialmente rápida absorção, baixa incidência de infecção e conveniência na autoadministração, além de evitar o ambiente gastrintestinal adverso e o metabolismo de primeira passagem. Os epitélios sublingual, ocular, pulmonar, nasal, retal, urinário e do trato reprodutor foram todos utilizados para administração de fármacos em gotas, comprimidos de rápida dissolução, aerossóis e supositórios (entre outras formas farmacêuticas). As mucosas são muito vascularizadas, possibilitando ao fármaco penetrar rapidamente na circulação sistêmica e alcançar seu órgão-alvo em tempo mínimo. Os fármacos também podem ser administrados diretamente no órgão-alvo, o que torna seu início de ação praticamente instantâneo. Esse aspecto constitui vantagem em situações críticas, como asma aguda, em que certos fármacos (p. ex., agonistas β-adrenérgicos) são administrados diretamente nas vias respiratórias por aerossóis.
Transdérmica:
Um número limitado de fármacos é tão lipofílico que atravessa a pele por difusão passiva, fazendo dela uma via de administração a ser considerada. Os fármacos administrados por via transcutânea são absorvidos a partir da pele e dos tecidos subcutâneos diretamente para o sangue. Essa via de administração é ideal para um fármaco que precisa ser administrado de modo lento e contínuo por longo período. Não oferece risco de infecção, e a administração é simples e conveniente. O sucesso dos adesivos transdérmicos de nicotina, estrógeno e escopolamina demonstra a utilidade potencial dessa via de administração.
Fatores locais, regionais e sistêmicos que afetam a absorção:
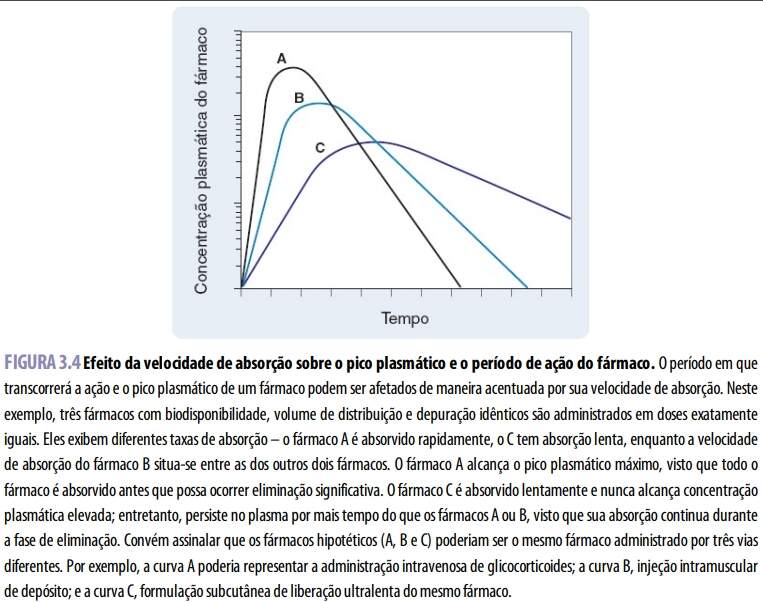
A velocidade e a magnitude de absorção de um fármaco são influenciadas por fatores locais, regionais e sistêmicos. De modo geral, uma dose alta e/ou administrada rapidamente resulta em concentração local elevada da substância. Um amplo gradiente de concentração entre o local da administração e o tecido circundante promove a distribuição do fármaco para o tecido próximo e/ou para a vasculatura. Qualquer fator que reduza o gradiente de concentração no local da administração diminui a força motriz do gradiente e pode reduzir a quantidade de fármaco a ser distribuída para os tecidos locais. O fluxo sanguíneo regional exerce o maior efeito nesse aspecto; em uma região com alta perfusão, as moléculas do fármaco que penetram nesse compartimento são rapidamente removidas. Esse efeito mantém a concentração do fármaco em baixos níveis no compartimento, possibilitando que a força propulsora para a entrada de novas moléculas do fármaco no compartimento permaneça alta. Por exemplo, os anestésicos gerais voláteis são administrados por inalação. Os pulmões são bem irrigados, e o anestésico é removido deles com rapidez para a circulação sistêmica. O fármaco não se acumula na circulação local, mantendo-se, assim, um gradiente de concentração que promove a difusão para o sangue. Nos indivíduos com elevada massa corporal, tanto a área de superfície absortiva como os volumes teciduais maiores disponíveis para distribuição tendem a remover a substância do local da administração e aumentar a velocidade e a magnitude da absorção do fármaco. A velocidade de absorção de um fármaco influencia a concentração local da substância (inclusive sua concentração plasmática) e o período de ação da mesma.
Distribuição:
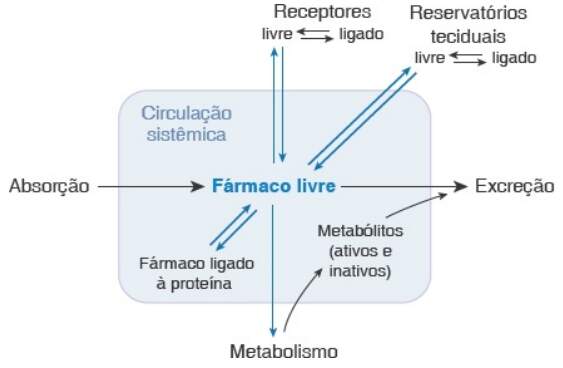
Embora a absorção do fármaco constitua pré-requisito para atingir níveis plasmáticos adequados desse fármaco, ele também precisa alcançar seu órgão ou órgãos-alvo em concentrações terapêuticas para exercer o efeito desejado sobre determinado processo fisiopatológico. A distribuição de um fármaco ocorre primariamente por meio do sistema circulatório, enquanto o sistema linfático contribui com um componente menor. Uma vez absorvido na circulação sistêmica, o fármaco é então capaz de alcançar qualquer órgão-alvo (com a possível exceção dos compartimentos santuários, como o cérebro e os testículos). A concentração do fármaco no plasma é tipicamente utilizada para definir e monitorar seus níveis terapêuticos, visto que é difícil medi-los no órgão-alvo. Mesmo em casos em que a concentração plasmática de um fármaco representa medida relativamente precária de sua concentração tecidual, seu efeito no tecido-alvo com frequência correlaciona-se bem com sua concentração plasmática.
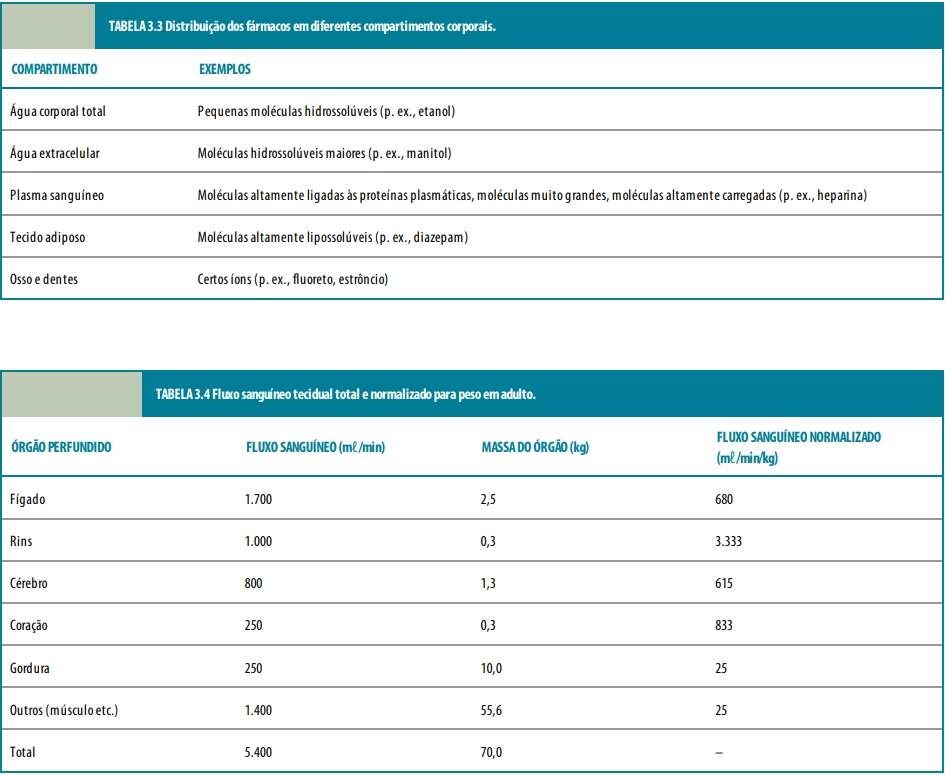
Órgãos e tecidos variam de modo acentuado em sua capacidade de captar diferentes tipos de fármacos, bem como na proporção de fluxo sanguíneo sistêmico que recebem. Por outro lado, esses fatores afetam a concentração do fármaco no plasma e determinam a quantidade que precisa ser administrada para atingir a concentração plasmática desejada. A capacidade de tecidos não vasculares e proteínas plasmáticas captarem o fármaco e/ou ligarem-se a ele deve ser considerada para configurar regimes de doses que alcancem níveis terapêuticos do fármaco.
Volume de distribuição
O volume de distribuição (Vd) descreve a proporção de fármaco que se divide entre o plasma e os compartimentos teciduais. Em termos quantitativos, Vd representa o volume de líquido necessário para conter a quantidade total do fármaco absorvido no corpo, em uma concentração equivalente à do plasma no estado de equilíbrio dinâmico.
O volume de distribuição é uma extrapolação do volume com base na concentração de fármaco no plasma, não se trata de volume físico. Desta maneira, Vd é baixo para fármacos principalmente retidos no compartimento vascular e alto para fármacos que sofrem ampla distribuição em músculo, tecido adiposo e outros compartimentos não vasculares. Para fármacos cuja distribuição é acentuadamente alta, o volume de distribuição é, com frequência, muito maior do que o volume de água corporal total, refletindo as baixas concentrações do fármaco no compartimento vascular, no estado de equilíbrio dinâmico. Numerosos fármacos apresentam volumes de distribuição muito grandes, como, por exemplo, a amiodarona (4.620 ℓ para uma pessoa de 70 kg), a azitromicina (2.170 ℓ), a cloroquina (9.240 ℓ) e a digoxina (645 ℓ), entre outros.
A capacidade do sangue e de vários órgãos e tecidos de captar e reter um fármaco depende tanto do volume (massa) do tecido quanto da densidade de sítios de ligação específicos e inespecíficos para o fármaco nesse tecido. Um fármaco captado em grandes quantidades por tecidos corporais como o adiposo e o músculo será amplamente removido da circulação no estado de equilíbrio dinâmico. Na maioria dos casos, esses tecidos precisam estar saturados para que os níveis plasmáticos dos fármacos possam aumentar o suficiente a ponto de afetar o órgão-alvo. Assim, considerando dois fármacos de potência igual, aquele que tiver distribuição mais alta entre os tecidos corporais, em geral, necessitará de dose inicial maior para estabelecer concentração plasmática terapêutica do que aquele que tiver distribuição mais baixa.
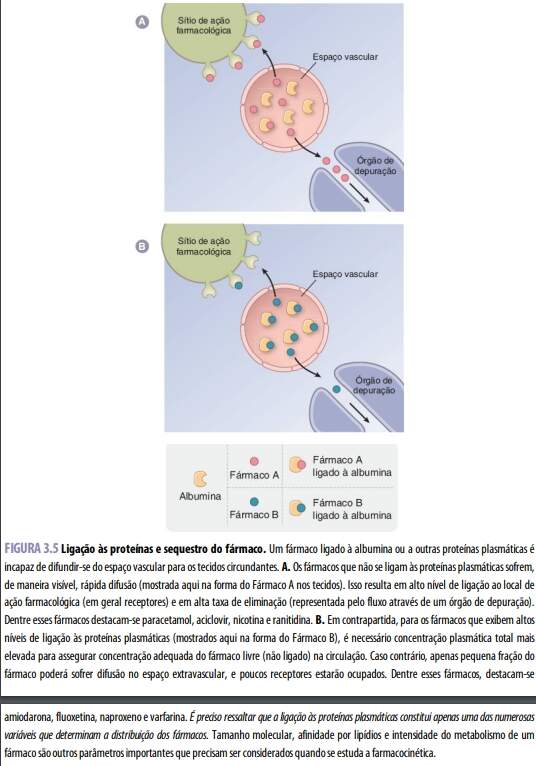
Ligação às proteínas plasmáticas:
A capacidade do músculo e do tecido adiposo de se ligarem a um fármaco aumenta a tendência desse fármaco de difundir-se do sangue para compartimentos não vasculares. Porém, essa tendência pode ser contrabalançada, em certo grau, pela ligação do fármaco às proteínas plasmáticas. A albumina, proteína plasmática mais abundante (com concentração de cerca de 4 g/dℓ), é responsável pela maioria das ligações dos fármacos. Muitos se ligam com baixa afinidade a ela por meio de forças hidrofóbicas e eletrostáticas. A ligação às proteínas plasmáticas tende a reduzir a disponibilidade de um fármaco para difusão ou transporte até seu órgão-alvo, visto que, em geral, apenas a forma livre ou não ligada do fármaco é capaz de propagar-se através das membranas. A ligação às proteínas plasmáticas também pode reduzir o transporte dos fármacos em compartimentos não vasculares (p. ex., o tecido adiposo e o músculo). Como um fármaco altamente ligado a elas tende a permanecer na vasculatura, frequentemente apresenta volume de distribuição relativamente baixo (em geral, 7 a 8 ℓ para um indivíduo de 70 kg).
Teoricamente, a ligação a tais proteínas poderia ser importante como mecanismo em algumas interações medicamentosas. A coadministração de dois ou mais fármacos que se ligam a elas pode resultar em uma concentração plasmática da forma livre acima do esperado de um ou de ambos os fármacos, quando competem entre si pelos mesmos sítios de ligação nessas proteínas. A concentração aumentada de fármaco livre é capaz de, eventualmente, causar efeitos terapêuticos e/ou tóxicos aumentados do fármaco. Nesses casos, é possível deduzir que será necessário ajustar o esquema de dosagem de uma ou de ambas as substâncias, de modo que a concentração de fármaco livre retorne à sua faixa terapêutica. Na prática, entretanto, tem sido difícil demonstrar interações medicamentosas clinicamente significativas ocasionadas por competição de dois fármacos por sua ligação às proteínas plasmáticas, talvez devido à depuração aumentada dos fármacos livres quando deslocados de seus sítios de ligação nessas proteínas (ver adiante).
Modelagem da cinética e da termodinâmica da distribuição dos fármacos:
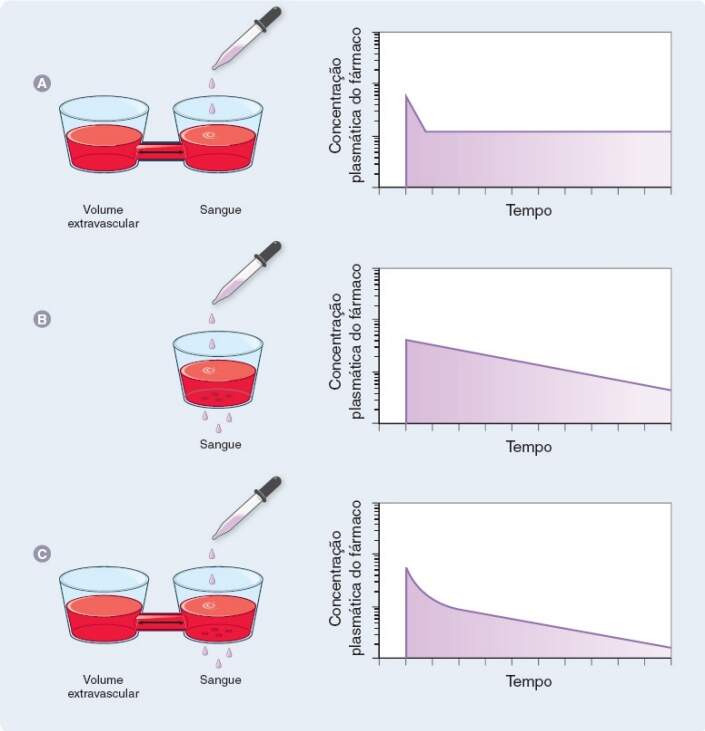
A maioria dos fármacos presentes na circulação sistêmica (compartimento intravascular) distribui-se rapidamente para outros compartimentos do corpo. Essa fase de distribuição acarreta acentuada diminuição da concentração plasmática do fármaco pouco depois de sua administração por injeção intravenosa única em bolo. Mesmo quando o fármaco já está equilibrado entre seus reservatórios teciduais, sua concentração plasmática continua declinando em virtude da eliminação do fármaco do corpo. Entretanto, tal concentração declina de modo mais lento durante a fase de eliminação, devido, em parte, a um “reservatório” de fármaco nos tecidos que pode difundir-se novamente para o sangue, a fim de substituir o que foi eliminado.
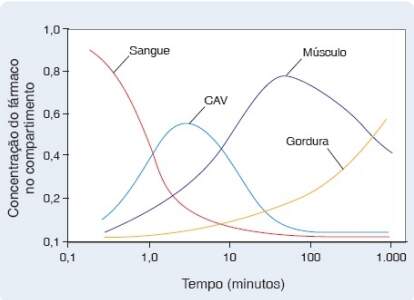
A tendência de um fármaco de ser captado pelos tecidos adiposo e muscular durante a fase de distribuição determina um conjunto de equilíbrios dinâmicos entre as concentrações nos vários compartimentos corporais. Conforme ilustrado na Figura 3.8, o rápido declínio da concentração plasmática de um fármaco, observado após a administração de injeção em bolo intravenosa, pode ser estimado com uso de um modelo de quatro compartimentos, constituídos por sangue, tecidos altamente vascularizados, tecido muscular e tecido adiposo. O compartimento altamente vascularizado é o primeiro compartimento extravascular no qual a concentração do fármaco aumenta, visto que o elevado fluxo sanguíneo recebido favorece cineticamente a entrada do fármaco nesse local. Entretanto, o tecido muscular e o adiposo frequentemente exibem maior capacidade de captar o fármaco do que o compartimento altamente vascularizado, visto que o tecido adiposo acumula maior quantidade de fármaco em velocidade mais lenta.
Metabolismo:
Diversos órgãos têm a capacidade de metabolizar em certo grau os fármacos, por meio de reações enzimáticas discutidas no Capítulo 4. Assim, rins, trato gastrintestinal, pulmões, pele e outros órgãos contribuem para o metabolismo de fármacos sistêmicos. Porém, o fígado contém diversidade e quantidade de enzimas metabólicas em larga escala, de modo que a maior parte do metabolismo dos fármacos ocorre nesse órgão. A capacidade do fígado de modificar os fármacos depende da quantidade de fármaco que penetra nos hepatócitos. Fármacos altamente hidrofóbicos podem penetrar de imediato nas células (inclusive nos hepatócitos), e o fígado metaboliza preferencialmente os hidrofóbicos. Entretanto, contém numerosos transportadores da superfamília de carreadores humanos ligados a solutos (CLS), que também possibilitam a entrada de alguns fármacos hidrofílicos nos hepatócitos. As enzimas hepáticas têm a propriedade de modificar quimicamente uma gama de substituintes nas moléculas dos fármacos, tornando-os inativos ou facilitando sua eliminação. Essas modificações são designadas, em seu conjunto, como biotransformação. As reações de biotransformação são classificadas em dois tipos: reações de oxidação/redução e reações de conjugação/hidrólise.

Reações de oxidação/redução:
As reações de oxidação/redução modificam a estrutura química de um fármaco; tipicamente, um grupo polarizado é adicionado ou encoberto. O fígado contém enzimas que facilitam cada uma dessas reações. O sistema enzimático do citocromo P450 microssomal, a via mais comum no fígado, medeia um grande número de reações oxidativas. Alguns fármacos podem ser administrados em forma inativa (profármacos) e alterados metabolicamente para a forma ativa mediante reações de oxidação/redução no fígado. Essa estratégia pode facilitar a biodisponibilidade oral, diminuir a toxicidade gastrintestinal e/ou prolongar a meia-vida de eliminação de um fármaco.
Modelo de distribuição dos fármacos em quatro compartimentos. Após administraçãode injeção intravenosa em bolo, ofármacoéliberadoem vários tecidosapartirdacirculaçãosistêmica. Noinício, suaconcentraçãoé maior nocompartimento vascular (sangue);entretanto, logoemseguida,aconcentraçãosanguíneacai rapidamenteàmedidaqueofármacodistribui-separaos diferentes compartimentos teciduais. Os tecidosaltamente vascularizados (i. e., supridospela maior fraçãododébitocardíaco) sãoem geral os primeiros a acumular o fármaco. Entretanto, os compartimentos teciduais também variam em sua capacidade de captação. Comoamassadocompartimentomuscularémaiorqueadocompartimentoaltamentevascularizado(CAV),ocompartimentomuscular tem maior capacidadedecaptação. Entretanto, comoosmúsculosrecebem menos sangue do que o compartimentovascular, tal efeito só se manifesta quando o fármaco começa a distribuir-se para o CAV. O compartimento mais precariamente vascularizado é o tecido adiposo; todavia, éoqueexibe maior capacidadedeacumular fármacos. O picodofármaco nessecompartimento nãoétãoaltoquanto aquele observado nocompartimento muscular, porquequantidade significativadofármacofoieliminadapor metabolismoe excreção antes de o compartimento adiposo começar a acumulá-lo. Uma vez concluída a administração de um fármaco, observa-se o padrão inverso – ele deixa em primeiro lugar o compartimento altamente vascularizado e, a seguir, os compartimentos muscular e adiposo, respectivamente. Ofármaco nesteexemploéotiopental,barbitúricousado nainduçãodaanestesiageral.
Reações de conjugação/hidrólise:
As reações de conjugação/hidrólise hidrolisam um fármaco ou conjugam-no com uma molécula grande e polar, a fim de inativá-lo ou, normalmente, aumentar sua solubilidade e excreção na urina ou na bile. Em certas ocasiões, a hidrólise ou a conjugação podem resultar em ativação metabólica de profármacos. Em geral, os grupos mais adicionados incluem glicuronato, sulfato, glutationa e acetato. Conforme descrito de maneira mais detalhada no próximo capítulo, os efeitos das reações de oxidação/redução e de conjugação/hidrólise sobre determinado fármaco também dependem da presença de outros fármacos tomados concomitantemente pelo paciente. Certas classes de fármacos, como os barbitúricos, são poderosos indutores de enzimas que medeiam reações de oxidação/redução; outros são capazes de inibir tais enzimas. A compreensão dessas interações medicamentosas constitui pré-requisito essencial para a dosagem apropriada de associações de fármacos. Médicos e pesquisadores começaram a elucidar o importante papel das diferenças genéticas entre indivíduos no que concerne aos vários transportadores e enzimas responsáveis pela absorção, distribuição, excreção e, particularmente, pelo metabolismo dos fármacos. Por exemplo, o complemento de enzimas do citocromo P450 no fígado de um indivíduo determina a taxa e a extensão com que esse indivíduo pode metabolizar numerosos agentes terapêuticos.
Excreção:
As reações de oxidação/redução e de conjugação/hidrólise aumentam a afinidade aquosa de um fármaco hidrofóbico e seus metabólitos, possibilitando-lhes serem excretados por uma via comum final com fármacos intrinsecamente hidrofílicos. Os fármacos e seus metabólitos são, em sua maioria, eliminados do corpo por excreção renal e biliar. A excreção renal é o mecanismo mais comum de eliminação de fármacos e baseia-se na natureza hidrofílica de um fármaco ou seu metabólito. Apenas um número relativamente pequeno de fármacos é excretado primariamente na bile ou pelas vias respiratórias ou dérmicas. Muitos fármacos administrados oralmente sofrem absorção incompleta pelo trato gastrintestinal superior, e o fármaco residual é então eliminado por excreção fecal.
Excreção renal:
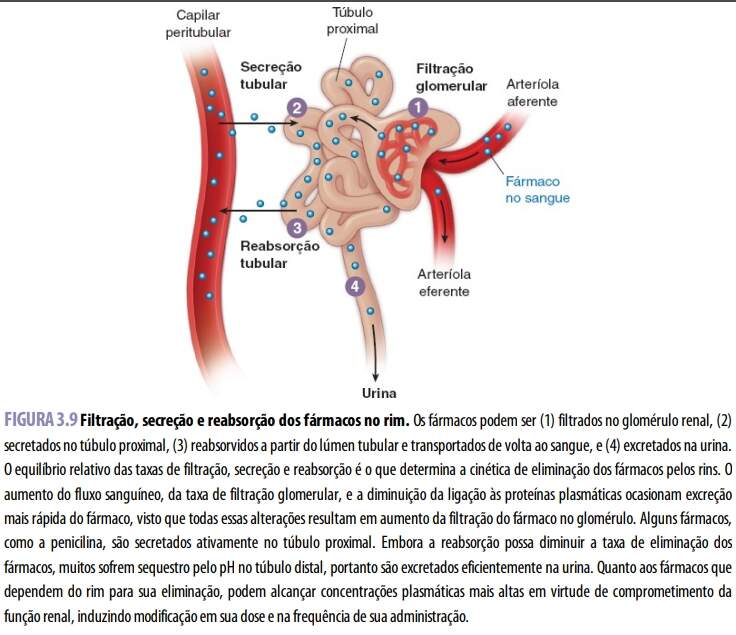
O fluxo sanguíneo renal representa cerca de 25% do fluxo sanguíneo sistêmico total, assegurando contínua exposição de qualquer fármaco presente no sangue aos rins. A taxa de eliminação dos fármacos pelos rins depende do equilíbrio das taxas de filtração, secreção e reabsorção. A arteríola aferente introduz no glomérulo tanto o fármaco livre (não ligado) quanto o ligado às proteínas plasmáticas. Entretanto, apenas a forma livre do fármaco é filtrada no túbulo renal. Logo, o fluxo sanguíneo renal, a taxa de filtração glomerular e a ligação do fármaco às proteínas plasmáticas afetam a quantidade de fármaco que penetra nos túbulos, no nível do glomérulo. O aumento do fluxo sanguíneo, da taxa de filtração glomerular, e a diminuição da ligação às proteínas plasmáticas causam excreção mais rápida dos fármacos. A excreção renal desempenha papel notável na depuração de numerosos fármacos, como, por exemplo, vancomicina, atenolol e ampicilina. Esses fármacos podem acumular-se até níveis tóxicos em pacientes com comprometimento da função renal e em idosos (que frequentemente manifestam algum grau de comprometimento renal).
A concentração urinária do fármaco aumenta no túbulo proximal devido à difusão passiva das moléculas de fármaco sem carga elétrica, à difusão facilitada de moléculas com carga ou sem carga e à secreção ativa de moléculas aniônicas e catiônicas do sangue para o espaço urinário. Em geral, os mecanismos secretórios não são específicos para fármacos; com efeito, a secreção tira proveito das semelhanças moleculares entre o fármaco e substâncias de ocorrência natural, como ânions orgânicos (transportados por proteínas da família dos OAT – organic anion transporter) e cátions orgânicos (transportados por proteínas da família dos OCT – organic cation transporter). A penicilina é um exemplo de fármaco eliminado, em grande parte, por transporte ativo no túbulo proximal. A extensão da ligação às proteínas plasmáticas parece exercer efeito relativamente pequeno sobre a secreção do fármaco no túbulo proximal, visto que os transportadores altamente eficientes que medeiam a secreção tubular ativa removem com rapidez o fármaco livre (não ligado) dos capilares peritubulares, alterando, portanto, o equilíbrio entre o fármaco livre e o fármaco ligado às proteínas nesses locais.
A concentração urinária de um fármaco pode declinar com sua reabsorção nos túbulos proximais e distais. Esta é limitada primariamente por sequestro pelo pH, conforme descrito anteriormente. O líquido tubular renal é ácido no túbulo proximal e além dele, o que tende a favorecer o sequestro da forma iônica das bases fracas. Como essa região do túbulo contém proteínas transportadoras que diferem daquelas encontradas nos segmentos anteriores do néfron, as formas iônicas de um fármaco resistem à reabsorção por difusão facilitada, com consequente aumento de sua excreção. A reabsorção de fármacos no túbulo pode ser intensificada ou inibida por um ajuste químico do pH urinário. A mudança na velocidade do fluxo urinário através dos túbulos também pode alterar a taxa de reabsorção de fármacos. Um aumento do débito urinário tende a diluir a concentração do fármaco no túbulo e o tempo durante o qual pode ocorrer difusão facilitada; ambos os efeitos podem diminuir a reabsorção de fármacos. Por exemplo, o ácido acetilsalicílico é um ácido fraco, excretado pelos rins. Sua superdosagem é tratada pela administração de bicarbonato de sódio para alcalinizar a urina (e, assim, sequestrar o ácido acetilsalicílico no túbulo) e pelo aumento do fluxo urinário (diluindo a concentração tubular do fármaco). Ambas as manobras clínicas resultam em eliminação mais rápida do fármaco.
Excreção biliar:
A reabsorção de fármacos também desempenha importante papel na excreção biliar. Alguns são secretados pelo fígado na bile por intermédio de membros da superfamília de transportadores do conjunto de ligação do ATP (ABC – ATP binding cassette), que inclui sete famílias de proteínas, como a de resistência a múltiplos fármacos (MDR, multidrug resistance). Como o ducto biliar desemboca no trato gastrintestinal no duodeno, esses fármacos devem passar por toda a extensão do intestino delgado e do intestino grosso antes de serem eliminados. Em muitos casos, sofrem circulação êntero-hepática, em que são reabsorvidos no intestino delgado, subsequentemente retidos na circulação porta e, a seguir, na circulação sistêmica. Certos fármacos, como hormônios esteroides, digoxina e alguns agentes quimioterápicos para o câncer, são excretados, em grande parte, na bile.
Aplicações clínicas da farmacocinética:
As interações dinâmicas entre absorção, distribuição, metabolismo e excreção de um fármaco determinam sua concentração plasmática e estabelecem sua capacidade de alcançar o órgão-alvo em concentração efetiva. Com frequência, a duração desejada da terapia farmacológica é maior do que a que pode ser obtida por dose única, tornando necessário o uso de múltiplas doses para proporcionar concentrações plasmáticas relativamente constantes do fármaco dentro dos limites de sua eficácia e toxicidade. Os resultados dos estudos clínicos de fármacos em fase de desenvolvimento, bem como a experiência clínica com fármacos aprovados pela Food and Drug Administration (FDA), sugerem que sejam alcançados níveis-alvo do medicamento no plasma de um paciente de constituição média. Entretanto, a farmacocinética e outras diferenças entre pacientes (como doença instaurada e perfil farmacogenético) também devem ser consideradas no planejamento do esquema posológico de um fármaco ou associação de fármacos para determinado paciente.
Depuração:
A depuração de um fármaco é o parâmetro farmacocinético que limita de modo mais significativo o tempo de ação do medicamento nos alvos moleculares, celulares e orgânicos. Pode ser conceituada de duas maneiras complementares: em primeiro lugar, como a taxa de eliminação de um fármaco do corpo em relação à concentração plasmática dele; alternativamente, como a taxa do fármaco da qual o plasma teria de ser depurado para justificar a cinética da mudança observada na quantidade total do fármaco no corpo, partindo do princípio de que todo o fármaco no corpo está presente na mesma concentração que a do plasma. Por conseguinte, a depuração é expressa em unidades de volume/tempo, como a seguir:



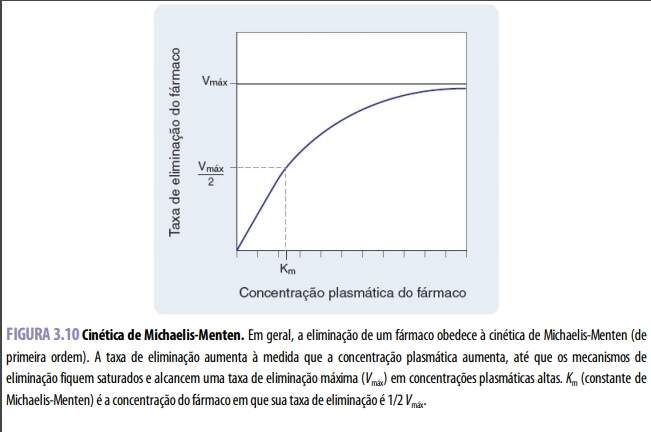
Fatores que alteram a meia-vida:
É preciso levar em conta as alterações fisiológicas e patológicas do volume de distribuição para determinar a dose apropriada de um fármaco, bem como o intervalo entre as doses. Com o processo de envelhecimento, a massa muscular esquelética diminui, o que pode reduzir o volume de distribuição. Em contrapartida, um indivíduo obeso apresenta aumento na capacidade de captação de um fármaco pelo tecido adiposo, e, para um fármaco que se distribui na gordura, pode ser necessário administrar uma dose mais alta a fim de alcançar níveis plasmáticos terapêuticos. Como terceiro exemplo, se a dose de um fármaco for baseada no peso corporal, porém o compartimento de tecido adiposo não captar esse fármaco, poderão ser alcançados níveis potencialmente tóxicos em uma pessoa obesa. Por fim, alguns fármacos podem distribuir-se de preferência em espaços líquidos patológicos, como ascite ou derrame pleural, causando toxicidade a longo prazo se a dose não for ajustada de acordo.
Os processos fisiológicos e patológicos também são capazes de afetar a depuração dos fármacos. Por exemplo, as enzimas do citocromo P450 responsáveis pelo metabolismo dos fármacos no fígado podem ser induzidas, aumentando a taxa de inativação dos fármacos, ou inibidas, diminuindo-a. As enzimas P450 específicas são induzidas por alguns fármacos (como carbamazepina, fenitoína, prednisona e rifampicina) e inibidas por outros (como cimetidina, ciprofloxacino, diltiazem e fluoxetina). Em que há extensa lista de indutores e inibidores de enzimas específicas. A falência de um órgão constitui outro fator crítico na determinação dos esquemas posológicos apropriados. Assim, a insuficiência hepática pode alterar a função das enzimas hepáticas e também diminuir a excreção biliar. A redução do débito cardíaco diminui a quantidade de sangue que alcança os órgãos de depuração. A insuficiência renal diminui a excreção dos fármacos, devido à redução da filtração e secreção deles nos túbulos renais. Em resumo, insuficiências hepática, cardíaca e renal podem, não necessariamente em conjunto, levar à redução da capacidade de inativação ou eliminação de um fármaco, aumentando, assim, sua meiavida de eliminação.

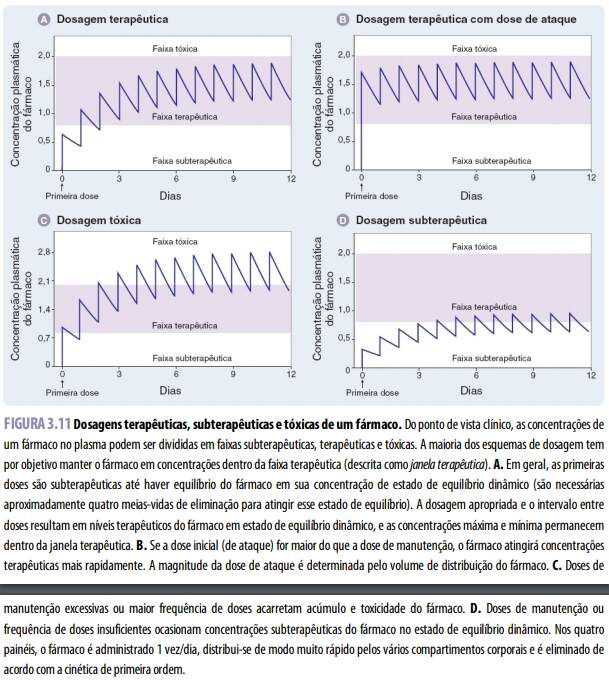
Dosagem terapêutica e intervalo entre doses:
Cada um dos princípios básicos de farmacocinética – absorção, distribuição, metabolismo e excreção – influencia o planejamento do esquema posológico eficaz de um fármaco. A absorção determina a via ou vias potenciais de administração e ajuda a definir a dose ideal do fármaco. Em geral, um fármaco que sofre acentuada absorção – evidenciada por sua alta biodisponibilidade – necessita de uma dose mais baixa do que a de um fármaco pouco absorvido. Em contrapartida, um fármaco de alta distribuição – evidenciada por grande volume de distribuição – necessita de uma dose maior. A taxa de eliminação influencia a meia-vida do medicamento, portanto determina a frequência de doses necessária para manter níveis plasmáticos terapêuticos do fármaco.
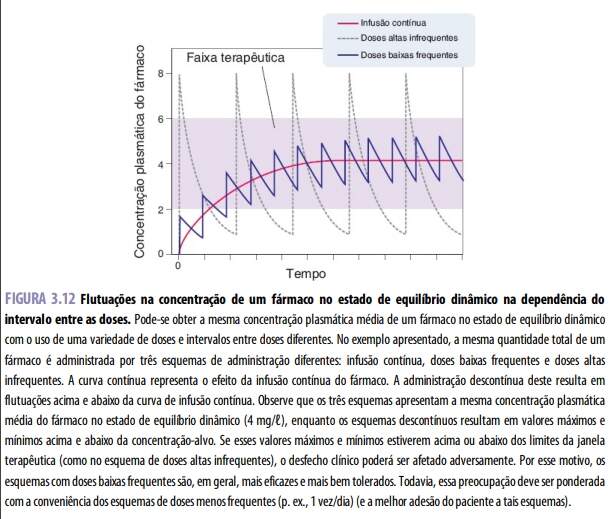
Em geral, a dosagem terapêutica de um fármaco procura manter seu pico plasmático abaixo da concentração tóxica, e a concentração mínima acima de seu nível minimamente efetivo. Isso pode ser obtido de modo mais eficiente mediante liberação contínua do fármaco IV (infusão contínua), SC (bomba de infusão contínua ou implante), VO (comprimidos de liberação prolongada) e outras vias de administração. Todavia, em muitos casos, o esquema posológico também deve levar em consideração a conveniência do paciente. Podem-se administrar doses pequenas e frequentes (habitualmente VO) para obter variação mínima na concentração plasmática do fármaco no estado de equilíbrio dinâmico, porém essa estratégia sujeita o paciente à inconveniência de uma administração frequente do medicamento. As doses administradas com menos frequência exigem quantidades mais elevadas e resultam em maiores flutuações nos níveis máximo e mínimo do fármaco; esse tipo de esquema é mais conveniente para o paciente, mas também tem mais tendência a causar problemas, devido a níveis excessivos (tóxicos) ou insuficientes (subterapêuticos) do fármaco. Os esquemas posológicos ótimos, em geral, mantêm a concentração plasmática do fármaco no estado de equilíbrio dinâmico dentro da janela terapêutica. Como esse estado de equilíbrio é alcançado quando a taxa de aporte do fármaco é igual à sua eliminação, a concentração do medicamento em tal estado é afetada por biodisponibilidade, depuração, dose e intervalo entre as doses (frequência de administração):
em que C é a concentração plasmática do fármaco. Imediatamente após iniciar terapia farmacológica, a taxa de entrada do fármaco no corpo (kinterna) é muito maior do que a taxa de eliminação (kexterna); como consequência, sua concentração no sangue aumenta. Supondo que a eliminação siga a cinética de primeira ordem, a taxa de eliminação também se eleva à medida que a concentração plasmática do fármaco aumenta, porque essa taxa é proporcional à concentração plasmática. O estado de equilíbrio dinâmico é alcançado quando as duas taxas (kinterna e kexterna) tornam-se iguais. Como kinterna é uma constante, a abordagem para o estado de equilíbrio dinâmico é governada pela kexterna , a taxa combinada de todos os mecanismos de depuração de fármacos. (kexterna também pode ser denominada ke , isto é, taxa combinada de eliminação de fármacos.) Na maioria dos esquemas posológicos, os níveis de fármacos acumulam-se depois de cada dose sucessiva, e o estado de equilíbrio dinâmico só é alcançado quando a quantidade de medicamento que entra no sistema é igual à que está sendo removida. Em nível clínico, é preciso lembrar-se desse princípio ao modificar o esquema posológico, visto que devem ocorrer pelo menos quatro a cinco meias-vidas de eliminação para que seja alcançado o novo estado de equilíbrio dinâmico.
A concentração plasmática no estado de equilíbrio dinâmico também pode ser alterada pela adição de outro fármaco ao esquema de tratamento de um paciente. No caso do Sr. W, a adição de sulfametoxazol-trimetoprima inibiu o metabolismo da varfarina, diminuindo a taxa de depuração desta e fazendo com que a concentração no estado de equilíbrio dinâmico atingisse níveis supraterapêuticos. Esse efeito foi exacerbado pela intoxicação aguda do Sr. W por etanol, que também inibe o metabolismo da varfarina. Pressupondo que o peso corporal do Sr. W seja aproximadamente 70 kg, que esteja tomando 5 mg de varfarina a cada 24 h e que a biodisponibilidade da varfarina seja 0,93, é possível calcular então a concentração plasmática inicial da substância no estado de equilíbrio dinâmico da seguinte maneira:
em que o valor de depuração de 0,192 ℓ/h é determinado a partir da meia-vida e do volume de distribuição do fármaco (ver Equações 3.9 e 3.10). Quando a depuração da varfarina foi reduzida pela adição de sulfametoxazol-trimetoprima e etanol, a concentração plasmática da substância no estado de equilíbrio dinâmico aumentou, atingindo níveis tóxicos. Essa situação poderia ter sido evitada pela determinação da INR do Sr. W alguns dias após o acréscimo do sulfametoxazoltrimetoprima (e, se necessário, ajuste da dose de varfarina) e pela recomendação de que o Sr. W evitasse o consumo de etanol enquanto tomasse a varfarina.