Manejo integrado de pragas II
Agroecologia e Manejo do Solo
1 Pragas das plantas ornamentais:
Manejo integrado das pragas da roseira:
- Diagnose:
a) Sugadores:
- ÁCARO RAJADO (Tetranychus urticae) Acari: Tetranychidae:
O ácaro rajado é a mais importante praga em rosas cultivadas sob casas de vegetação. Os ácaros são mais facilmente detectados nas casas de vegetação onde as temperatura são maiores. Eles podem se distribuir facilmente por toda a plantação de rosa durante uma colheita de flores. Alimentam-se principalmente na parte de baixo da folha, e os ovos são postos entre os fios de teia que o ácaro tece na página inferior das folhas; assim é imprescindível que o acaricida cubra adequadamente toda a planta. Atacam a face inferior das folhas de onde sugam o conteúdo citoplasmático, tornando as folhas cloróticas e acarretando um desfolhamento da planta e falta de florescimento. causam clorose e bronzeamento das folhas.
- PULGÕES: (Capitophorus rosarum, Macrosiphum rosae):
Se alimentam nos caules, folhas e flores. Pulgões são fáceis de serem identificados através da observação direta na camada externa da fuligem preta de fungos que crescem na substância doce secretada pela planta. Em casas de vegetação todos os pulgões são fêmeas. O ciclo de vida é curto, e podem se reproduzir de 7 a 8 dias. Atacam as roseiras, principalmente nos brotos novos e tenros, onde sugam a seiva para sua alimentação, causando o enrolamento das folhas e atrofiamento dos brotos, prejudicando sensivelmente a planta.
Quando a infestação é intensa, atacam, também, os botões florais novos, atraindo ainda, pelo líquido açucarado que expelem, as formigas, favorecendo o desenvolvimento da fumagina sugam seiva, causam amarelecimento e retorcimento de ramos e de folhas, transmitem vírus e possibilitam ainda o aparecimento da fumagina.
- TRIPES: Frankliniella spp.,(Thysanoptera: Thripidae):
São insetos pequenos de coloração variável, de 1 a 3 mm de comprimento no máximo. Vivem nas folhas, causando dobramento dos bordos para cima provocando estrias esbranquiçadas e prateadas nas mesmas. Durante o ciclo de vida, os ovos são colocados na flor e durante o desenvolvimento, as ninfas caem da planta para o solo duas vezes antes de amadurecerem. O controle é difícil por causa da proteção promovida pela flor e o fato de que as ninfas passam por dois períodos no solo.
Manejo integrado das pragas de ornamentais gerais:
a. SUGADORES;
- MOSCA BRANCA;
- MINADORES;
- Mosca minadora (Liriomyza spp.):
Vivem no interior das folhas formando minas serpentadas, provocando em consequência, seu secamento.
- DESFOLHEADORES:
Vaquinhas (Paraulaca dives e Diabrotica speciosa):
Alimentam de folhas fazendo furos no interior das mesmas, podem atacar também flores e os botões florais.
Lagartas (Brassolis spp., Agrotis ipisilon e Spodoptera spp.):
Também se alimentam de folhas e flores.
- BROQUEADORES:
Vespinha (Eurytoma orchidearum):
Broqueia rebentos e bulbos florais de orquídeas, podendo causar a seca desses orgãos. Sua maior ocorrência é no período de inverno.
Broca-do-olho do coqueiro (Rhynchophorus palmarum):
Causa danos na parte apical do caule de palmeiras e coqueiros em fase de produção. Além disso, podem transmitir uma doença conhecida como anel-vermelho-do-coqueiro. O sintoma dessa doença é o contínuo amarelecimento das folhas.
Amostragem:
Como não existem resultados de pesquisa que definam sistemas de amostragem e índices de decisão de controle para as pragas de plantas ornamentais no Brasil, será proposto a seguir uma forma para realização dos processos de acordo com os grupos de pragas anteriormente citados. Como para planta ornamental o que importa na maioria das vezes é o aspecto visual o índice considerado será o nível estético, ou seja, aquele em que a planta está em condições inadequadas para comercialização.
- Amostragem das pragas:
Para realização de amostragem primeiramente deve-se dividir o plantio em blocos. Cada bloco deve ser constituído de uma única cultura, genótipo, idade e sistema de cultivo, sendo que cada estufa deve fazer parte de blocos diferentes. Serão amostradas 1% das plantas de cada bloco.
- Mosca-branca, pulgão e tripes:
Batida de bandeja:
A batida de bandeja consiste na batida dos ponteiros com flores ou não, das plantas dentro de uma bandeja plástica de cor branca, onde se deve contar o número de ninfas e adultos que caem dentro. O nível estético para tripés, mosca-branca e pulgões é de 1 inseto/batida de bandeja.
Cartões adesivos:
Para a amostragem em casas de vegetação podem-se utilizar cartões adesivos, sendo que os cartões amarelos são mais atrativos aos pulgões e mosca branca e os azuis aos tripes.
Deve-se colocar o número de cartões equivalente ao número de plantas, ou seja 1% de cartões por talhão.
- Ácaros e cochonilhas:
Contagem direta:
A contagem direta é uma breve vistoriada da planta, onde se observa se há presença de ácaros ou cochonilhas na planta. Para ácaros a contagem de indivíduos deve ser feita com auxílio de uma lupa de 10x de aumento, avaliando-se 1 cm2 de área de limbo foliar na porção mediana da planta. O nível estético para ácaro é 10 % de plantas atacadas e para cochonilhas um inseto por amostra.
- Minadores:
Contagem direta:
Se a cultura for atacada por minadores de folhas, deve-se também realizar contagem direta de minas presentes nas plantas, em que se deve anotar a presença de minas nas folhas. O nível estético para mosca minadora é 10 % de plantas atacadas.
- Desfolhadores:
Contagem direta:
Deve-se fazer a contagem direta da percentagem de desfolha nas plantas. O nível estético para desfolhadores é 10 % de plantas atacadas.
- Broqueadores:
Para amostragem das pragas broqueadoras do caule (orquídeas), deverá se anotar se este está, ou não, atacado pela praga. Na amostragem de pragas de flores em vasos deverão ser amostrados cinco destes órgãos por planta, observando se estes estão ou não atacados por pragas. Neste caso, não há nível estético para broqueadores, pois somente a presença destas pragas indica praticamente a perda total da planta, o que recomenda é a retirada e eliminação de plantas atacadas.
Controle:
- Seleção do local de plantio;
- Obtenção de mudas e materiais propagativos sadios;
- Limpeza das instalações de cultivo e dos materiais utilizados:
A limpeza de todas as instalações como casas de vegetação e viveiros, além dos materiais utilizados como vasos, bandejas e ferramentas. Além disso, toda a parte interna das instalações (laterais, piso, teto, portas e estrados), deve ser tratada com inseticida e/ou acaricida para controle das pragas existentes. Após, as instalações devem permanecer sem cultivo pelo menos por duas semanas. Após este período deve ser realizada nova pulverização das instalações.
- Destruição dos restos culturais;
- Eliminar focos de pragas;
- Plantio de variedades atrativas a inimigos naturais;
- Plantio antecipado de variedades atrativas a pragas;
- Densidade de plantio;
- Controle do ambiente dentro das casas de vegetação:
Como os insetos são influenciados por vários fatores ecológicos, entre eles o fotoperíodo, quando se utiliza o lançamento de inimigos naturais em casas de vegetação para controle biológico é importante controlar algumas características do ambiente como luz, temperatura, umidade, etc. Exemplos disso são algumas espécies de Orius que em zonas temperadas hibernam como adultos em lugares secos e protegidos.
- Manejo das podas;
- Manejo da adubação;
- Manejo da irrigação;
- Uso de telas anti-afídeos:
Para evitar entrada de pragas nas casas de vegetações uma tática muito importante é o uso de telas anti-afídeos. É uma tela de pequeno diâmetro colocada em todas as laterais impedindo a entrada até mesmos de pragas menores como pulgões e permitindo, contudo uma boa ventilação. Além disso, é necessário vedar todos os buracos de possível entrada de insetos e manter as portas fechadas em todo momento.
- Plantio de plantas repelentes:
Algumas espécies de plantas são citadas, como repelentes de insetos. A maioria delas são plantas daninhas, portanto na hora de se executar as capinas deve-se deixá-las na área ou até mesmo realizar semeaduras. Como exemplos, têm-se o gerânio (Pelargonium hortorum) que impede a presença principalmente de pulgões. A hortelã (Menta piperita) que quando plantada nas bordaduras dos age como repelente de formigas. Além da capuchinha (Trapaeolium majus), que atura contra os pulgões.
- Controle químico;
2 Pragas de eucalipto:
Diagnose:
- Pragas de Viveiro:
a) Agrotis ipsilon (Lepidoptera):
Problemas são expressivos quando há grande quantidade de mudas na fase susceptível, que é logo nos primeiros dias ou semanas após a germinação, quando a lagarta alimenta-se de folhas e partes tenras apicais. Com o crescimento da muda e o enrijecimento do caule a voracidade da lagarta diminui e esta fica limitada a roer o caule da muda.
b) Térmitas - Cupins (Isoptera):
Destroem raízes, a planta fica amarelada e as folhas secam e caem.
c) Gryllus assimilis, Gryllotalpa hexadactyla (Orthoptera):
Comem raízes, caules e folhas de mudas novas e tenras de eucalipto. Atacam plantinhas, cortando-as à altura do coleto e transportam a parte aérea para abrigos.
- Insetos de Mudas no Campo:
a) Cupins subterrâneos: Syntermes insidians e Syntermes molestus (Isoptera);
b) Besouros Desfolhadores:
besouro-amarelo: Costalimaita ferruginea vulgata, besouro-pardo: Bolax flavolineatus, besouro-carneirinho: Asynonychus spp., Besouro-limeira: Sternocolaspis quatuordecimcostata (Coleoptera) - O ataque resulta no envassouramento e morte das mudas.
- Insetos de Tronco:
a) Serrador: Psyllotoxus griseocinctus (Coleoptera: Cerambycidae);
b) Besouros Ambrósia: Xyleborus, Platypus spp. (Coleoptera):
São broqueadores do lenho vivo das plantas. As larvas se alimentam de fungos que são cultivados nas galerias.
c) Cupins: Coptotermes testaceus (Isoptera):
Penetram na planta através das raízes e cicatrizes deixadas no tronco pela desrama natural. O dano causado por estes insetos, localiza-se a partir do coleto e alastra-se no sentido ascendente até alturas variadas.
d) Lepitobrocas: Timocratica albella, Phasus giganteus (Lepidoptera):
As larvas desses insetos broqueiam o tronco, fazendo galerias em vários sentidos.
- Insetos desfolhadores:
a) Formigas Cortadeiras: Saúvas: Atta spp., Acromyrmex spp. (Hymenoptera):
Cortam as folhas e pontas apicais para servir de meio de cultura para o fungo do qual se alimentam. Este ataque é bem caracterizado, porque se dá de cima para baixo.
b) Lagartas Desfolhadoras: Thyrinteina arnobia, Glena bipennaria bipennaria, Sabulodes caberata caberata, Oxydia vesulia, Eupseudosoma involuta, Eupseudosoma aberrans, Sarsina violascens, Blera varana, Psorocampa denticulata e Apatelodes sericea (Lepidoptera).
O ataque da maioria dos lepidópteros desfolhadores ocorre de forma semelhante, são ávidas comedoras de folhas e não há como negar que os surtos trazem grandes prejuízos.
Amostragem:
a) Lepidópteros desfolhadores:
Devemos amostrar o local da seguinte forma:
- Dividir a área em parcelas de 30 a 60 ha e de acordo com o tamanho da quadra;
- Amostrar 9 árvores/parcela;
- Contar o número de lagartas em 100 folhas;
- Fazer a contagem nos galhos, nos quatro lados da árvore, sendo 25 por lado.
Devemos avaliar nessa amostragem:
- Estádio em que se encontra as lagartas;
- Número de posturas;
- Número de pré-pupas e pupas;
- Número de adultos (machos e fêmeas);
- Desfolha da árvore e desfolha média das árvores vizinhas;
- Presença de lagartas mortas e de inimigos naturais.
- Luz:
Pode ser feito para monitoramento da área e para controle, nesse último caso, recomenda-se aplicar produtos químicos nas árvores próximas a este local.
Controle:
a) No viveiro:
Com a utilização de sacos plásticos, contribuiu-se para que fosse minimizado os danos causados pelos cupins, pois este age como uma barreira para estes insetos. Os tubetes, determinaram uma redução acentuada do ataque de cupins, lagarta-rosca, grilos e paquinhas.
- Armadilhas luminosas;
- Catação manual;
- Limpeza ao redor do viveiro;
- Viveiro temporário;
- Controle silvicultural (revolver a terra);
- Controle biológico natural;
- Controle químico.
b) Mudas no Campo:
Para cupins:
- Uso de tratamentos alternativos: Aplicação de produtos químicos pode ser feita das seguintes maneiras: aplicação na cova, imersão dos recipientes e aplicação na mistura;
- Determinação prévia da existência ou não de cupins na área.
Para besouros desfolhadores:
São restritos a determinados períodos, fazendo com que o monitoramento constitua numa prática que indique a época adequada de controle, quando necessário.
c) Insetos de Tronco:
Eliminar árvores infestadas, derrubando e queimando, evitar o transporte dessas para outros locais, pois estas podem ser veículo de disseminação das pragas. Inspeções periódicas bem feitas para se proceder a eliminação de focos. Utilização de armadilhas ou árvores armadilhas com etanol para atração desses insetos.
d) Formigas Cortadeiras;
e) Outros métodos de controle.
3 Formigas cortadeiras:
Biologia das formigas cortadeiras:
As saúvas (Atta spp.) e as quenquéns (Acromyrmex spp.) (Hymenoptera) são insetos sociais e normalmente são muito ativas durante a noite, mas em locais sombreados e durante períodos frios a atividade de corte e forrageamento pode ocorrer durante o dia.
- Principais diferenças entre os gêneros Atta e Acromyrmex:
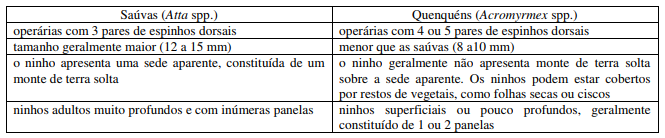
- Injúrias: Causam desfolhas.
a. Constituição de um sauveiro:
- Na superfície do solo, os sauveiros apresentam monte de terra solta e orifícios por onde saem as operárias, denominados olheiros.
- Na porção subterrânea, existem as câmaras conhecidas como panelas e as galerias ou canais (interligam as panelas) e esta porção apresenta 2 zonas, nem sempre bem distintas: na zona morta predominam as panelas de lixo, com terra ou panelas vazias; e na zona viva, existem as panelas com fungo, ovos, larvas e a rainha.
- A sede aparente é a área do solo coberta com terra solta - o murundum.
- A sede real é aquela onde na sua porção subterrâneas está localizada a zona viva. Na maioria das espécies de saúvas, a sede real quase se superpõe à sede aparente, exceto em Atta capiguara, que coincide com a área de olheiros ativos fora do murundum e nestes olheiros podem ocorrer montículos de terra solta, parecidos com discos.
b. Castas de um sauveiro:
- As castas temporárias são responsáveis pela formação de novos formigueiros, - As colônias de saúva são monogínicas (uma única rainha), já as de quenquém são poligínicas. Há referências que a rainha de saúva sobrevive no período médio de até 20 anos., e esta é insubstituível.
- As jardineiras são as menores formigas da colônia (< 2 mm), e sua função é a incorporação do vegetal na massa de fungo, cuidam da prole (ovos e larvas) e da rainha. As cortadeiras apresentam porte médio (4 a 7 mm) e executam tarefas de corte e transporte do alimento para o ninho, escavação das panelas e canais, descarte do lixo. Os soldados são as “cabeçudas” (> 7 mm), possuindo mandíbulas fortíssimas são responsáveis pela defesa da colônia e proteção da rainha e dos alados (castas temporárias).
c. Etapas para formação de um sauveiro:
Fase I :
- Anicia-se com a fecundação da içá durante o vôo nupcial. Depois de fecundadas toda as rainhas têm condições de fundar um formigueiro, porém apenas 0,05% têm sucesso;
- A rainha recém fecundada, corta suas asas e inicia a escavação de um pequeno canal (cerca de 15 cm de profundidade);
- Após a rainha inicia a construção da 1a. câmara (panela com cerca de 4 cm de diâmetro), cuja terra é usada para obstruir a entrada;
- 2 dias após a revoada, a rainha regurgita o micélio de fungo, que coletou antes do vôo nupcial;
- Os primeiros ovos são postos 5 a 6 dias após a revoada. As primeiras larvas, pupas e adultos aparecem 30, 50 e 62 dias após a revoada, respectivamente;
- As primeiras formigas permanecem no interior da panela por 20 dias, antes de iniciarem a obstrução do canal feito pela içá.
Fase II:
- Após a reabertura do canal, as operárias iniciam o corte e o transporte do material vegetal e a rainha se dedica exclusivamente à postura;
- A abertura do 1° olheiro se dá em média, 87 dias após a penetração da içá no solo. O segundo aparece 14 meses após a abertura do 1°. Os outros sucedem-se rapidamente e em 82 dias, em média, são abertos 8 olheiros (do 3° ao 10º). Portanto, o 10º olheiro é aberto 20 meses após a fundação;
- Ao atingir 2 anos de idade, as saúvas já abriram 120 olheiros e aos 3 anos, com até 700 olheiros, o formigueiro torna-se adulto e produz a sua 1o revoada, que se dará anualmente;
- O número de içás liberados por sauveiro chega a 5000 por revoada;
- Durante a revoada as içás podem atingir 1 Km de distância e 100 m de altura.
d. Principais espécies de saúvas:
Atta sexdens rubropilosa (“saúva limão”): cheiro de limão, cortam dicotiledôneas, soldados opacos e de coloração pardo a avermelhada, montes de terra solta irregulares.
Atta laevigata (“saúva cabeça-de-vidro”): cortam monocotiledôneas e dicotiledôneas (maior preferência), soldados com cabeça muito brilhante, monte de terra solta arredondado e de maior espessura.
Atta bisphaerica (“saúva mata pasto”): cortam monocotiledônea, soldados com certo brilho e dois lóbulos característicos na cabeça, monte de terra solta espalhada.
Atta capiguara (“saúva parda”): cortam preferencialmente gramíneas, soldados semelhantes ao da “saúva limão”, porém quando esmagados não cheiram a limão, produzem odor semelhante ao de gordura rançosa.
Amostragem:
a. Pequenos produtores: pomares de frutíferas, viveiros, hortas e outras culturas agrícolas.
- Controle imediato após sua constatação na área (praga-chave severa);
- Controle deve ser feito na propriedade e áreas adjacentes (um sauveiro adulto tem capacidade de ataque de até 400 m de distância).
b. Grandes produtores:
- Para grandes áreas de pastagens e cultivos agrícolas, não existe metodologias de amostragem e nem definição de NC;
- As grandes empresas florestais se utilizam de “softwares” para tomadas de decisão impíricas e de sistemas de monitoramento..
Controle:
a. Controle cultural:
- Arações sucessivas para eliminação de panelas superficiais de Acromyrmex e de sauveiros iniciais (3 a 4 meses após a revoada).
- Uso de barreiras de proteção: pequenos canais cheios de água, ao redor da planta; uso de frascos plástico de refrigerante com graxa, colocada na base do tronco da planta; recipiente com formato de bacia em anel ou pneu velho partido ao meio, cheios de água, ao redor da árvore ou muda.
b. Controle biológico natural:
- Mais acentuado durante a revoada: pássaros, aves domésticas, aranhas, sapos, rãs, lagartos, besouros, tatus e tamanduá realizam eficiente controle, sobretudo das fêmeas aladas.
c. Plantas resistentes e tóxicas:
- Espécies de Eucalyptus menos preferidas a A. sexdens rubropilosa e A. laevigata: E. citriodora, E. grandis, E. maculata, E. nova-anglica, E. deanei, E. acmenioides, E. andrewsii e E. propingua.
- Dentre estes pode-se destacar: mamona (Ricinus communis), gergelim (Sesanum indicum), inhame-amarelo (Diocorea cayanensis cayanensis), batata-doce (Ipomea batatas), fava-branca (Centrosema brasilianus) e jatobá (Hymenaea courbaril).
d. Controle químico:
Formicidas usados:
Pós-secos:
- Aplicação nos olheiros através de bombas manuais (“tamanduá”);
- Aplicados na época seca. O solo deve estar seco até a 30 cm de profundidade, senão o pó umidece e aderindo-se à superfície interna dos canais, provoca entupimento.
- Iscas granuladas:
- Técnica eficiente (depende de cuidados especiais durante a aplicação) e de baixo custo;
- Cuidado com o dimensionamento da área do formigueiro para não provocar sub ou super dosagem, o que poderá acarretar em aumento do formigueiro e desperdícios, respectivamente;
- Cálculo da área do formigueiro:
- Para Atta capiguara: é calculada, medindo-se o maior comprimento pela maior largura do retângulo formado pelo monte de terra solta mais a área de montículos menores e canais situados ao longo do montículo de terra solta;
- Para as demais espécies de Atta: maior comprimento do monte de terra solta x maior largura do monte de terra solta. Formuladas geralmente com casca de laranja, que funciona como um atraente (pouco eficiente para Atta bisphaerica). Devem ser aplicadas na época seca e evitar contato da isca com a umidade do solo. Em extensos plantios, utiliza-se micro-porta-iscas (sacos de polietileno, contendo de 10 a 30 g de isca e ao ser encontrado é rasgado pelas próprias formigas). Outro método de aplicação utilizado são as “isqueiras” (plantadeiras modificadas e adaptadas em tratores). Aplicar 20 cm em torno dos olheiros de carregamento e ao lado das trilhas de forrageamento. Não colocar sobre os olheiros e nem dentro da trilha!
- Termonebulização:
- Usar aplicador motorizado (termonebulizador) que aquece o óleo mineral presente no produto comercial, formando uma corrente de ar quente (fumaça), que arrasta as partículas do inseticida. As formigas morrem por contato com a fumaça tóxica ou por ingestão do fungo contaminado;
- A aplicação deve visar a zona viva, portando deve fazer a aplicação da fumaça nos olheiros ativos;
- Controle é eficiente para formigueiros de todos os portes, não depende das condições climáticas, promove rápida paralização das atividades da colônia;
- Restrições do método: requer constantes manutenções de equipamentos, treinamento de operadores, dificuldade de transporte com os equipamentos em áreas extensas e riscos de incêndios.
4 Pragas de grãos armazenados:
- PERDAS CAUSADAS POR PRAGAS DE PRODUTOS ARMAZENADOS:
- Quantitativas (consumo do grão);
- Qualitativas (contaminação dos produtos armazenados).
- OCORRÊNCIAS DE PERDAS:
- No campo;
- No transporte;
- No armazenamento.
Classificação das pragas de produtos armazenados:
A. Quanto ao hábito alimentar:
- A.1. Pragas primárias: Aquelas capazes de romperem os grãos intactos.
A.1.1 Internas: Rompem os grãos e alimentam-se do seu conteúdo interno.
Ex.: Sitophilus zeamais e Acanthoscelides obtectus (Coleoptera), Sitotroga cerealella (Lepidoptera).
A.1.2. Externas: Alimentam-se dos grãos externamente, podendo atacar a parte interna.
Ex: Lasioderma serricorne e Rhizopertha dominica (Coleoptera), Plodia interpunctella (Lepidoptera).
- A.2. Pragas secundárias: São incapazes de romperem os grãos intactos, ação comumente associada às primárias.
Ex.: Tribolium castaneum, T. confusum (Coleoptera).
- A.3. Pragas associadas: Encontradas nos grãos, mas não os atacam. Alimentam-se de detritos e fungos, podendo alterar a qualidade do produto.
Ex.: Psocoptera e Ácaros.
- A.4. Pragas acidentais: Raramente danificam os grãos.
- A.5. Inimigos naturais: Patógenos, predadores, parasitóides e parasitas.
B. Quanto ao produto armazenado:
- B.1. Cereais (arroz, milho, sorgo e trigo).
a) Gorgulhos: Sitophilus zeamais, S. oryzae (Coleoptera);
b) Traças: Sitotroga cerealella e Plodia interpunctella (Lepidoptera);
c) Besouros: Oryzeaphilus surinamensi, Tribolium castaneum e Rhyzopertha dominica (Coleoptera).
- B.2. Feijão:
a) Carunchos: Zabrotes subfasciatus, Callosobruchus maculatus e Acanthocelides obtectus (Coleoptera);
b) Traça: Plodia interpunctella (Lepidoptera).
- B.3. Soja:
a) Traça: Plodia interpunctella (Lepidoptera);
b) Besourinho do fumo: Lasioderma serricorne (Coleoptera).
- B.4. Farinhas:
a) Traças: Pyralis farinalis, Anagasta kuehniella (Lepidoptera);
b) Besouros: Tenebrio molitor, Stegobium paniceum, Tenebroides mauritanicus, Oryzaephilus surinamensis, Tribolium confusum, T. Castaneum (Coleoptera).
- B.5. Café:
a) Carunchos das tulhas: Araecerus fasciculatus (Coleoptera);
b) Traça: - Corcyra cephalonica (Lepidoptera)
Sistema de monitoramento de pragas:
a) Termometria:
Esse sistema tem por objetivo o monitoramento da temperatura da massa de grãos, feito através de sensores presentes em cabos termométricos que medem a temperatura da massa de grãos ao longo de sua extensão. O princípio desse sistema de monitoramento, baseia-se no fato de que a presença de insetos na massa de grãos eleva a temperatura devido ao seu próprio metabolismo.
b) Acústico:
Esse sistema baseia-se no fato de que o inseto ao se movimentar na massa de grãos provoca sons. Assim sensores acústicos, instalados dentro da massa de grãos por meio de cabos, à semelhança de um sistema de termometria, permitem uma boa estimativa do nível de infestação das pragas em todo o volume de um silo.
c) Armadilha-sonda eletrônica contadora de insetos:
O monitoramento dos insetos é feito através de armadilhas do tipo sondas-perfuradas dotadas de sensores óticos. Esse sistema é conectado à um computador e toda vez que um inseto entra na armadilha ele é contado pelo sensor ótico e essa informação é transmitida ao computador.
- NÍVEIS DE CONTROLE:
Até o momento não existem níveis de controle para as pragas de grãos armazenados, entretanto estudos estão sendo realizados para se conseguir esses níveis.
Táticas de controle:
a) Inspeção das instalações e produtos armazenados:
a1). Exame visual: Peneiramento do produto e inspeção visual (para detecção);
a2). Infestação interna: Método de coloração (para distinção da praga dentro do produto armazenado). Método de flotação (separação do produto contaminado do sadio por diferença de densidade) e Método de raio-X (verificação de presença da praga dentro do grão).
b) Limpeza das instalações:
- Constitui o meio mais eficiente de controle preventivo;
- A área ao redor, instalações e os equipamentos devem ser mantidos limpos.
c) Métodos físicos e mecânicos de controle:
a) Métodos físicos: Temperatura e umidade do produto armazenado.
b) Métodos mecânicos: Uso de impacto, barreiras (envoltórios resistentes) e armadilhas.
d) Métodos químicos de controle:
a) Inseticidas fumigantes: Produtos químicos que produzem vapores ou gases tóxicos, inseticida utilizado: Fosfina.
Fosfina :
- Pode ser utilizada em sementes, grãos e farinhas;
- O tempo de exposição recomendado é de 120 horas;
- É tóxico à todas as fases de vida do inseto : ovo, larva, pupa e adulto;
e) Métodos legislativos:
- Leis que visam, através de quarentena, impedir a entrada de pragas exóticas.
Ex.: Os besouros Bruchidius spp. de grãos de ervilha no armazenamento na Europa e ainda não existente no Brasil: Trogoderma granarium e Prostephanus truncatus.
f) Métodos comportamentais:
- Uso de técnicas de insetos estéreis (que competem com os insetos não estéreis na reprodução);
- Uso de feromônios (substâncias responsáveis pela comunicação química intraespecífica).
Ex.: Essas substâncias podem ser usadas no monitoramento e controle de pragas de produtos armazenados.
- Uso do feromônio "Serricornin" no controle de Lasioderma serricorne em galpões de secagem de folhas de fumo.
g) Controle biológico:
- Uso de patógenos, predadores, parasitas e parasitódes no controle de pragas dos produtos armazenados.
Ex.: A bactéria Bacillus thuringiensis é registrada em vários países para o controle de lagartas que atacam produtos armazenados.
h) Atmosfera modificada:
- Em armazéns herméticos é modificada a "atmosfera" que envolve os produtos armazenados, de tal forma que controle as pragas desses produtos.
Ex.: Uso de baixas concentrações de oxigênio em atmosfera rica em, nitrogênio ou dióxido de carbono constituem método alternativo para prevenção de perdas causadas por pragas aos produtos armazenados.
i) Substratos inertes:
- Substratos como argila e calcário filler têm capacidade de remoção da camada de cera da cutícula dos insetos, ocasionando a morte desses por dessecação.
Ex.: Uso de terra de "formigueiro".
j) Uso de plantas e extratos de plantas:
- Ex: A planta Azadirachta indica que apresenta o composto Azadirachtin que tem ação repelente e fagoinibidora para diversos insetos, como por exemplo, Rhyzopherta dominica e Tribolium castaneum.