Manual Prático de Análise de Água
NOÇÕES BÁSICAS EM VIGILÂNCIA AMBIENTAL EM SAÚDE
1 Manual Prático de Análise de Água
Bactérias do grupo coliforme:
Conceito:
Denomina-se de bactérias do grupo coliforme bacilos gram negativos, em forma de bastonetes, aeróbios ou anaeróbios facultativos que fermentam a lactose a 35-37ºC, produzindo ácido, gás e aldeído em um prazo de 24-48 horas. São também oxidase-negativos e não formam esporos. A razão da escolha desse grupo de bactérias como indicador de contaminação da água deve-se aos seguintes fatores:
• estão presentes nas fezes de animais de sangue quente, inclusive os seres humanos;
• sua presença na água possui uma relação direta com o grau de contaminação fecal;
• são facilmente detectáveis e quantificáveis por técnicas simples e economicamente viáveis, em qualquer tipo de água;
• possuem maior tempo de vida na água que as bactérias patogênicas intestinais, por serem menos exigentes em termos nutricionais, além de ser incapazes de se multiplicarem no ambiente aquático;
• são mais resistentes à ação dos agentes desinfetantes do que os germes patogênicos.
A Contagem Padrão de Bactérias é muito importante durante o processo de tratamento da água, visto que permite avaliar a eficiência das várias etapas do tratamento.
É importante, também, conhecer a densidade de bactérias, tendo em vista que um aumento considerável da população bacteriana pode comprometer a detecção de organismos coliformes. Embora a maioria dessas bactérias não seja patogênica, pode representar riscos à saúde, como também, deteriorar a qualidade da água, provocando odores e sabores desagradáveis.
As técnicas adotadas neste manual para quantificar os coliformes e heterótrofos na água são as preconizadas no Standard Methods for the Examination of Water and Wastewater publicação da American Public Health Association (APHA), American Water Works Association (AWWA) e Water Environment Federation.
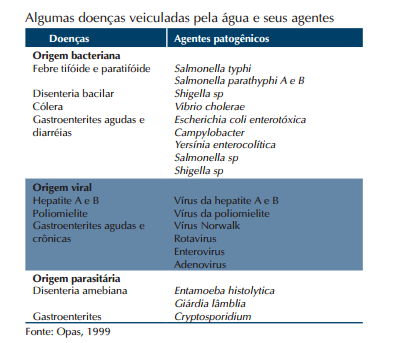
Material utilizado em bacteriologia
a) autoclave;
b) estufa bacteriológica;
c) estufa de esterilização e secagem;
d) balança;
e) destilador;
f) banho-maria;
g) contador de colônias;
h) alça de platina com cabo;
i) tubo de Durhan;
j) tubo de ensaio;
k) algodão em rama;
l) meios de cultura;
m) frascos de coleta;
n) pipetas graduadas;
o) papel-alumínio;
p) lamparina a álcool ou bico de Bunsen;
q) placas de Petri;
r) pinça de aço inox;
s) membranas filtrantes; porta-filtro de vidro ou aço inox; lâmpada ultravioleta.
2 Introdução:
A água potável não deve conter microrganismos patogênicos e deve estar livre de bactérias indicadoras de contaminação fecal. Os indicadores de contaminação fecal, tradicionalmente aceitos, pertencem a um grupo de bactérias denominadas coliformes. O principal representante desse grupo de bactérias chama-se Escherichia coli.
A Portaria nº 518/2004 do Ministério da Saúde estabelece que sejam determinados, na água, para aferição de sua potabilidade, a presença de coliformes totais e termotolerantes de preferência Escherichia coli e a contagem de bactérias heterotróficas. A mesma portaria recomenda que a contagem padrão de bactérias não deve exceder a 500 Unidades Formadoras de Colônias por 1 mililitro de amostra (500/UFC/ml).

3 Preparo do material de vidro:
Tubos de ensaio:
a) colocar o tubo de Durhan na posição invertida dentro do tubo de ensaio;
b) tampar o tubo de ensaio com um chumaço de algodão em rama.
Frascos de coleta:
a) colocar duas gotas (0,1 ml) de Tiossulfato de Sódio a 10% dentro do frasco;
b) colocar uma tira de papel-alumínio entre a boca e a tampa do frasco;
c) envolver a boca e tampa do frasco em papel-alumínio.
Pipetas:
a) colocar um pequeno chumaço de algodão no bocal da pipeta;
b) envolvê-la em papel-alumínio ou papel-madeira (Kraft).
Placas de petri de vidro:
a) envolvê-las em papel-alumínio ou papel-madeira.
Meios de cultura:
a) caldo lactosado;
b) caldo lactosado verde brilhante Bile a 2%;
c) caldo EC;
d) Plate Count Agar
4 Preparação dos meios de cultura:
Caldo lactosado de concentração dupla:
a) pesar 26 gramas do meio de cultura e dissolver em 1.000 ml de água destilada;
b) distribuir em tubos de ensaio (10 ml em cada tubo), tampar os tubos;
c) esterilizar a 121º C (1 Kg/cm2 de pressão) em autoclave durante 15 minutos;
d) deixar esfriar;
e) guardar no refrigerador (válido por uma semana).
Caldo lactosado de concentração simples:
a) pesar 13 gramas do meio de cultura desidratado e dissolver em 1.000 ml de água destilada;
b) distribuir em tubos de ensaio (10 ml em cada tubo), tampar os tubos;
c) esterilizar a 121º C (1 Kg/cm2 de pressão) em autoclave durante 15 minutos;
d) deixar esfriar;
e) guardar no refrigerador (válido por uma semana).
Caldo lactosado verde brilhante bile a 2%:
a) pesar 40 gramas do meio de cultura desidratado e dissolver em 1.000 ml de água destilada;
b) distribuir em tubos de ensaio (10 ml em cada tubo), tampar os tubos;
c) esterilizar a 121º C (1 Kg/cm2 de pressão) em autoclave durante 15 minutos;
d) deixar esfriar;
e) guardar no refrigerador (válido por uma semana).
Meio EC:
a) pesar 37,0 gramas do meio desidratado e dissolver em 1000 ml de água destilada;
b) distribuir em tubos de ensaio contendo o tubo Durhan invertido, 10 ml em cada tubo, tampar os tubos;
c) esterilizar a 121º C (1Kg/cm2 de pressão) em autoclave durante 15 minutos;
d) guardar no refrigerador (Válido por 96 horas).
Plate Count Agar:
a) pesar 20,5 gramas do meio de cultura desidratado e dissolver em 1000 ml de água destilada fria;
b) deixar em repouso durante 5 minutos;
c) aquecer, agitando frequentemente com bastão de vidro, até completa dissolução do meio (durante o aquecimento não deixar entrar em ebulição);
d) se necessário, ajustar o pH para 7,0 com Hidróxido de Sódio solução normal (NaOH 1N);
e) distribuir em tubos de ensaio com tampa rosqueável (12 ml em cada tubo );
f) esterilizar a 121º C (1 Kg/cm2 de pressão) em autoclave durante 15 minutos.
5 Água de diluição:
Solução 1:
- Pesar 34 gramas de Fosfato de Potássio Monobásico (KH2PO4) e dissolver em 500 ml de água destilada, ajustar o pH para 7,2 com Hidróxido de Sódio, solução normal (NaOH 1N) e diluir a 1 litro com água destilada. Normalmente são necessários 175 ml de NaOH 1N para elevar o pH.
Solução 2:
- Pesar 81,1 gramas de Cloreto de Magnésio hexahidratado (MgCl2 .6H2 O) e dissolver em 1 litro de água destilada.
Solução 3:
- Adicionar 1,25 ml da solução 1 e 5 ml da solução 2 a 1 litro de água destilada. Distribuir em tubos de ensaio em quantidade que, após autoclavação, assegurem um volume de 9 ± 0,2 ml.Esterilizar em autoclave a 121º C (1Kg/cm2 de pressão) durante 15 minutos.
Modo de usar a água de diluição quando for determinar o NMP de coliformes:
a) tomar 1 tubo de ensaio contendo 9 ± 0,2 ml de água de diluição esterilizada;
b) adicionar 1 ml da amostra de água a ser examinada;
c) misturar bem. Está pronta a diluição 1:10;
d) tirar da diluição acima, com pipeta esterilizada, 1 ml e inocular no tubo contendo caldo lactosado de concentração simples. (diluição 1:100).
Coleta de amostras de água para exames bacteriológicos:
As amostras devem ser coletadas em frascos de vidro branco, boca larga, com tampa de vidro esmerilhada, bem ajustada, capacidade de 125 ml, previamente esterilizados ou saco plástico estéril, descartável, contendo pastilha de tiossulfato de sódio.
Os frascos para a coleta de águas cloradas devem receber, antes de serem esterilizados, 0,1 ml (2 gotas) de tiossulfato de sódio a 10%.
Procedimentos para coleta em residências:
a) lavar as mãos com água e sabão;
b) limpar a torneira do usuário com um pedaço de algodão embebido em álcool;
c) abrir a torneira e deixar escorrer a água durante 1 ou 2 minutos;
d) fechar e flambar a torneira;
e) abrir novamente a torneira e deixar escorrer por mais 2 ou 3 minutos;
f) coletar a amostra de água;
g) encher com pelo menos ¾ de seu volume;
h) tampar o frasco, Identificá-lo, anotando endereço, a hora e a data da coleta, o estado do tempo, o nome do coletor, etc;
i) marcar o frasco com o número da amostra, correspondente ao ponto de coleta;
j) preencher a ficha de identificação da amostra de água;
k) colocar o frasco da amostra na caixa de isopor com gelo;
l) lacrar, identificar e enviar a caixa para o laboratório. O tempo de coleta e a realização do exame não deve exceder 24 horas;
Fases do procedimento:
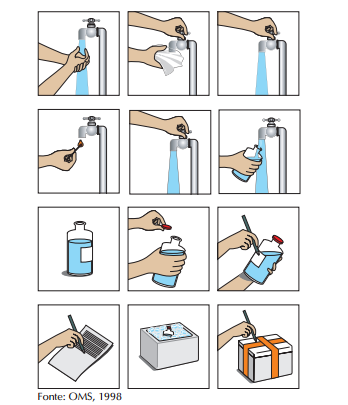
Outros locais de coleta:
Nas estações de tratamento, as amostras são coletadas na captação (água bruta), nos decantadores, na saída dos filtros e nos reservatórios de água tratada.
6 Coliformes totais:
Método dos tubos múltiplos:
Material necessário:
a) tubo de ensaio.
b) estante para tubo de ensaio.
c) tubo de Durhan.
d) pipeta graduada de 10 ml.
e) pipeta graduada de 1 ml.
f) bico de Bunsen ou lamparina a álcool.
g) caldo Lactosado de concentração dupla.
h) caldo Lactosado de concentração simples.
i) caldo Lactosado Verde Brilhante Bile a 2%.
j) água de diluição.
k) alça de platina com cabo de Kolle.
l) estufa bacteriológica.
7 Execução do teste:
Teste presuntivo:
a) tomar uma bateria contendo 15 tubos de ensaio distribuídos de 5 em 5;
b) nos primeiros 5 tubos, (os que contêm caldo lactosado de concentração dupla) inocular com pipeta esterilizada, 10 ml da amostra de água a ser examinada, em cada tubo. (Diluição 1:1);
c) nos 10 tubos restantes (os que contêm caldo lactosado de concentração simples), inocular nos 5 primeiros, 1 ml da amostra (Diluição 1:10) e nos 5 últimos tubos, inocular 0,1 ml da amostra, em cada tubo. (Diluição 1:100). Ver página 15;
d) misturar;
e) incubar a 35 ± 0,5º C durante 24/48 horas;
f) se no final de 24/48 horas, houver a formação de gás dentro do tubo de Durhan, significa que o teste Presuntivo foi Positivo. Neste caso, fazer o teste confirmativo. Se não houver a formação de gás durante o período de incubação, o exame termina nesta fase e o resultado do teste é considerado negativo.
Observação:
No lugar do caldo Lactosado pode ser usado o caldo Lauril Triptose.
Teste confirmativo:
a) tomar o número de tubos do Teste Presuntivo que deram Positivos (Formação de gás) nas 3 diluições 1:1; 1:10 e 1:100;
b) tomar igual número de tubos contendo o meio de Cultura Verde Brilhante Bile a 2%;
c) com a alça de platina, previamente flambada e fria, retirar de cada tubo positivo uma porção de amostra e inocular no tubo correspondente contendo o meio Verde Brilhante. Este procedimento chama-se repicagem;
d) identificar os tubos;
e) incubar durante 24/48 horas a 35 ± 0,5ºC;
f) se no final do período de 24/48 horas houver a formação de gás dentro do tubo de Durhan o teste é considerado Positivo. Caso não haja formação de gás, o teste é considerado negativo.
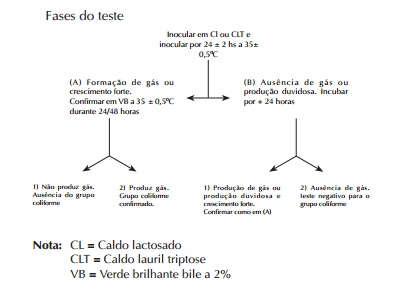
Expressão dos resultados:
a) os resultados são expressos em N.M.P (Número Mais Provável) /100 ml de amostra.
b) para se determinar o N.M.P, verifica-se a combinação formada pelo número de tubos positivos que apresentaram as diluições 1:1; 1:10 e 1:100 no Teste Confirmativo.
Exemplo:
a) nos 5 tubos da diluição 1:1, obtiveram-se 3 tubos positivos;
b) nos 5 tubos da diluição 1:10, obtiveram-se 2 tubos positivos;
c) nos 5 tubos da diluição 1:100, obteve-se 1 tubo positivo;
d) formou-se, portanto, a combinação 3-2-1;
e) determina-se o N.M.P consultando a tabela 1.
Se não quiser trabalhar com 15 tubos para determinar o NMP fazer apenas 5 tubos na diluição 1:1 (10 ml do meio de cultura + 10 ml da amostra) e calcular o NMP consultando a tabela 2.
Tabela 1 – do NMP:
Com limite de confiança de 95% para várias combinações de resultados positivos quando 5 tubos são usados para cada diluição (10 ml, 1,0 ml e 0,1 ml).
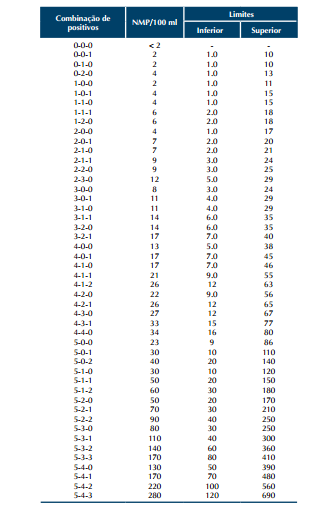
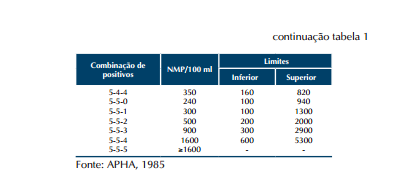
Tabela 2 – do NMP:
Com limite de confiança de 95% para os resultados positivos quando 5 porções de 10 ml são examinadas.
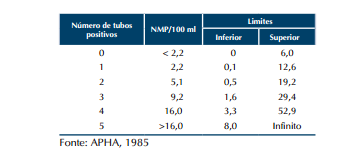
8 Coliformes termotolerantes:
Método dos tubos múltiplos:
Material necessário:
a) tubos de ensaio com Meio EC;
b) bico de Bunsen ou lamparina a álcool;
c) alça de platina;
d) banho-maria.
Execução do ensaio:
a) tomar todos os tubos do Teste Presuntivo que deram Positivos (Formação de gás) e todos os tubos negativos em que houve crescimento após 48 horas, nas 3 diluições (1:1; 1:10 e 1:100);
b) transferir, com alça de platina flambada e fria, uma porção para os tubos de ensaio contento o meio EC;
c) misturar e deixar todos os tubos em banho de água durante 30 minutos;
d) incubar em banho-maria a 44,5 ± 0,2º C durante 24 ± 2 horas;
e) se no final de 24 horas ou menos houver a formação de gás, está indicado a presença de coliformes de origem fecal;
f) calcular o N.M.P consultando a tabela 1.
Nota: Este ensaio deve ser realizado simultaneamente com o Teste Confirmativo para Coliformes Totais.
Observação:
Fazer sempre este exame toda vez que forem realizados testes confirmativo para coliformes totais.
9 Contagem padrão de bactérias:
Bactérias heterotróficas:
Material necessário:
a) placa de Petri;
b) pipeta graduada;
c) bico de Bunsen ou lamparina a álcool;
d) plate Count Agar;
e) estufa bacteriológica;
f) contador de colônia.
Execução do ensaio:
a) transferir, com pipeta estéril, 1 ml da amostra para uma placa de Petri previamente esterilizada;
b) entreabrir a placa e adicionar o meio de cultura, previamente fundido e estabilizado em banho-maria a 44-46ºC, contido no tubo de ensaio;
c) homogeneizar o conteúdo da placa em movimentos circulares moderados em forma de ( ∞ ), em torno de 10 vezes consecutivas;
d) quando o meio de cultura se solidificar, incubar a placa em posição invertida a 35 ± 0,5º C durante 48 ± 3 horas;
e) no final do período de incubação, fazer a contagem das colônias com o auxílio de um contador de colônias.
Expressão dos resultados:
Os resultados são expressos como nº de Colônias de bactérias/ ml ou Unidades Formadoras de Colônias (UFC)/ml.
a) antes de iniciar os exames desinfetar a bancada do laboratório, usando uma solução de álcool etílico a 70% ou outro desinfetante que não deixe resíduo;
b) todas as amostras a serem examinadas devem ser homogeneizadas pelo menos 25 vezes;
c) não esquecer de flambar a boca dos tubos de ensaio contendo meios de cultura, antes de usá-los;
d) o Tiossulfato de Sódio a 10% colocado nos frascos de coleta é para neutralizar a ação do cloro;
e) as placas de Petri devem ser colocadas na posição invertida para evitar a condensação de água na superfície do ágar;
f) fazer a Contagem Padrão de Bactérias, sempre em duplicata.
10 Coliformes totais:
Método da membrana filtrante:
Material necessário:
a) equipamento de filtração com porta-filtro;
b) placa de Petri esterilizada de Ø 47 mm;
c) filtros de membrana de Ø 47 mm e porosidade de 0,45µm, com cartão absorvente;
d) meio de cultura (M ENDO MF);
e) água de diluição estéril;
f) pinça de aço inox;
g) copo de aço inox;
h) bico de Bunsen ou lamparina a álcool;
i) bomba de vácuo (Seringa);
j) estufa bacteriológica.
Execução do ensaio:
a) com a pinça, colocar cuidadosamente na placa de Petri um cartão absorvente;
b) com pipeta esterilizada colocar 1,8 ml do meio de cultura no cartão absorvente e tampar a placa;
c) colocar a membrana filtrante no porta-filtro, com a pinça previamente flambada e fria;
d) agitar o frasco contendo a amostra, pelo menos 25 vezes;
e) destampar e flambar a boca do frasco;
f) verter, cuidadosamente, 100 ml de amostra no portafiltro, evitando que a água respingue sobre as bordas superiores;
g) ligar a bomba de vácuo (seringa) e fazer a sucção;
h) após filtrada a amostra, lavar 3 vezes as paredes do funil com água de diluição estéril com porções de 20 ml aplicando vácuo;
i) após a lavagem e filtração, aliviar o vácuo e remover o funil do suporte;
j) com a pinça flambada e fria, remover o filtro do suporte e colocá-lo na placa de Petri, antes preparada, com o lado quadriculado para cima;
k) tampar a placa de Petri e incubá-la invertida a 35º C durante 24 ± 2 horas;
l) após o período de incubação, examinar o filtro fazendo a contagem das colônias.
Leitura dos resultados:
As colônias indicativas de Coliformes Totais típicas têm uma cor rosa a vermelho escuro, com brilho metálico. O brilho pode aparecer no centro ou na periferia da colônia.
As não coliformes aparecem com coloração vermelho-clara ou escura sem o brilho metálico característico.
Observação:
Às vezes, quando o disco está muito úmido e a fonte de luz é muito intensa, as colônias de não Coliformes podem aparecer com um brilho falso, causando erros. Isto poderá ser contornado usando-se fonte de luz mais difusa ou secando-se o filtro antes de ser examinado.
11 Preparo do meio de cultura:
Material necessário:
a) meio de cultura desidratado (M ENDO MF);
b) água destilada;
c) álcool etílico a 95%;
d) frasco Erlenmeyer de 125 ml;
e) vidro de relógio;
f) bico de Bunsen ou lamparina a álcool.
Técnica:
a) pesar 4,8 gramas do meio desidratado;
b) transferir para o Erlenmeyer;
c) adicionar aos poucos 100 ml de água destilada contendo 2 ml de álcool etílico a 95%;
d) aquecer em banho-maria ou no bico de Bunsen até o início da fervura (não deixar ferver);
e) deixar esfriar;
f) distribuir 1,8 ml em cada placa.
Observação:
Preparar somente a quantidade necessária para uso. Este meio pode ser adquirido em ampolas de 2 ml, porém o custo é muito elevado. É mais econômico prepará-lo no laboratório.
Em substituição ao Caldo M FC poderá ser utilizado o meio sólido (Ágar M-Endo LES).
12 Coliformes termotolerantes:
Método da membrana filtrante:
Material necessário
a) equipamento de filtração com porta filtro;
b) placa de esterilizada de Ø 47 mm;
c) filtros de membrana de Ø 47 mm e porosidade de 0,45µm, com cartão absorvente;
d) meio de cultura (Caldo M FC);
e) água de diluição estéril;
f) pinça de aço inox;
g) copo de aço inox;
h) bico de Bunsen ou lamparina a álcool;
i) bomba de vácuo (seringa);
j) estufa bacteriológica ou banho-maria.
Preparo do meio de cultura:
Material necessário
a) meio de cultura desidratado (Caldo M FC);
b) água destilada;
c) ácido rosólico a 1% em NaOH 0,2 N;
d) frasco Erlenmeyer de 125 ml;
e) vidro de relógio;
f) bico de Bunsen ou lamparina a álcool.
Técnica:
a) pesar 3,7 gramas do meio desidratado;
b) transferir para o Erlenmeyer;
c) dissolver o meio pesado, em 100 ml de água destilada;
d) adicionar 1 ml da solução de ácido rosólico a 1%;
e) aquecer até a ebulição;
f) deixar esfriar;
g) distribuir 2,0 ml em cada placa.
Observação:
Preparar somente a quantidade necessária para uso; Este meio pode ser adquirido em ampolas de 2 ml,porém o custo é muito elevado. É mais econômico prepará-lo no laboratório; Para preparar o ácido rosólico a 1% dissolver 1 grama do ácido em 100 ml de NaOH 0,2 N; Para preparar o NaOH 0,2 N diluir 20 ml da solução 1N para 100 ml de água destilada; O ácido rosólico dura 2 semanas ou menos, quando guardado na geladeira (2 a 10ºC). Descarte-o quando a coloração mudar de vermelho-escuro para marrom; Em substituição ao Caldo M FC poderá ser utilizado o meio sólido (Ágar M FC).
13 Execução do ensaio:
a) com a pinça, colocar cuidadosamente na placa de Petri um cartão absorvente;
b) com pipeta esterilizada colocar 2,0 ml do meio de cultura no cartão absorvente e tampar a placa;
c) colocar a membrana filtrante no porta-filtro, com a pinça previamente flambada e fria;
d) agitar o frasco contendo a amostra, pelo menos 25 vezes;
e) destampar e flambar a boca do frasco;
f) verter, cuidadosamente, 100 ml de amostra no porta filtro, evitando que a água respingue sobre as bordas superiores;
g) ligar a bomba de vácuo (seringa) e fazer a sucção;
h) após filtrada a amostra, lavar 3 vezes as paredes do funil com água de diluição estéril com porções de 20 ml aplicando vácuo;
i) Após a lavagem e filtração, aliviar o vácuo e remover o funil do suporte;
j) com a pinça flambada e fria, remover o filtro do suporte e colocá-lo dentro, da placa de Petri, com o lado quadriculado para cima;
k) tampar a placa de Petri e incubá-la invertida a 44,5 ± 0,2º C durante 24 ± 2 horas;
l) após o período de incubação, examinar o filtro fazendo a contagem das colônias;
m) as colônias indicativas de Coliformes termotolerantes aparecem de cor azul. As não coliformes, aparecem com coloração clara ou rósea.
Esterilização do conjunto de filtração no campo:
a) umedecer cuidadosamente o anel de asbesto situado na base do suporte, com meia tampa de álcool metílico (tampa do frasco de álcool);
b) atear fogo;
c) colocar a cuba de aço por cima do funil quase o tampando;
d) após aquecer a cuba até o suportável pela mão, tampar o suporte;
e) esperar 15 minutos, aproximadamente e então remover a cuba e lavar o funil com água de diluição estéril a fim de remover qualquer resíduo tóxico.
Observações:
a) A combustão incompleta do metanol provoca a formação de aldeído fórmico que é o agente esterilizante;
b) O suporte do filtro deve estar estéril no início de cada série de filtração e essa série não deve ultrapassar mais de 30 amostras. A cada série de filtração efetuar o exame de 100 ml da água de diluição para controle da esterilidade do porta-filtro;
c) Os meios de cultura preparados para uso com membrana filtrante valem por 96 horas quando guardados em refrigerador com temperatura entre 2 a 10º C;
d) O conjunto de filtração também pode ser esterilizado em autoclave.
14 Colimetria total e Escherichia coli:
Método do substrato cromogênico:
Material necessário:
a) recipiente de coleta de vidro ou de plástico;
b) substrato Cromogênico;
c) estufa bacteriológica;
d) lâmpada ultravioleta de 365 nm.
Execução do ensaio:
a) coletar a amostra em um frasco estéril ou saco de coleta contendo tiossulfato de sódio a 10% para água tratada;
b) no próprio frasco ou saco adicionar o conteúdo de 1 (um) frasconete contendo o substrato cromogênico; 0 0,5º C durante 24 horas.
c) fechar o frasco ou o saco e agitar levemente, não precisa dissolver totalmente, essa dissolução ocorrerá normalmente;
d) incubar a 35,0 0,5º C durante 24 horas.
Interpretação e expressão dos resultados:
Decorridos 24 horas de incubação, retirar da estufa o material: ao observar a cor amarela, o resultado é presença de Coliformes Totais na amostra.
Com o auxílio de uma lâmpada ultravioleta 365 nm, observar se existe fluorescência azul no frasco amarelo aproximando a lâmpada do frasco. Caso isso aconteça, significa que há presença de Escherichia coli na amostra examinada. Caso a amostra permaneça transparente, o resultado é negativo, tanto para Coliformes Totais como para E. coli. Expressar o resultado como: Presença ou Ausência de Coliformes Totais ou Escherichia coli.
Nota:
A fluorescência azul ocorre somente na presença da luz ultravioleta, ao tirar o frasco da frente da luz ele volta a ficar amarelo.
Esterilização:
Os seguintes materiais devem ser esterilizados: frascos de coleta de amostra, pipetas, placas de Petri de vidro, frascos e tubos com água de diluição e meios de cultura.
Procedimentos para a esterilização:
a) preparar todo o material;
b) verificar o nível da água dentro da autoclave está acima das resistências. Completar se necessário;
c) colocar todo o material dentro do depósito metálico e tampar a autoclave;
d) apertar as travas da tampa duas a duas para não permitir saída de vapor pela borda do aparelho. Ligar o aparelho na tomada;
e) ligar a chave seletora de temperatura na posição “Máximo”;
f) abrir imediatamente a válvula de escape de vapor;
g) quando começar sair vapor por esta válvula, esperar três minutos e fechá-la;
h) neste instante, o ponteiro do manômetro começará a subir;
i) quando o ponteiro atingir a marca de 1Kg/cm² de pressão, a temperatura deverá estar em 121ºC. Deixar nesta posição durante 15 minutos;
j) se a pressão continuar subindo, coloque a chave seletora de temperatura da autoclave, na posição média“ e fique observando;
k) depois de 15 minutos, o material já estará esterilizado;
Observação:
Normalmente as autoclaves possuem uma chave seletora de temperatura que indica três posições “Mínima, Média e Máxima”, justamente para manter a pressão e temperatura dentro da faixa utilizada. Serve, também, para ligar e desligar o aparelho.
Desligar o aparelho e esperar que o ponteiro do manômetro atinja a posição “0”. Este procedimento poderá ser acelerado abrindo-se lentamente a válvula de escape de vapor;
Atenção:
Não abrir esta válvula de uma vez. Quando o ponteiro do manômetro atingir a posição “zero” e não estiver mais saindo vapor pela válvula, abrir a tampa do aparelho e retirar o material.
Nota:
Existem vários modelos de autoclaves no mercado. É importante seguir sempre as instruções do fabricante.
15 Análises físico-química da água:
Alcalinidade total:
A alcalinidade total de uma água é dada pelo somatório das diferentes formas de alcalinidade existentes, ou seja, é a concentração de hidróxidos, carbonatos e bicarbonatos, expressa em termos de Carbonato de Cálcio. Pode-se dizer que a alcalinidade mede a capacidade da água em neutralizar os ácidos. A medida da alcalinidade é de fundamental importância durante o processo de tratamento de água, pois, é em função do seu teor que se estabelece a dosagem dos produtos químicos utilizados. Normalmente as águas superficiais possuem alcalinidade natural em concentração suficiente para reagir com o sulfato de alumínio nos processos de tratamento. Quando a alcalinidade é muito baixa ou inexistente há a necessidade de se provocar uma alcalinidade artificial com aplicação de substâncias alcalinas tal como cal hidratada ou Barrilha (carbonato de sódio) para que o objetivo seja alcançado. Quando a alcalinidade é muito elevada, procede-se ao contrário, acidificando-se a água até que se obtenha um teor de alcalinidade suficiente para reagir com o sulfato de alumínio ou outro produto utilizado no tratamento da água.
Titulação com Ácido Sulfúrico:
Material necessário:
a) pipeta volumétrica de 50 ml;
b) frasco Erlenmeyer de 250 ml;
c) bureta de 50 ml;
d) fenolftaleína;
e) indicador metilorange;
f) mistura Indicadora de Verde de Bromocresol/Vermelho de Metila;
g) solução de Ácido Sulfúrico 0,02 N;
h) solução de Tiossulfato de Sódio 0,1 N.
Técnica:
a) tomar 50 ml da amostra e colocar no Erlenmeyer;
b) adicionar 3 gotas da solução indicadora de verde de bromocresol/vermelho de metila;
c) titular com a Solução de Ácido Sulfúrico 0,02 N até a mudança da cor azul-esverdeada para róseo;
d) anotar o volume total de H2 SO4 gasto (V) em ml.
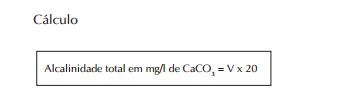
Notas:
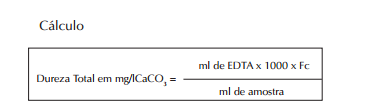
Usar 0,05 ml (1 gota) da solução de Tiossulfato de Sódio 0,1 N, caso a amostra apresente cloro residual livre; Utilizar esta técnica na ausência de alcalinidade à fenolftaleina; Caso haja alcalinidade à Fenolftaleina, adicionar, antes da mistura indicadora de verde de bromocresol/ vermelho de metila 3 gotas de Fenolftaleina e titule com H2 SO4 0,02N até desaparecer a cor rósea.formada. Em seguida continuar no passo b da técnica A alcalinidade à Fenolftaleína só poderá ocorrer se o pH da amostra for maior que 8,2; Na impossibilidade de conseguir a mistura indicadora de verde de bromocresol/vermelho de metila, usar o indicador de metilorange. Nesse caso o ponto de viragem no passo 3 da técnica será de amarelo para alaranjado; O ponto de viragem quando se usa o indicador verde de bromocresol/vermelho de metila é mais nítido do que quando se usa metilorange; A fórmula acima é para ser utilizada quando se usa uma amostra de 50 ml. Quando for usado 100 ml de amostra, o volume (V) passará a ser multiplicado por 10; Fc – Fator de correção da solução titulante.
Fluxograma da análise:
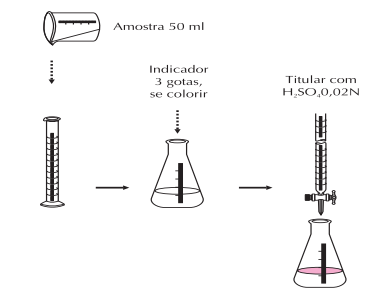
Gás carbônico livre:
O gás carbônico livre existente em águas superficiais normalmente está em concentração menor do que 10 mg/L, enquanto que em águas subterrâneas pode existir em maior concentração.
O gás carbônico contido na água pode contribuir significativamente para a corrosão das estruturas metálicas e de materiais à base de cimento (tubos de fibro-cimento) de um sistema de abastecimento de água e por essa razão o seu teor deve ser conhecido e controlado.
16 Gás carbônico livre:
Método de determinação:
Titulação com Hidróxido de Sódio
Material necessário:
a) bureta de 50 ml;
b) frasco Erlenmeyer de 250 ml;
c) pipeta volumétrica de 100 ml;
d) rolha de borracha;
e) hidróxido de Sódio 0,02N;
f) fenolftaleina.
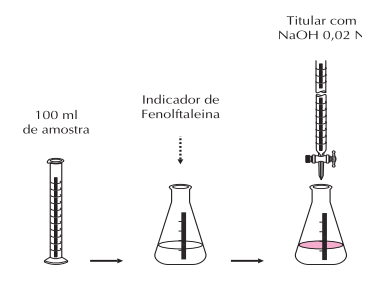
Técnica:
a) tomar 100 ml de amostra (sem agitar) em um Erlenmeyer;
b) adicionar 10 gotas de fenolftaleina, se colorir, não contém CO2 , se não colorir, prosseguir;
c) titular com a solução de Hidróxido de Sódio (NaOH) 0,02 N gota a gota até o aparecimento de leve coloração rósea persistente por pelo menos 30 segundos;
d) anotar o volume (ml) de NaOH gasto ( V ).


Fluxograma da análise de CO2:
17 Cloretos:
Geralmente os cloretos estão presentes em águas brutas e tratadas em concentrações que podem variar de pequenos traços até centenas de mg/l. Estão presentes na forma de cloretos de sódio, cálcio e magnésio. A água do mar possui concentração elevada de cloretos que está em torno de 26.000 mg/l. Concentrações altas de cloretos podem restringir o uso da água em razão do sabor que eles conferem e pelo efeito laxativo que eles podem provocar. A portaria nº 518/2004 do Ministério da Saúde estabelece o teor de 250 mg/l como o valor máximo permitido para água potável. Os métodos convencionais de tratamento de água não removem cloretos. A sua remoção pode ser feita por desmineralização (deionização) ou evaporação.
Método de determinação:
Titulação com nitrato de prata.
Material necessário:
a) bureta de 50 ml;
b) becker de 250 ml;
c) frasco Erlenmeyer de 250 ml;
d) medidor de pH;
e) proveta de 100 ml;
f) solução Padrão de Nitrato de Prata 0,0141N;
g) solução Indicadora de Cromato de Potássio K2 CrO4 2 C.
h) hidróxido de Sódio 1N;
i) ácido Sulfúrico 1N;
j) cloreto de Sódio 0,0141 N.
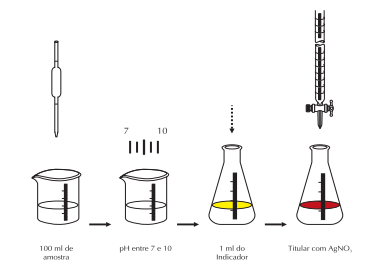
Técnica:
a) colocar 100 ml de amostra no Erlenmeyer;
b) ajustar o pH entre 7 e 10, se necessário, com NaOH ou H2 aOH H ) a
c) adicionar 1 ml da solução indicadora de K2 CrO4;
d) titular com a Solução Padrão de Nitrato de Prata 0,0141 N até a viragem para amarelo avermelhado que é o ponto final da titulação;
e) fazer um branco da mesma maneira que a amostra.

Fluxograma da análise de cloretos:
Dureza total:
A dureza total é calculada como sendo a soma das concentrações de íons cálcio e magnésio na água, expressos como carbonato de cálcio. A dureza de uma água pode ser temporária ou permanente. A dureza temporária, também chamada de dureza de carbonatos, é causada pela presença de bicarbonatos de cálcio e magnésio. Esse tipo de dureza resiste à ação dos sabões e provoca incrustações. É denominada de temporária porque os bicarbonatos, pela ação do calor, se decompõem em gás carbônico, água e carbonatos insolúveis que se precipitam. A dureza permanente, também chamada de dureza de não carbonatos, é devida à presença de sulfatos, cloretos e nitratos de cálcio e magnésio, resiste também à ação dos sabões, mas não produz incrustações por serem seus sais muito solúveis na água. Não se decompõe pela ação do calor. A portaria nº 518/2004 do Ministério da Saúde estabelece para dureza o teor de 500 mg/L em termos de CaCO3 como o valor máximo permitido para água potável.
Método de determinação:
Titulação com EDTA
Material necessário:
a) bureta de 50 ml;
b) pipeta volumétrica de 25 ml;
c) balão volumétrico de 50 ml;
d) beaker de 100 ml;
e) frasco erlenmeyer de 250 ml;
f) solução padrão de EDTA 0,01 M;
g) solução tampão;
h) indicador eriochrome Black T; inibidor I - cianeto de sódio P.A em pó; inibidor II - sulfeto de sódio.
18 Cloretos II:
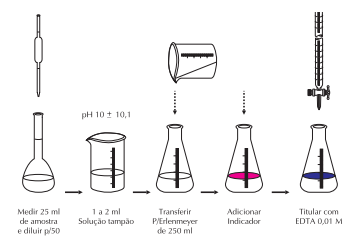
Técnica:
a) tomar 25 ml da amostra e diluir para 50 ml com água destilada em balão volumétrico;
b) transferir para um becker de 100 mL e adicionar 1 a 2 ml da solução tampão para elevar o pH a 10 ± 0,1;
c) transferir para um frasco Erlenmeyer de 250 ml e adicionar aproximadamente 0,05 gramas do Indicador Eriochrome Black T;
d) titular com EDTA 0,01M agitando continuamente até o desaparecimento da cor púrpura avermelhada e o aparecimento da cor azul (final da titulação);
e) anotar o volume de EDTA gasto (ml);
f) fazer um branco com água destilada;
g) subtrair o volume de EDTA gasto na titulação do branco do volume de EDTA gasto na titulação da amostra. A diferença é o volume que será aplicado no cálculo abaixo.
Notas:
1. A ausência de um ponto de viragem definido, geralmente, indica a necessidade de adição de um inibidor ou que o indicador está deteriorado;
2. Não leve mais do que 5 minutos para a titulação, medido após a adição da solução tampão;
3. Caso a dureza da água seja muito baixa, use amostra maior, 50 a 250 ml adicionando proporcionalmente maior quantidade de solução tampão, do inibidor e indicador;
4. Se precisar usar o inibidor adicionar 20 gotas do inibidor II;
5. Fc = Fator de correção do EDTA quando houver e for diferente de 1.
Fluxograma da análise:
PH:
O termo pH representa a concentração de íons hidrogênio em uma solução. Na água, este fator é de excepcional importância, principalmente nos processos de tratamento. Na rotina dos laboratórios das estações de tratamento ele é medido e ajustado sempre que necessário para melhorar o processo de coagulação/floculação da água e também o controle da desinfecção. O valor do pH varia de 0 a 14. Abaixo de 7 a água é considerada ácida e acima de 7, alcalina. Água com pH 7 é neutra.
A Portaria nº 518/2004 do Ministério da Saúde recomenda que o pH da água seja mantido na faixa de 6,0 a 9,5 no sistema de distribuição. Existem no mercado vários aparelhos para determinação do pH. São denominados de potenciômetros ou colorímetros. Neste manual, descreve-se o funcionamento básico de um potenciômetro, embora as instruções dos fabricantes devam ser seguidas.
Material necessário:
a) potenciômetro;
b) cubetas;
c) frasco lavador;
d) papel absorvente;
e) soluções tampão de pH conhecido;
Técnica:
a) ligar o aparelho e esperar a sua estabilização;
b) lavar os eletrodos com água destilada e enxugá-los com papel absorvente;
c) calibrar o aparelho com as soluções padrão (pH 4 - 7 ou 9);
d) lavar novamente os eletrodos com água destilada e enxugá-los;
e) introduzir os eletrodos na amostra a ser examinada e fazer a leitura;
f) lavar novamente e deixá-los imersos em água destilada;
g) desligar o aparelho.
19 Fluxograma do teste:
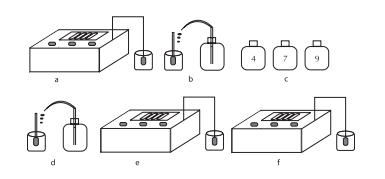
Cloro residual livre:
O cloro é um produto químico utilizado na desinfecção da água. Sua medida é importante e serve para controlar a dosagem que está sendo aplicada e também para acompanhar sua evolução durante o tratamento.
A portaria nº 518/2004 do Ministério da Saúde determina a obrigatoriedade de se manter em qualquer ponto na rede de distribuição a concentração mínima de cloro residual livre de 0,2 mg/l. Recomenda, ainda, que o teor máximo seja de 2,0 mg/l de cloro residual livre em qualquer ponto do sistema de abastecimento.
Os principais produtos utilizados são: hipoclorito de cálcio, cal clorada, hipoclorito de sódio e cloro gasoso.
Método de determinação
Comparação visual
Material necessário:
a) comparador colorimétrico;
b) cubetas de vidro ou de acrílico;
c) DPD para cloro livre em cápsula;
Técnica:
a) Encher a cubeta com água da amostra até a marca de 5,0 ml;
b) Colocá-la na abertura do lado esquerdo do aparelho;
c) Encher outra cubeta até a marca de 5,0 ml com a amostra a ser testada;
d) Adicionar uma cápsula do reagente DPD na segunda amostra e misturar;
e) Colocar a cubeta no compartimento no aparelho;
f) Antes de 1 minuto fazer a leitura do teor de cloro.
Notas:
Quando fizer a leitura posicionar o comparador (equipamento) contra uma fonte de luz como, por exemplo, uma janela, o céu ou uma lâmpada. Rotacione o disco até que se obtenha a mesma tonalidade nos dois tubos.
Resultado:
O resultado é expresso em mg/l de Cloro Residual Livre.
Observação:
Existem no mercado vários tipos de comparadores colorimétricos para medir o cloro residual, tanto com o uso de ortotolidina quanto o DPD. O uso da ortotolidina está sendo evitado por tratar-se de substância cancerígena e não recomendado pelo Standard Methods.
Cor:
A cor da água é proveniente da matéria orgânica como, por exemplo, substâncias húmicas, taninos e também por metais como o ferro e o manganês e resíduos industriais fortemente coloridos. A cor, em sistemas públicos de abastecimento de água, é esteticamente indesejável. A sua medida é de fundamental importância, visto que, água de cor elevada provoca a sua rejeição por parte do consumidor e o leva a procurar outras fontes de suprimento muitas vezes inseguras. A Portaria nº 518/2004 do Ministério da Saúde estabelece para cor aparente o Valor Máximo Permitido de 15 (quinze) uH como padrão de aceitação para consumo humano.
Método de determinação:
Comparação visual
Material necessário
a) tubos de Nessler forma alta de 50 ml;
b) suporte de madeira;
c) solução-Padrão de Cloroplatinato de Potássio (500 Unidades de Cor);
Técnica:
a) preparar Padrões de Cor na faixa de 5 a 50 unidades de cor, medindo 0,5; 1,0; 1,5; 2,0; 2,5; 3,0; 3,5; 4,0; 4,5; 5,0; 6,0 e 7,0 ml da solução padrão (500 Unidades de Cor) e colocar em tubos de Nessler de 50 ml;
b) diluir com água destilada até a marca de 50 ml;
c) medir 50 ml da amostra em outro tubo de Nessler e comparar com os padrões.
Resultado:
O resultado é expresso em Unidades de Cor ou unidade Hazen (uH). Notas: A comparação deverá ser feita olhando os tubos verticalmente contra um fundo branco; Proteger os Padrões contra evaporação e poeira; Quando a cor da amostra for maior do que 70 unidades, fazer diluição até que se obtenha resultado dentro da faixa coberta pelos padrões. Neste caso, o resultado deve ser multiplicado pelo fator de diluição uH é a unidade de escala de Hazen (platinacobalto).
20 Fluxograma do teste II:
Resultado:
O resultado é expresso em Unidades de Cor ou unidade Hazen (uH).
Notas:
1. A comparação deverá ser feita olhando os tubos verticalmente contra um fundo branco;
2. Proteger os Padrões contra evaporação e poeira;
3. Quando a cor da amostra for maior do que 70 unidades, fazer diluição até que se obtenha resultado dentro da faixa coberta pelos padrões. Neste caso, o resultado deve ser multiplicado pelo fator de diluição;
4.uH é a unidade de escala de Hazen (platinacobalto).
21 Alumínio:
O teste de alumínio é indicado para estações de tratamento onde o sulfato de alumínio é usado como coagulante. A dosagem incorreta desse coagulante é denotada pela quantidade significativa de alumínio que persiste na água tratada.
O hidróxido de alumínio – Al(OH)3 - formado na reação é anfótero. Sua ionização se processa em pH ácido ou básico, segundo as equações:
Em pH ácido:
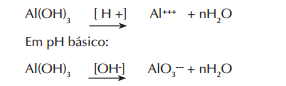
Nas duas formas ele pode se solubilizar e atravessar os decantadores e filtros. A solubilização acontece com a correção do pH. Quando o pH ótimo de floculação não está correto, o teor de alumínio da água tratada aumenta. A Portaria nº 518/2004 do Ministério da Saúde estabelece que o padrão de aceitação para consumo humano é de 0,2 mg/l.
Método de determinação:
A determinação do alumínio pode ser feita através dos métodos de Absorção Atômica, Eriocromo Cianina – R utilizando um fotômetro de filtro ou espectrofotômetro e também pelo método de Comparação Visual, utilizando-se tubos de Nessler. Neste manual, descreveremos o método de Comparação Visual, considerando que a maioria dos laboratórios dos serviços de abastecimento de água nem sempre possuem equipamentos como Espectrofotômetro de Absorção Atômica ou outro.
Material necessário:
a) tubo de Nessler forma alta, de 50 ml;
b) pipeta graduada de 1 ml;
c) pipeta graduada de 5 ml;
d) pipeta graduada de 10 ml;
e) suporte para tubos de Nessler.
Reagentes:
a) ácido sulfúrico 0,02N;
b) reagente tampão de acetato de sódio;
c) eriocromo cianina-R - (corante);
d) solução de trabalho do corante.
Técnica:
a) medir 25 ml de amostra ou uma porção diluída para 25 ml em um frasco Erlenmeyer de 125 ml;
b) adicionar 3 gotas de metilorange e titular com ácido sulfúrico (H2SO4) 0,02N até ligeira coloração rosa pálido;
c) anotar o volume gasto de ácido e descartar a amostra;
d) medir novamente 25 ml de amostra ou uma alíquota diluída a 25 ml e transferir para um tubo de Nessler de 50 ml;
e) adicionar à amostra o mesmo volume de ácido sulfúrico gasto no passo 2, acrescentando 1 ml em excesso;
f) adicionar 1,0 ml de ácido ascórbico e misturar;
g) adicionar 10,0 ml do reagente tampão e misturar;
h) adicionar 5,0 ml da solução de trabalho do corante e misturar;
i) imediatamente, diluir até a marca de 50 ml, com água destilada;
j) misturar e deixar em repouso por 5 a 10 minutos e comparar a cor desenvolvida pela amostra com os padrões preparados da mesma maneira e na mesma hora.
Resultado:
O resultado é expresso em mg/l de alumínio.
Observação:
Neste método não é necessário preparar o branco da amostra e ele também não é recomendado para amostras que contém cor e turbidez porque pode levar a erros consideráveis.
22 Alumínio II:
Preparo dos Padrões.
Material necessário:
a) tubo de nessler forma alta, de 50 ml;
b) pipeta graduada de 1 ml;
c) pipeta graduada de 5 ml;
d) pipeta graduada de 10 ml;
e) suporte para tubos de Nessler.
Reagentes:
a) ácido sulfúrico 0,02N;
b) reagente tampão de acetato de sódio;
c) eriocromo cianina-R - (corante);
d) solução de trabalho do corante;
e) solução padrão de alumínio (1 ml = 5 µg Al).
Técnica:
Preparar os padrões na faixa de 0 a 0,5 mg/l, pipetando: 0,0 – 0,5 – 1,0 – 1,5 – 2,0 e 2,5 ml da solução padrão (1 ml = 5 µg) e diluindo para 25 ml com água destilada em tubos de nessler (ver quadro abaixo).
Tratar esses padrões do seguinte modo:
a) adicionar 1,0 ml de ácido sulfúrico 0,02N e misturar;
b) adicionar 1,0 ml de ácido ascórbico e misturar;
c) adicionar 10 ml do reagente tampão e misturar;
d) adicionar 5 ml da solução de trabalho do corante e misturar;
e) levar o volume para 50 ml com água destilada e misturar;
f) deixar em repouso por 5 a 10 minutos.
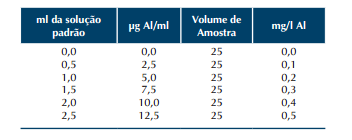
Notas:
1. Para o padrão 0,0 mg/l, tomar 25 ml de água destilada e proceder igual aos outros;
2. Preparar os padrões toda vez que for examinar a amostra;
3. Caso o laboratório possua espectrofotômetro, fazer a leitura dos padrões a 535 nm e traçar a curva de calibração em papel semi-logaritmo (% de transmitância x concentração). Nesse caso, não é necessária a preparação de todos os padrões quando examinar a amostra. Fazer apenas um ou dois para checar a curva de calibração do aparelho.
23 Turbidez:
A turbidez da água é devida à presença de materiais sólidos em suspensão, que reduzem a sua transparência. Pode ser provocada também pela presença de algas, plâncton, matéria orgânica e muitas outras substâncias como o zinco, ferro, manganês e areia, resultantes do processo natural de erosão ou de despejos domésticos e industriais.
A turbidez tem sua importância no processo de tratamento da água. Água com turbidez elevada e dependendo de sua natureza, forma flocos pesados que decantam mais rapidamente do que água com baixa turbidez. Também tem suas desvantagens como no caso da desinfecção que pode ser dificultada pela proteção que pode dar aos microrganismos no contato direto com os desinfetantes. É um indicador sanitário e padrão de aceitação da água de consumo humano.
A Portaria nº 518/2004 do Ministério da Saúde estabelece que o Valor Máximo Permitido é de 1,0 uT para água subterrânea desinfectada e água filtrada após tratamento completo ou filtração direta, e 5,0 uT como padrão de aceitação para consumo humano. Para água resultante de filtração lenta o Valor Máximo Permitido é 2,0 uT.
Existem equipamentos específicos para determinação da turbidez na água. Neste manual, apresenta-se a técnica de determinação da turbidez utilizando a metodologia nefelometrica.
Método Nefelométrico:
Material necessário:
a) turbidímetro com nefelômetro;
b) células de amostras de vidro incolor (quartzo),
c) balão volumétrico de 100 ml;
d) pipeta volumétrica de 5 ml;
e) conjunto de filtração;
f) filtros de membrana de 0,2 µm.
Reagentes:
a) Água isenta de turbidez: passar água destilada através de um filtro de membrana de 0,02 µm de porosidade. Enxaguar o frasco de coleta pelo menos duas vezes com água filtrada e desprezar os primeiros 200 ml;
b) Suspensão estoque de turbidez – padrão primário.
Solução I:
- Dissolver 1,0 g de Sulfato de Hidrazina (NH2 ).H2 SO4 em água destilada e diluir a 100 ml em balão volumétrico;
Advertência:
Sulfato de Hidrazina é carcinogênico. Evitar inalação, ingestão e contato com a pele.
Solução II:
- Dissolver 10,0 gramas de Hexametilenotetramina (CH2 a ( em água destilada e diluir a 100 mL em balão volumétrico;
- Mistura 5,0 ml da solução I e 5,0 ml da solução II. Deixar em repouso por 24 horas a 25 ± 3º C. A turbidez desta suspensão é de 4000 UTN. Transferir a solução estoque para um frasco de cor âmbar ou outro frasco protegido da luz ultravioleta, para armazenagem. Fazer diluição desta suspensão estoque. A suspensão estoque é estável por um ano quando corretamente armazenada;
c) Suspensão padrão de turbidez:
- Diluir 1, 0 ml da solução estoque para 100 ml com água isenta de turbidez. A turbidez desta suspensão é de 40 UTN. Preparar diariamente
d) Padrões de turbidez diluídos:
- Diluir porções da suspensão padrão de turbidez com água livre de turbidez de acordo com a faixa de interesse. Preparar diariamente.
Procedimento:
a) Calibrar o turbidímetro de acordo com as instruções do fabricante;
b) Medida de turbidez menor que 40 UTN: Agitar a amostra suavemente e esperar até que as bolhas de ar desapareçam e colocá-la na célula de amostra do turbidímetro; Fazer a leitura da turbidez diretamente na escala do instrumento ou na curva de calibração apropriada.
c) Medida de turbidez acima de 40 UTN: Diluir a amostra com um ou mais volumes de água isenta de turbidez até que a turbidez da amostra diluída fique entre 30 e 40 NTU. Fazer a leitura e multiplicar o resultado pelo fator de diluição.

24 Temperatura:
A temperatura está relacionada com o aumento do consumo de água, com a fluoretação, com a solubilidade e ionização das substâncias coagulantes, com a mudança do pH, com a desinfecção, etc.
Procedimento para determinação na água.
Material necessário:
a) termômetro;
b) becker de 250 ml.
Técnica:
a) coletar um pouco de água em um becker de 250 ml;
b) mergulhar o termômetro na água;
c) esperar até que o material dilatante (mercúrio) se estabilize;
d) fazer a leitura com o bulbo do termômetro ainda dentro da água.
25 Fluoretos:
A aplicação de flúor na água para consumo humano tem a finalidade de prevenir a cárie dental. Hoje, esse procedimento é considerado um processo normal de tratamento de água e o teor ótimo de flúor é parte essencial de sua qualidade. Em razão disso e outros fatores, é que o seu controle se faz necessário na estação de tratamento de água. Existem vários métodos para determinação de flúor na água. Os três mais conhecidos são: O método Spadns, o Scott-Sanchis e o método do eletrodo específico para íons fluoretos. Neste manual, descreve-se apenas o método Scott-Sanchis, que embora não seja o que dá maior grau de exatidão, atende às expectativas e é o de custo mais barato. É um método de comparação visual de cor feito em tubos de Nessler.
Método Scott-Sanchis:
Material necessário
a) tubo de Nessler de 100 ml;
b) suporte para tubo de Nessler;
c) termômetro;
d) pipeta volumétrica de 5 ml;
e) pipeta graduada de 10 ml.
Reagentes:
a) solução padrão de fluoretos (1ml = 10 µgF-);
b) reagente Scott-Sanchis;
c) arsenito de sódio (0,5%).
Preparo dos padrões e da amostra:
a) tomar 7 tubos de Nessler de 100 ml;
b) encher o 1º tubo com água destilada (branco);
c) pipetar no 2º tubo 2 ml da solução padrão,
d) pipetar no 3º tubo 4 ml da solução padrão,
e) pipetar no 4º tubo 6 ml da solução padrão,
f) pipetar no 5º tubo 8 ml da solução padrão,
g) pipetar no 6º tubo 10 ml da solução padrão,
h) encher o 7º tubo com 100 ml de amostra ou uma alíquota diluída a 100 ml. Caso haja cloro na amostra, removê-lo pela adição de 0,1ml (2 gotas) da solução de arsenito de sódio para cada mg/l de cloro;
i) diluir os padrões de 2 a 6 a 100 ml com água destilada;
j) ajustar a temperatura dos padrões e da amostra;
k) adicionar a cada tubo, inclusive no branco (1º tubo) 5 ml do reagente Scott-Sanchis;
l) misturar e deixar em repouso por uma hora;
m) decorrido uma hora da adição do reagente ScottSanchis, comparar a amostra com os padrões e expressar o resultado em mg/l F-.
Exemplo:
Se a coloração desenvolvida pela amostra for semelhante ao padrão do tubo nº 5 essa amostra terá 0,8 mg/l de íon fluoreto. Caso a amostra desenvolva uma coloração que se situe entre dois padrões poderá ser feita a interpolação dos resultados. Ex.: leitura entre 0,6 e 0,8 expressar como 0,7 mg/l.
26 Fluoretos II:
Fluxograma do teste:
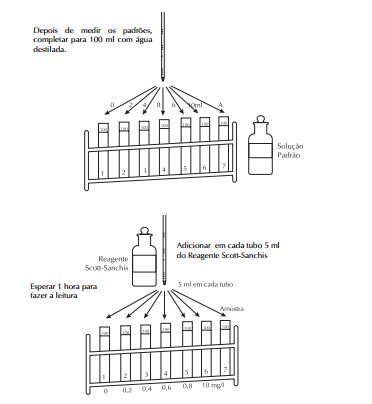
Notas:
1. A concentração dos padrões preparados (tubos de 2 a 6) correspondem a 0,2 – 0,4 – 0,6 – 0,8 – 1,0 mg/l de íon fluoreto, respectivamente;
2. Poderão ser analisadas várias amostras simultaneamente com os padrões;
3. Caso haja interferentes nas amostras em concentrações que possam alterar os resultados, essas amostras deverão ser destiladas;
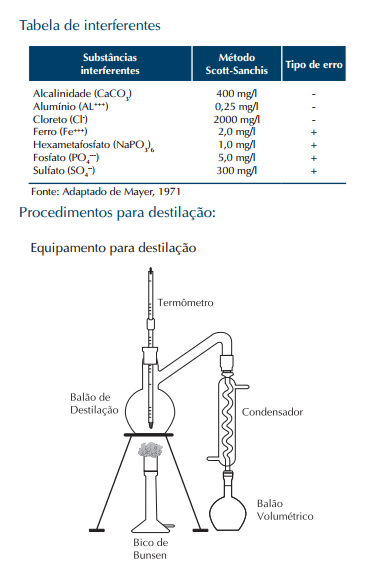
Fazer primeiro uma destilação preliminar para remover qualquer contaminação de fluoreto e ajustar a reação ácido/água para as destilações subsequentes, do seguinte modo:
a) colocar 400 ml de água destilada no balão de destilação;
b) adicionar lentamente e com agitação 200 ml de ácido sulfúrico concentrado (H2 SO4 );
c) adicionar algumas pérolas de vidro;
d) conectar o balão ao condensador e começar a destilação;
e) quando a temperatura atingir 180º C, parar a destilação e eliminar o destilado. O conjunto está pronto para a destilação da amostra.
Destilação da amostra:
Adicionar à mistura de ácido que sobrou da destilação preliminar 300 ml de amostra, misturar cuidadosamente e destilar como anteriormente, até que a temperatura atinja 180º C. Nesse momento o destilado será igual a 300 ml.
Notas:
1. Não deixar que a temperatura ultrapasse 180º C, assim se evita que haja arraste de sulfato para o destilado.
2. Quando amostras de alto conteúdo de cloretos são analisadas, adicionar ao balão de destilação 5 mg de sulfato de prata para cada mg de cloreto presente na amostra.
3. Usar a solução de ácido sulfúrico várias vezes até que os contaminantes das amostras de água acumulados no frasco de destilação, comecem a interferir no destilado. Quando isso acontecer, o melhor é desprezar o ácido e começar tudo novamente.
Importante:
A dosagem de flúor na água para consumo humano é estabelecida em função da média das temperaturas máximas diárias da localidade observadas durante um determinado período. A Portaria nº 518/2004 do Ministério da Saúde estabelece como Valor Máximo Permitido 1,5 mg/l de íon fluoreto.
Coleta e preservação de amostras para análise físico-químicas deste manual:
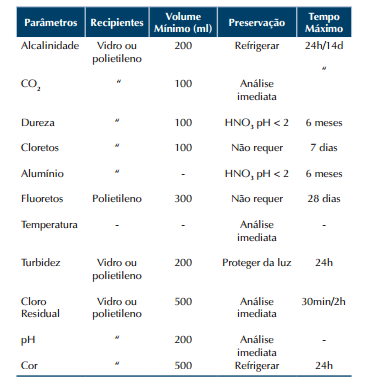
Notas:
1. Os volumes aqui descritos são estimados. Na prática, deve-se coletar o volume necessário para realização das análises, até porque existem repetições de análises muitas vezes necessárias.
2. Quando preservar com ácido nítrico, usar 2 ml do ácido para cada litro de amostra.
3. Normalmente, nas ETAs, as análises devem ser efetuadas imediatamente após a coleta. Não é de boa prática deixar as amostras por muito tempo para serem analisadas.
27 Ensaio de coagulação (Jar-test):
O ensaio de coagulação é um procedimento de rotina em estações de tratamento de água para determinar a dosagem dos produtos químicos utilizados no tratamento. Podemos dizer, que é uma simulação do que ocorre na ETA. Para realizar este ensaio, é necessário que se conheça previamente as seguintes características da água bruta: cor, turbidez, alcalinidade, pH e temperatura; além de parâmetros hidráulicos da estação de tratamento, tais como: vazão, tempo de detenção no floculador, velocidade de sedimentação no decantador, etc.
O ensaio de coagulação não é uma operação muito simples, pois devem ser consideradas algumas variáveis do processo, como a cor e turbidez da água bruta; se a alcalinidade natural da água é suficiente, se o pH está dentro da faixa ótima de floculação, o tipo de coagulante empregado, etc. Neste exemplo prático, vamos apenas considerar os parâmetros: cor, turbidez, pH e alcalinidade total, já que o objetivo principal do teste é a remoção da cor e turbidez da água, aplicando-se uma menor quantidade de coagulante. O produto químico utilizado é o sulfato de alumínio, sendo o mais comum.
Etapas do teste de coagulação que devem ser observados:
a) fazer análise da amostra bruta – cor, pH, turbidez e alcalinidade total, temperatura;
b) descobrir o pH ótimo de floculação;
c) verificar a menor dosagem do coagulante no pH ótimo;
d) observar a velocidade de sedimentação dos flocos;
e) analisar o sobrenadante, verificando, principalmente, a remoção de cor e turbidez.
Material necessário:
a) aparelho de Jar-test conforme o da figura;
b) becker forma baixa de 1000 ml;
c) solução de sulfato de alumínio a 1%;
d) solução de cal a 0,5%;
e) Pipetas graduadas de 5 e 10 ml.
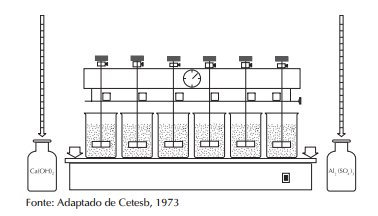
Procedimento 1:
Considerando que a água bruta tenha alcalinidade natural suficiente e tenha, também, um pH ótimo de floculação).
a) colocar 6 beckers de 1 litro na plataforma do aparelho de Jar-Test;
b) enchê-los com água bruta até a marca de 1000 ml;
c) ligar o aparelho na velocidade máxima 100 r.p.m;
d) adicionar simultaneamente nos beckers a quantidade de coagulante (sulfato de alumínio) que foi calculada para cada becker;
e) deixar agitar nessa velocidade por 2 a 3 minutos (tempo de detenção na câmara de mistura rápida);
f) reduzir a velocidade de agitação para 50 r.p.m durante 10 a 30 minutos (tempo de detenção nos floculadores);
g) deixar as amostras decantar por algum tempo(esse tempo seria o correspondente à velocidade de sedimentação no decantador – 10 a 30 minutos);
h) coletar o sobrenadante de todos os beckers e analisar os parâmetros necessários para verificar qual deles apresentou melhor resultado;
i) normalmente o melhor resultado é aquele que apresentou maior redução de cor e turbidez e essa dosagem deverá ser a escolhida.
28 Ensaio de coagulação (Jar-test) II:
Procedimento 2:
Quando a água não tem alcalinidade natural suficiente e desconhece-se o pH ótimo de floculação.
a) colocar 6 beckers de 1 litro na plataforma do aparelho de Jar-Test;
b) enchê-los com água bruta até a marca de 1000 ml;
c) ligar o aparelho na velocidade máxima 100 r.p.m;
d) estabelecer diferentes pH nos beckers usando álcali (cal hidratada);
e) aplicar uma quantidade fixa de sulfato de alumínio em todos os beckers e proceder de acordo com os passos (e) e (i) do procedimento 1;
f) medir o pH do frasco que apresentou melhor resultado;
g) executar novo ensaio, fixando em todos os beckers o pH ótimo encontrado no item anterior;
h) adicionar sulfato de alumínio em cada becker, variando a concentração em valores próximos (menor e maior) da dosagem utilizada na letra c;
i) proceder de acordo com os passos de (e) e (i) do procedimento 1.
Notas:
1. dependendo das alterações que a água bruta possa sofrer, consequência de enchentes, estiagens, alterações climáticas, etc., é recomendado sempre fazer novos testes para ajustar as dosagens dos coagulantes.
2. Quando a água bruta não tiver alcalinidade natural suficiente para reagir com o sulfato de alumínio, usar cal hidratada ou outro álcali para promover uma alcalinidade artificial.
3. Quando a água bruta não tiver um pH ótimo de floculação, criar essa condição, utilizando ácidos ou bases (álcalis).
4. O álcali mais usado é a cal hidratada.
5. Normalmente se usa sulfato de alumínio a 1% e cal a 0,5% para fazer os ensaios, pois facilita a medição de volumes utilizados no processo.
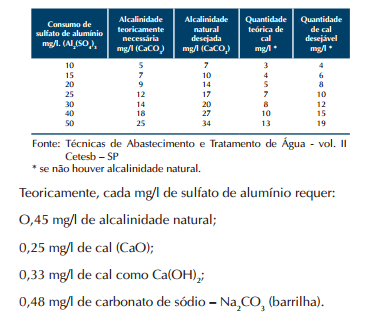
6. Para dosagens de sulfato de alumínio de 10 – 15 – 20– 25 – 30 e 35 mg/L de uma solução a 1% são necessários os seguintes volumes: 1,0 ml, 1,5 ml, 2,0 mL, 2,5 ml, 3,0 ml e 3,5 ml, respectivamente. Para dosagem de cal, usa-se metade desses volumes em ml.
7. Consultar a tabela abaixo para estabelecer a quantidade de cal necessária em função do consumo de sulfato de alumínio.
Correção do pH da água tratada:
A correção do pH da água tratada é um procedimento utilizado nas ETAs com a finalidade de prevenir o processo de corrosão das estruturas metálicas do sistema de distribuição que é provocado pela acidez da água, consequência da presença de gás carbônico dissolvido. As águas superficiais possuem gás carbônico dissolvido. Esse gás carbônico pode ser proveniente da atmosfera, da respiração dos seres aquáticos e até da reação do sulfato de alumínio quando este reage com a alcalinidade natural da água. A correção do pH significa elevar o pH da água tratada até o pH de saturação que é o ponto onde não acontece mais o processo de corrosão. Esse pH não é igual para todas as águas e sua determinação pode ser feita no laboratório.
Método de determinação:
Ensaio do mármore
Material necessário:
a) balão volumétrico de 1000 mL;
b) medidor de pH;
c) balança;
Reagente:
Carbonato de cálcio
29 Ensaio de coagulação (Jar-test) III:
Técnica:
a) colocar 750 ml de água filtrada em um balão volumétrico de 1000 ml;
b) determinar o pH e a alcalinidade (I) dessa água;
c) adicionar 10 gramas de Carbonato de cálcio ao balão;
d) agitar por ½ hora e deixar decantar e filtrar;
d) determinar o pH;
e) agitar novamente o balão por mais ½ hora;
f) deixar decantar e filtrar;
g) determinar novamente o pH.
Repetir a operação iniciada no item 6 até pH constante. O pH de saturação será o pH constante encontrado. Determinar na última operação a alcalinidade (II).
Conclusão:
Se a alcalinidade II > alcalinidade I ⇒ água corrosiva
Se a alcalinidade II=alcalinidade I ⇒ água não corrosiva
Se a alcalinidade II < alcalinidade I ⇒ água incrustante
Determinação do teor de cloro ativo em uma solução de cloro (hipoclorito de sódio e hipoclorito de cálcio):
Material necessário:
a) frasco Erlenmeyer de 250 ou 500 ml;
b) bureta de 50 ml;
c) pipeta volumétrica de 1; 5 e 10 ml;
d) balança de precisão.
Reagentes:
a) tiossulfato de sódio 0,1N (Na2S2O35H2O);
b) iodeto de potássio (KI);
c) ácido acético P.A;
d) indicador de amido.
Técnica:
a) medir 1,0 ml da solução;
b) Dissolver em 50 ml de água destilada;
c) Adicionar 5,0 ml de ácido acético concentrado (glacial);
d) Adicionar 1, 0 g de Iodeto de potássio;
e) Titular com a solução de tiossulfato de sódio 0,1 N;
f) Anotar os ml de tiossulfato gastos.

Observação:
Dependendo da concentração da solução a ser analisada usar um peso ou volume que não gaste mais do que a capacidade da bureta utilizada, de tiossulfato de sódio 0,1 N. Fazer um branco com água destilada.
30 Preparação dos reagentes para análise do Teor de Cloro ativo:
Tiossulfato de sódio 0,1 N:
Dissolver 25 gramas de tiossulfato de sódio Na2 .5H2 O em 1 litro de água destilada fervida recentemente. Armazenar durante duas semanas e padronizar com Dicromato de potássio K2 er 0,1 N.
Notas:
1. Usar água destilada fervida na preparação do tiossulfato
2. Adicionar alguns mililitros de clorofórmio (±5 ml) para minimizar a decomposição bacteriana da solução de tiossulfato.
Dicromato de potássio 0,1 N:
Pesar 4,904 gramas de dicromato de potássio (K2 ar .) e dissolver em um pouco de água destilada e em seguida diluir para 1 litro. Armazenar em frasco de vidro com tampa de vidro.
Solução indicadora de amido :
Pesar 5,0 gramas de amido. Adicionar um pouco de água destilada até formar uma pasta. Em seguida dissolver essa pasta em um litro de água destilada fervente. Deixar em repouso durante uma noite. Usar o líquido sobrenadante preservando-o pela adição de 1,25 gramas de ácido salicílico.
Padronização da solução de tiossulfato de sódio 0,1N:
Material necessário:
a) bureta de 50 ml;
b) frasco Erlenmeyer de 250 ml;
c) Pipeta graduada de 1 ml;
d) Pipeta volumétrica de 10 ml.
Procedimento:
a) colocar 80 ml de água destilada no Erlenmeyer;
b) adicionar, com agitação constante, 1 ml de H2SO4 concentrado e 10 ml de dicromato de potássio 0,1 N;
c) adicionar 1,0 grama de Iodeto de potássio;
d) deixar a mistura reagir durante 6 minutos no escuro;
e) titular com a solução de Tiossulfato de sódio até o aparecimento da coloração amarelo claro;
f) adicione 1,0 ml da solução de amido e continue a titulação até o desaparecimento da cor azul formada.

31 Preparação dos Reagentes Utilizados nas Análises Constantes neste Manual:
Reagentes para alcalinidade:
Solução de ácido sulfúrico 0,02 N
Para preparar esta solução, faz-se primeiro uma solução 0,1N do seguinte modo:
a) transferir, com pipeta, lentamente, 2,8 ml de acido sulfúrico concentrado (96% d=1,84) para um balão volumétrico de 1000 ml contendo cerca de 500 ml de água destilada;
b) completar o volume, até a marca, com água destilada e agitar;
c) desta solução, medir, com pipeta volumétrica, 200 ml e transferir para um balão volumétrico de 1000 ml e completar o volume com água destilada. Esta solução é aproximadamente 0,02 N.
Solução de carbonato de sódio 0,02 N:
Para preparar a solução de carbonato de sódio 0,02 N secar 1,5 a 2,0 gramas de Na2 Co3 grau padrão primário, a 2500 C por quatro horas. Esfriar em dessecador. Em seguida, pesar 1,060 gramas e dissolver em 250 ml de água destilada e completar o volume para 1000 ml com água destilada em balão volumétrico
.
Padronização da solução:
Colocar 50 ml de uma solução de carbonato de Sódio 0,02 N em um frasco Erlenmeyer de 250 ml e adicionar 4 gotas do indicador metilorange. Titular com H2 SO4 0,02N até a viragem do indicador para leve coloração avermelhada. Anotar o volume do ácido gasto.
Para calcular a normalidade correta, use a seguinte fórmula:

Solução de tiossulfato de sódio 0,1 N:
Pesar exatamente 25,0 gramas de Na2 .5H2 O e dissolver em um pouco de água destilada e completar o volume para 1000 ml em balão volumétrico.
Indicador metilorange:
Pesar 0,100 gramas de metilorange e dissolver em 200 ml de água destilada.
Fenolftaleina:
a) dissolver 1 grama de fenolftaleína em um pouco de água destilada e diluir a 200 ml.
b) adicionar gotas de NaOH 0,02 N até o aparecimento de leve coloração cor-de-rosa.
Mistura indicadora de verde de bromocresol/ vermelho de metila:
Pesar 20 mg de vermelho de metila e 100 mg e verde de bromocresol e dissolver em 100 ml de água destilada ou álcool etílico a 95%.
Reagentes para CO2:
Hidróxido de sódio 0,02 N
a) Para preparar esta solução, faz-se primeiro uma solução 0,1N do seguinte modo;
b) Pesar rapidamente 4,2 gramas de Hidróxido de sódio em lentilhas e transferir para um becker de 500 ml e dissolver em água destilada isenta de gás carbônico;
c) Transferir esta solução para um balão volumétrico de 1 litro e completar o volume até a marca. Esta solução é aproximadamente 0,1 Normal.
Padronizar com uma solução de Ácido Sulfúrico 0,1 normal do seguinte modo:
a) Tomar 100 ml de água destilada em um frasco Erlenmeyer de 250 ml;
b) Medir, com pipeta volumétrica ou bureta 10 ml da Solução de NaOH 0,1 Normal e transferir para o Erlenmeyer acima;
c) Juntar 3 a 4 gotas do Indicador de Metilorange;
d) Titular com a Solução de Äcido Sulfúrico 0,1 Normal e) Anotar os ml de H2 aOH gastos que devem ser 10 ou próximo de 10.
Se o volume de H2 SO4 0,1 N gastos na titulação forem maior ou menor que 10 ml, calcular o Fator de Correção (Fc) da solução de NaOH utilizando a seguinte fórmula:
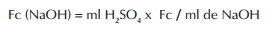
Anotar o Fc no rótulo do frasco. Preparação da solução de hidróxido de sódio N/50:
a) Transferir 200 ml da solução estoque de NaOH 0,1 N para um balão volumétrico de 1 litro e completar com água destilada. Esta nova solução é aproximadamente N/50 (0,02 N).
32 Preparação dos Reagentes Utilizados nas Análises Constantes neste Manual II:
Padronização da solução de NaOH 0,02 N:
a) Tomar 100 ml de água destilada em um frasco Erlenmeyer de 250 ml;
b) Medir, com pipeta volumétrica ou bureta 10 ml da Solução de NaOH 0,02 N, e transferir para o Erlenmeyer acima;
c) Juntar 3 a 4 gotas do Indicador de Metilorange;
d) Titular com a Solução de Ácido Sulfúrico 0,02 N até a viragem do indicador;
e) Anotar o volume de H2 SO4 gastos que devem ser em torno de 10 ml .
Cálculo do fator de correção do NaOH:
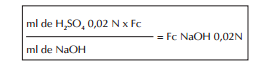
Notas:
1. A viragem do indicador não é muito fácil de se visualizar. Fazer um branco com 100 mL de água destilada para a comparação de cor no momento da viragem do indicador;
2. Ao adicionar o indicador, a solução fica amarelada e no final da titulação a solução fica levemente avermelhada;
3. Água isenta de CO2 pode ser obtida pela fervura da água destilada durante 15 minutos e resfriada rapidamente até a temperatura ambiente.
Fenolftaleina:
a) Dissolver 1 grama de fenolftaleína em um pouco de água destilada e diluir a 200 ml;
b) Adicionar gotas de NaOH 0,02N até o aparecimento de leve coloração cor-de-rosa.
Reagentes para análise de cloretos:
Solução-Padrão de Nitrato de Prata 0,0141 N
a) pesar 2,395 gramas de AgNO3 e dissolver em um pouco de água destilada. Completar para 1 litro em balão volumétrico; 1,00 ml = 500 µg Cl
b) padronizar contra uma solução de Cloreto de Sódio 0,0141N;
c) guardar a solução em frasco escuro.
Cloreto de sódio 0,0141 N:
a) dissolver 824,1 mg de Cloreto de Sódio seco a 140º C em água livre de cloretos e diluir para 1000 ml. 1,00 ml = 500 µg Cl.
Padronização da solução de nitrato de prata 0,0141 N:
a) usar 100 ml de amostra (NaCl 0,0141 N) ou uma porção diluída a 100 ml;
b) ajustar o pH entre 7 e 10 com NaOH ou H2 aOH 1 N;
c) adicionar 1 ml de K2 CrO4 (Cromato de Potássio);
d) titular com a solução de Nitrato de Prata 0,0141 N até o aparecimento da cor amarelo avermelhado;
e) anotar o volume de Nitrato de Prata gasto na titulação; f) calcular o fator de correção do AgNO3 0,0141 N usando a seguinte fórmula:

Solução indicadora de cromato de potássio (K2 CrO4 ):
a) pesar 50 gramas de K2 CrO4 e dissolver em um pouco de água destilada;
b) adicionar solução de AgNO3 0,0141 N até formar um precipitado vermelho;
c) deixar em repouso por 12 horas;
d) filtrar e completar o volume para 1000 ml com água destilada.
Hidróxido de sódio (NaOH) 1N:
a) pesar 40 gramas de Hidróxido de Sódio e dissolver em um pouco de água destilada e diluir a 1 litro;
b) guardar em frasco de polietileno ou vidro-pirex.
33 Preparação dos Reagentes Utilizados nas Análises Constantes neste Manual III:
Ácido sulfúrico (H2 SO4 ) 1N:
a) em um becker de 1000 ml colocar cerca de 500 ml de água destilada;
b) Em seguida medir 28 ml de ácido sulfúrico concentrado e adicionar lentamente no becker acima, com agitação constante;
c) Deixar esfriar;
d) Transferir para um balão volumétrico de 1000 ml e completar o volume com água destilada, homogeneizando a seguir;
e) Armazenar em frasco de polietileno ou vidro pirex.
Notas:
1. Agitar com bastão de vidro;
2. Nunca adicionar água no ácido, e sim ácido na água.
Reagentes para análise de dureza:
Solução padrão de EDTA 0,01 M
a) pesar 3,723 gramas de EDTA (sal di-sódio do ácido etilenodiamino tetraacético), dissolver em água destilada e diluir a 1000 ml;
b) padronizar contra uma solução-padrão de Carbonato de Cálcio;
c) guardar esta solução em frasco de polietileno.
Solução padrão de cálcio:
a) pesar 1,0 grama de Carbonato de Cálcio anidro (CaCO3 ) padrão primário e colocar em um frasco Erlenmeyer de 250 ml;
b) adicionar aos poucos, com auxílio de um funil HCl 1:1 até dissolver todo CaCO3
c) adicionar 200 mL de água destilada e ferver por alguns minutos para eliminar o CO2 ;
d) esfriar e adicionar algumas gotas de vermelho de metila e ajustar para a cor laranja intermediária por adição de NH4 OH 3N ou HCl 1:1;
e) transferir toda a mistura para um balão volumétrico de 1000 ml e completar o volume até a marca com água destilada (1 ml desta solução = 1,0 mg de CaCO3 ).
Padronização da solução de EDTA 0,01 M:
a) medir 25 ml da solução padrão de cálcio e diluir para 50 ml com água destilada em frasco Erlenmeyer de 125 ml
b) adicionar 1 a 2 ml da solução tampão para obter o pH em torno de 10 ± 0,1;
c) adicionar 0,05 gramas do indicador Eriochrome Black T;
d) titular com EDTA 0,01 M gota a gota até desaparecer a última coloração violácea e aparecer a cor azul indicadora do ponto final da titulação.
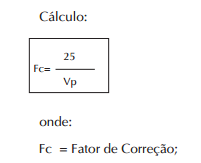
Vp = Volume de EDTA gasto na titulação.
Solução tampão para dureza:
a) pesar 16,9 gramas de Cloreto de Amônia (NH4Cl) e dissolver em 143 ml de Hidróxido de Amônia concentrado (NH4 OH);
b) adicionar 1,25 gramas do sal de magnésio do EDTA e diluir a 250 ml com água destilada.
Observação:
Caso não disponha do sal de magnésio do EDTA, dissolver 1,179 gramas do sal sódico do EDTA e 780 mg do MgSO4 .7H2 O ou 644 mg do MgCl2 .6H2 O em 50 ml de água destilada e juntar à solução do item 1, completando o volume para 250 ml com água destilada.
Indicador Eriocrome Black T:
a) pesar 0,5 gramas de Eriocrome Black T em um vidro de relógio;
b) pesar 100 gramas de Cloreto de Sódio P. A. em um Becker;
c) transferir os dois reagentes para um almofariz e triturar a mistura até se transformar em pó;
d) armazenar em frasco de boca larga, bem fechado.
34 Preparação dos Reagentes Utilizados nas Análises Constantes neste Manual IV:
Inibidor I - cianeto de sódio P.A:
Usar 250 mg na solução a ser titulada.
Inibidor II - sulfeto de sódio:
a) pesar 5 gramas de Sulfeto de Sódio ( Na2 S.9H2 O) ou 3,7 gramas de Na2 S.5H2 O;
b) dissolver em 100 ml de água destilada;
c) guardar em frasco de vidro bem fechado a fim de evitar sua deterioração por contato com o ar.
Solução padrão de cor:
a) pesar 1,246 gramas de Cloroplatinato de Potássio (K2 PtCl6 ) e 1,0 grama de Cloreto Cobaltoso cristalizado ( CoCl2 .6H2 O);
b) dissolver em água destilada;
c) acrescentar 100 ml de ácido clorídrico concentrado e diluir para 1000 ml com água destilada. (Esta solução equivale a 500 Unidades de Cor).
- Ácido sulfúrico (H2 SO4 ) 0,02N:
a) preparar igual ao utilizado para alcalinidade total.
- Ácido ascórbico:
a) pesar 0,1g de ácido ascórbico e dissolver em um pouco de água destilada e completar o volume para 100 ml. Esta solução deverá ser preparada diariamente.
- Reagente tampão:
a) pesar 136 g de acetato de sódio - NaC2 3H2 O e dissolver em água destilada. Adicionar 40 ml de solução de ácido acético 1N e diluir para 1000 ml com água destilada.
- Solução de ácido acético 1N:
a) medir 58 ml de ácido acético concentrado e diluir para 1000 ml com água destilada.
- Solução de Eriocromo Cianina-R (estoque):
a) pesar e dissolver 150 mg do corante em cerca de 50 ml de água destilada. Ajustar o pH para 2,9 com ácido acético 1:1 (são requeridos aproximadamente 2 ml de ácido). Diluir para 100 ml com água destilada.
- Solução de trabalho (Eriocromo Cianina-R):
a) medir 10 ml da solução-estoque e diluir para 100 ml com água destilada. Esta solução é estável por 6 meses.
- Solução indicadora de Metilorange:
a) pesar e dissolver 100 mg de metilorange em 200 ml de água destilada.
- Solução Estoque de Alumínio (1ml=500 μg Al):
a) pesar 8,791 g de Sulfato duplo de alumínio e potássio- AlK(SO4 o- .12H2 O e dissolver em um pouco de água destilada. Completar o volume para 1000 ml em balão volumétrico.
- Solução Padrão (1ml = 5 μg):
a) diluir 10 ml da solução estoque para 1000 ml com água destilada, em balão volumétrico. Preparar diariamente.
Observação:
a) todos os reagentes devem ser preparados com água destilada isenta de alumínio.
b) todos os procedimentos que determinam diluir ou completar para x ml, fazer em balão volumétrico.
- Solução de EDTA 0,01M:
a) (3,7 gramas de EDTA em 1000 ml de água destilada).
Reagentes para análise de fluoretos
- Solução padrão de fluoretos:
a) preparar uma solução-estoque, dissolvendo 221,0 mg de Fluoreto de Sódio anidro (NaF) em água destilada e diluir a 1000 ml (1 ml desta solução equivale a 100µgF-);
b) diluir 100 ml da solução estoque acima, para 1000 ml com água destilada (1 ml = 10 µgF-).
Reagente zirconio-alizarina:
a) pesar e dissolver 300 mg de Oxicloreto de Zircônio (ZrOCl2 .8H2 O), em 50 ml de água destilada e transferir para um frasco volumétrico de 1000 ml com tampa;
b) pesar e dissolver 70 mg de Monosulfato de Alizarina em 50 ml de água destilada
c) colocar a solução 2 na solução 1, lentamente e com agitação;
d) a solução resultante deverá ficar em repouso por alguns minutos.
35 Preparação dos Reagentes Utilizados nas Análises Constantes neste Manual V:
Mistura ácida:
a) medir 101 ml de Ácido Clorídrico concentrado (HCl) e diluir para aproximadamente 400 ml com água destilada;
b) adicionar cuidadosamente 33,3 ml de Ácido Sulfúrico concentrado (HC SO4 ) em aproximadamente 400 ml de água destilada;
c) após esfriar, misturar as duas soluções ácidas.
Reagentes Scott-Sanchis:
a) adicionar a mistura ácida à solução reagente Zirconilalizarina;
b) completar o volume para 1000 ml com água destilada e misturar;
c) guardar em frasco de cor âmbar e em lugar protegido da incidência de luz direta. Este reagente é estável por 6 meses.
Arsenito de sódio:
a) pesar 5 g de Arsenito de Sódio (NaAsO3 ) e dissolver em um pouco de água, diluir para 1 litro com água destilada (usar 1 gota para cada 0,1mg de cloro existente na amostra).
Observação: esta solução é tóxica - evitar ingestão.
36 Regras gerais para corrigir as soluções tituladas:
A correção das soluções tituladas é um procedimento muito utilizado em laboratório. Serve para aferir o grau de exatidão das soluções padronizadas. Periodicamente, o técnico deve verificar a exatidão dessas soluções para que os resultados das análises sejam os mais corretos possíveis.
Regra 1:
Quando o volume consumido de solução a titular for igual ao volume da solução-padrão tomado para a titulação, significa que aquela está exata. Ex.: 10 ml de HCl 0,1N foram consumidos para titular 10 ml de Na2 CO3 0,1N.
Regra 2:
Quando o volume consumido da solução a titular for menor que o volume do padrão tomado, significa que a solução a titular encontra-se mais concentrada. Nesse caso, faz-se a correção do seguinte modo: Ex.: Foram gastos na titulação de 10 ml de Na2 CO3 0,1N; 8,3 ml de HCl 0,1 N. Aplicando-se a seguinte equação, temos: 8,3 : 10 :: x : 1000. Efetuando-se os cálculos tem-se:

Regra 3:
No caso em que o volume da solução a titular for maior do que o da solução padrão, significa que a solução a titular encontra-se mais diluída. Nesse caso, calcula-se o fator de correção da seguinte forma:
Exemplo: 10,5 ml de uma solução de HCl 0,1N foram consumidos para titular 10 ml de uma solução padrão de Carbonato de Sódio. Aplicando-se a seguinte equação, temos: 10,5 : 10 :: 1 : x Efetuando-se os cálculos temos: 10 = 10,5x x = 10/10,5 x = 0,9524 Logo o Fator de correção da solução é 0,9524.
Limpeza de material de vidro no laboratório:
A precisão e exatidão das análises estão, além de outros fatores, também, ligadas ao uso do material de vidro no laboratório. Faz-se, portanto, necessário que toda a vidraria esteja perfeitamente limpa, livre de impurezas, tais como sabões, detergentes e outros produtos que podem ficar aderidos às paredes dos recipientes. A vidraria em geral pode ser lavada simplesmente com água,água e sabão neutro ou por meio de soluções especiais, como a solução sulfo-crômica, por exemplo.
Para vidraria nova:
a) a maioria dos materiais de vidros novos é levemente alcalina, portanto esses materiais devem ser colocados de molho por algumas horas em solução de ácido clorídrico ou nítrico a 1% antes de serem lavadas.
Para vidraria usada:
a) os materiais de vidro já utilizados com meio de cultura (placas de Petri, tubos de cultura), devem ser esterilizados antes de serem lavados. Depois devem ser colocados em um recipiente grande, com água contendo 1 a 2 % de sabão ou detergente, deixando ferver por 30 minutos. Em seguida devem ser enxaguados com água corrente, esfregados com detergentes neutros e enxaguados novamente;
b) em determinadas situações em que os materiais de vidro não puderem ser limpos com os detergentes comuns ou outros produtos de limpeza, faz necessário o uso de uma mistura constituída de acido sulfúrico e solução saturada de dicromato de sódio, preparada do seguinte modo: misturar 1 litro de ácido sulfúrico concentrado com 35 ml da solução saturada de dicromato de sódio. Esta solução não deve ser usada para lavagem de vidrarias utilizadas para análise de cromo.
Notas:
1. a solução acima é ácida e ataca a pele;
2. não permitir contato da mão com a solução;
3. a solução ataca os tecidos. Evitar contato com a roupa;
4. não lavar com a esta solução vidros colados como cubetas utilizadas em espectrofotômetros, cubetas de turbidez, etc.;
5. depois de passar esta solução na vidraria, enxaguá-la com bastante água e em seguida com água destilada.
37 Relação de materiais de laboratório de análise de água:
Equipamentos:
a) autoclave vertical, capacidade para 18, 24,48 ou 72 litros, 110/220 volts;
b) estufa para cultura bacteriológica, com termostato regulável na faixa de 30 a 65º C, tamanho 45x45x40 cm de largura, profundidade e altura, respectivamente, equipada com bandeja regulável para três posições;
c) balança analítica, elétrica, capacidade para 160 g, sensibilidade de 1/100 mg, cinco casas decimais, 110/220 volts;
d) balança de precisão, com dupla escala, pesagem máxima 200 gramas, sensibilidade de 0,1 g;
e) destilador de água, capacidade para 2 litros/hora, 110/220 volts;
f) banho-maria capacidade para 50 tubos de ensaio, com termostato regulável na faixa de 35 a 65º C, 110/220 volts;
g) banho de vapor, para 6 provas simultâneas, construído em chapa metálica, com termostato regulável em até 6 posições, 110/220 volts;
h) capela para exaustão forçada de gases, com motor elétrico de 1/3 de HP, 110/220 volts;
i) chapa aquecedora com termostato regulável, tamanho s, 110/220 volts;
j) estufa para esterilização e secagem, tamanho 50x40x50 cm de largura, profundidade e altura, respectivamente, com termostato regulável até 300º C, e bandeja regulável para 3 posições, 110/220 volts;
k) aparelho de Jar-Test para 6 provas simultâneas, com regulador de velocidade de 0 a 100 rpm, com base de vidro ou acrílico iluminada, 110/220 volts;
l) medidor de cloro residual, portátil, com disco de cor, escala de 0 a 3,5 mg/L, para uso com reagente DPD;
m) termômetro bacteriológico, com escala de 0 a 60º C, com divisões de 1ºC;
n) termômetro químico com escala de 0 a 300º C, com divisão de 1º C;
o) turbidímetro , completo;
p) medidor de pH digital, de bancada, faixa de medição de 0 a 14, com eletrodo, 110/220 volts;
q) medidor de pH, digital, portátil, faixa de medição de 0 a 14, com eletrodo, funcionamento à bateria de 9 volts;
r) lanterna para identificação de E.coli, com lâmpada fluorescente ultravioleta, 6 watts, 365 nm, recarregável, portátil, 110 volts;
s) bico de Bunsen;
t) deionizador capacidade para 50 litros/hora - 110/220 volts.
38 Vidraria:
a) tubo para cultura, sem borda, tamanho 150 x 16 mm;
b) tubo para cultura, sem borda, tamanho 180 x 18 mm;
c) tubo para cultura, sem borda, tamanho 125 x 15 mm;
d) tubo de Nessler, forma alta, capacidade de 50 e 100 ml;
e) tubo de Durhan, tamanho 40 x 5 mm;
f) balão volumétrico, fundo chato, com tampa de teflon ou vidro esmerilhado, classe ‘’ A “ capacidade de 50, 100, 250, 500 e 1000 ml;
g) becker forma baixa, graduado, capacidade de 50, 100, 250, 500 e 1000 ml;
h) bureta com torneira de vidro ou teflon, gravação permanente, classe “A “capacidade de 10, 25, e 50 ml;
i) pipeta sorológica, codificada por cores, com bocal para algodão, gravação permanente, capacidade de 1, 2, 5 e 50 ml;
j) pipeta de MOHR, codificada por cores, bocal e bico temperados, gravação permanente, capacidade de 1, 2, 5 e 10 ml;
k) pipeta volumétrica, codificada por cores, bocal e bicos temperados, gravação permanente, classe “A”, capacidade de 10, 25, 50 e 100 ml;
l) frasco de vidro para reagentes, boca larga, cor branca, com rolha de vidro esmerilhada intercambiável, capacidade de 125 ml;
m) proveta graduada a conter, com base hexagonal de vidro, gravação permanente, classe “A “, capacidade de 10, 25, 50, 100, 250, 500 e 1000 ml;
n) frasco Erlenmeyer, boca larga, reforçada, graduado, capacidade de 125, 250 e 500 ml;
o) funil analítico, ângulo de 60º, liso, haste curta, com diâmetro de 50, 75 e 100 mm;
p) funil analítico, ângulo de 60º, raiado, haste longa, com diâmetro de 50, 75 e 100 mm;
q) funil analítico, ângulo de 60º, raiado, haste curta, com diâmetro de 50, 75 e 100 mm;
r) Placa de Petri de vidro, transparente, tamanho 100 x 15 mm;
s) conjunto de destilação para fluoretos, constituído de balão de fundo chato de 1000 ml com saída lateral para condensador Grahan, com juntas esmerilhadas;
t) bastão de vidro de 30 cm de comprimento x 5 mm de diâmetro;
39 Materiais diversos:
a) alça de platina calibrada com 3 mm de diâmetro;
b) cabo de Kolle para alça de platina;
c) algodão em rama para bacteriologia;
d) lápis dermográfico;
e) caldo lactosado, desidratado, embalagem de 100 ou 500 gramas;
f) caldo lactosado, verde brilhante bile a 2%, desidratado, embalagem de 100 ou 500 gramas;
g) Meio ENDO MF, para coli total, embalagem de 100 ou 500 gramas;
h) Meio EC MF, para coli fecal, embalagem de 100 ou 500 gramas;
i) púrpura de bromocresol, embalagem de 5 gramas;
j) estante para tubo de ensaio, com capacidade para 15 tubos de 180 x 18 mm, de madeira ou plástico resistente.
k) estante para tubo de ensaio com capacidade para 40 tubos de 180 x 18 mm, em arame resistente a autoclavação;
l) caldo lauril triptose, desidratado, embalagem de 100 ou 500 gramas;
m) Meio EC, desidratado, embalagem de 100 ou 500 gramas.
n) Plate Count Agar, desidratado, embalagem de 100 ou 500 gramas;
o) substrato cromogênico para determinação enzimática qualitativa de coliformes totais e E.coli em amostras de 100 ml de água, caixa com 20 ampolas;
p) cesto de arame com capacidade para 50 tubos de ensaio de 180 x 18 mm, resistente a autoclavação;
q) suporte para tubo de Nessler de 50 e 100 ml, em madeira ou alumínio, capacidade para 8 tubos;
r) papel de alumínio, medindo 7,5 m de comprimento x 30 cm de largura;
s) algodão hidrófilo, pacote de 500 gramas;
t) Placa de Petri, de plástico, esterilizada, de 47 mm de diâmetro;
u) filtros estéries de 47 mm de diâmetro, 0,45µm de porosidade, com cartão absorvente, embalagem com 100 unidades;
v) conjunto porta-filtro de membrana, construído em aço inoxidável, com dispositivo para esterilização no ampol
w) pinça de aço inoxidável, de 10 cm de comprimento.
40 Biossegurança em laboratório:
Neste manual, constam apenas os principais procedimentos relacionados a Biossegurança em laboratório que deverão ser observados pelos técnicos que atuam na área.
Procedimentos de ordem pessoal:
a) não pipetar nenhum tipo de líquido com a boca;
b) usar óculos de proteção nos ambientes do laboratório onde o uso é obrigatório;
c) não levar as mãos à boca ou aos olhos quando estiver manuseando produtos químicos;
d) não guardar alimentos na geladeira do laboratório;
e) não fazer refeições dentro do laboratório;
f) não fumar no interior do laboratório;
g) lavar cuidadosamente as mãos com bastante água e sabão, antes de fazer qualquer refeição;
h) usar avental, sempre;
i) não manipular produtos tóxicos sem antes se certificar de sua toxicidade.
Procedimentos relacionados ao laboratório:
a) manter as bancadas do laboratório sempre limpas e livres de materiais estranhos ao trabalho;
b) retirar da bancada os materiais, amostras e reagentes empregados no trabalho, logo após utilizá-los;
c) limpar imediatamente qualquer derramamento de produtos e reagentes com os cuidados necessários;
d) ao esvaziar um frasco de reagente, fazer a limpeza prévia com água, antes de colocá-lo para lavagem;
e) rotular imediatamente qualquer reagente ou solução preparada e as amostras coletadas;
f) não jogar produtos corrosivos concentrados na pia; descartá-los somente após serem diluídos;
g) na preparação de soluções ácidas nunca adicionar água no ácido e sim ácido na água;
h) não jogar na pia líquidos inflamáveis e/ou voláteis; estocá-los em recipientes adequados;
i) dispor os cilindros com gases em ambiente externo ao laboratório, devidamente acondicionados;
j) usar capela de exaustão de gases para trabalhos com líquidos inflamáveis e/ou voláteis.
41 Procedimentos para o uso de vidrarias:
a) não utilizar materiais de vidro trincados;
b) usar luvas de amianto para manusear peças de vidro que estejam quentes;
c) não deixar frascos quentes sem proteção sobre as bancadas do laboratório, colocá-los sobre placas de amianto;
d) não aquecer recipiente de vidro em chama direta, usar tela de amianto;
e) não pressurizar recipientes de vidro;
f) não esquecer vidraria em aquecimento - usar despertador, sempre;
g) não usar frascos para amostras que não estejam perfeitamente limpos e sem certificar-se de sua adequação aos serviços a serem executados;
h) usar luvas de pelica e óculos de segurança, sempre que: atravessar ou remover rolhas de borracha ou cortiça, de tubos de vidro ou termômetros;
i) remover tampas de vidro emperradas;
j) remover cacos de vidro - usar pá de lixo e escova;
k) usar protetor facial e luvas de pelica quando agitar solventes voláteis em frascos fechados.
Procedimento para uso de equipamentos em geral:
a) antes de utilizar qualquer equipamento ler antes as instruções de operação fornecidas pelo fabricante;
b) nunca ligar equipamentos elétricos sem antes verificar a voltagem;
c) não instalar nem operar equipamentos elétricos sobre superfícies úmidas;
d) não deixar equipamentos elétricos ligados no laboratório fora do expediente, exceto os de energia constante como geladeiras, estufas, etc.;
e) combater fogo em equipamentos elétricos somente com extintor de CO2 ;
f) manter os equipamentos de segurança em locais de fácil acesso e ao alcance de todos os funcionários do laboratório, tais como:
- extintor de incêndio;
- chuveiro de emergência;
- lavador de olhos;
- cobertor de segurança;
- máscara contra gases;
- máscaras e óculos de segurança, etc.
42 Padrão microbiológico de potabilidade da água para consumo humano:
Art.11. A água potável deve estar em conformidade com o padrão microbiológico conforme Tabela 1, a seguir:
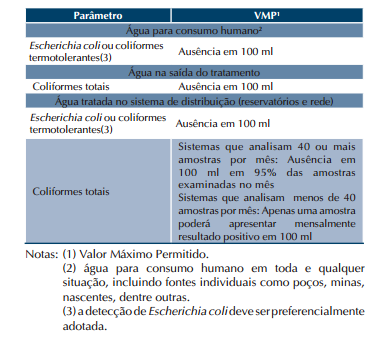
1º No controle da qualidade da água, quando forem detectadas amostras com resultado positivo para coliformes totais, mesmo em ensaios presuntivos, novas amostras devem ser coletadas em dias imediatamente sucessivos até que as novas amostras revelem resultado satisfatório. Nos sistemas de distribuição, a recoleta deve incluir, no mínimo, três amostras simultâneas, sendo uma no mesmo ponto e duas outras localizadas a montante e a jusante.
2º Amostras com resultados positivos para coliformes totais devem ser analisadas para Escherichia coli e, ou, coliformes termotolerantes, devendo, neste caso, ser efetuada a verificação e confirmação dos resultados positivos.
3º O percentual de amostras com resultado positivo de coliformes totais em relação ao total de amostras coletadas nos sistemas de distribuição deve ser calculado mensalmente, excluindo as amostras extras (recoleta).
4º O resultado negativo para coliformes totais das amostras extras (recoletas) não anula o resultado originalmente positivo no cálculo dos percentuais de amostras com resultado positivo.
5º Na proporção de amostras com resultado positivo admitidas mensalmente para coliformes totais no sistema de distribuição, expressa na Tabela 1, não são tolerados resultados positivos que ocorram em recoleta, nos termos do § 1º deste artigo.
6º Em 20% das amostras mensais para análise de coliformes totais nos sistemas de distribuição, deve ser efetuada a contagem de bactérias heterotróficas e, uma vez excedidas 500 unidades formadoras de colônia (UFC) por ml, devem ser providenciadas imediata recoleta, inspeção local e, se constatada irregularidade, outras providências cabíveis.
7º Em complementação, recomenda-se a inclusão de pesquisa de organismos patogênicos, com o objetivo de atingir, como meta, um padrão de ausência, dentre outros, de enterovírus, cistos de Giardia spp e oocistos de Cryptosporidium sp.
8º Em amostras individuais procedentes de poços, fontes, nascentes e outras formas de abastecimento sem distribuição canalizada, tolera-se a presença de coliformes totais, na ausência de Escherichia coli e, ou, coliformes termotolerantes, nesta situação devendo ser investigada a origem da ocorrência, tomadas providências imediatas de caráter corretivo e preventivo e realizada nova análise de coliformes.
Art. 12. Para a garantia da qualidade microbiológica da água, em complementação às exigências relativas aos indicadores microbiológicos, deve ser observado o padrão de turbidez expresso na Tabela 2, abaixo:
Tabela 2 - Padrão de turbidez para água pós-filtração ou pré-desinfecção:

1º Dentre os 5% dos valores permitidos de turbidez superiores aos VMP estabelecidos na Tabela 2, o limite máximo para qualquer amostra pontual deve ser de 5,0 uT, assegurado, simultaneamente, o atendimento ao VMP de 5,0 UT em qualquer ponto da rede no sistema de distribuição.
2º Com vistas a assegurar a adequada eficiência de remoção de enterovírus, cistos de Giardia spp e oocistos de Cryptosporidium sp., recomenda-se, enfaticamente, que, para a filtração rápida, se estabeleça como meta a obtenção de efluente filtrado com valores de turbidez inferiores a 0,5 uT em 95% dos dados mensais e nunca superiores a 5,0 uT.
3º O atendimento ao percentual de aceitação do limite de turbidez, expresso na Tabela 2, deve ser verificado, mensalmente, com base em amostras no mínimo diárias para desinfecção ou filtração lenta e a cada quatro horas para filtração rápida, preferivelmente, em qualquer caso, no efluente individual de cada unidade de filtração.
Art. 13. Após a desinfecção, a água deve conter um teor mínimo de cloro residual livre de 0,5 mg/l, sendo obrigatória a manutenção de, no mínimo, 0,2 mg/L em qualquer ponto da rede de distribuição, recomendando-se que a cloração seja realizada em pH inferior a 8,0 e tempo de contato mínimo de 30 minutos.
Parágrafo único. Admite-se a utilização de outro agente desinfetante ou outra condição de operação do processo de desinfecção, desde que fique demonstrado pelo responsável pelo sistema de tratamento uma eficiência de inativação microbiológica equivalente à obtida com a condição definida neste artigo.
Art.14. A água potável deve estar em conformidade com o padrão de substâncias químicas que representam risco para a saúde expresso na Tabela 3, a seguir:
Tabela 3 - Padrão de potabilidade para substâncias químicas que representam risco à saúde:
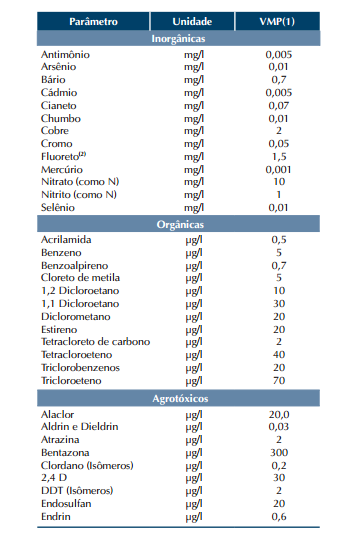

1º Recomenda-se que as análises para cianotoxinas incluam a determinação de cilindrospermopsina e saxitoxinas (STX), observando, respectivamente, os valores limites de 15,0 µg/l e 3,0 µg/l de equivalentes STX/l.
2º Para avaliar a presença dos inseticidas organofosforados e carbamatos na água, recomenda-se a determinação da atividade da enzima acetilcolinesterase, observando os limites máximos de 15% ou 20% de inibição enzimática, quando a enzima utilizada for proveniente de insetos ou mamíferos, respectivamente.
Art. 15. A água potável deve estar em conformidade com o padrão de radioatividade expresso na Tabela 4, a seguir:
Tabela 4 - padrão de radioatividade para água potável:

Art. 16. A água potável deve estar em conformidade com o padrão de aceitação de consumo expresso na Tabela 5, a seguir:
Tabela 5 - padrão de aceitação para consumo humano:
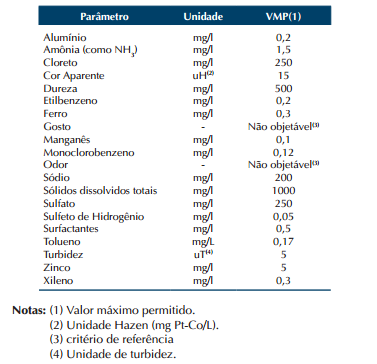
Recomenda-se que, no sistema de distribuição, o pH da água seja mantido na faixa de 6,0 a 9,5. Recomenda-se que o teor máximo de cloro residual livre, em qualquer ponto do sistema de abastecimento, seja de 2,0 mg/l. Recomenda-se a realização de testes para detecção de odor e gosto em amostras de água coletadas na saída do tratamento e na rede de distribuição de acordo com o plano mínimo de amostragem estabelecido para cor e turbidez nas Tabelas 6 e 7.
Art. 17. As metodologias analíticas para determinação dos parâmetros físicos, químicos, microbiológicos e de radioatividade devem atender às especificações das normas nacionais que disciplinem a matéria, da edição mais recente da publicação Standard Methods for the Examination of Water and Wastewater, de autoria das instituições American Public Health Association (APHA), American Water Works Association (AWWA) e Water Environment Federation (WEF), ou das normas publicadas pela ISO (International Standartization Organization).
Para análise de cianobactérias e cianotoxinas e comprovação de toxicidade por bioensaios em camundongos, até o estabelecimento de especificações em normas nacionais ou internacionais que disciplinem a matéria, devem ser adotadas as metodologias propostas pela Organização Mundial da Saúde (OMS) em sua publicação Toxic cyanobacteria in water: a guide to their public health consequences, monitoring and management. Metodologias não contempladas nas referências citadas no 1º e “caput” deste artigo, aplicáveis aos parâmetros estabelecidos nesta Norma, devem, para ter validade, receber aprovação e registro pela SVS.
As análises laboratoriais para o controle e a vigilância da qualidade da água podem ser realizadas em laboratório próprio ou não que, em qualquer caso, deve manter programa de controle de qualidade interna ou externa ou ainda ser acreditado ou certificado por órgãos competentes para esse fim.
43 Planos de amostragem:
At. 18. Os responsáveis pelo controle da qualidade da água de sistema ou solução alternativa de abastecimento de água devem elaborar e aprovar, junto a autoridade de saúde pública, o plano de amostragem de cada sistema, respeitando os planos mínimos de amostragem expressos nas Tabelas 6, 7, 8 e 9.
Tabela 6 -
Número mínimo de amostras para o controle da qualidade da água de sistema de abastecimento, para fins de análises físicas, químicas e de radioatividade, em função do ponto de amostragem, da população abastecida e do tipo de manancial.
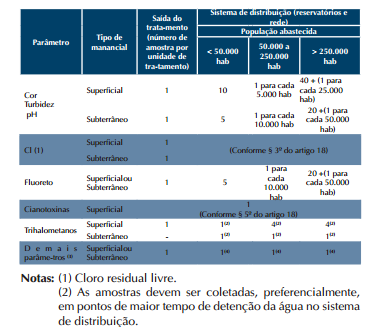
Apenas será exigida obrigatoriedade de investigação dos parâmetros radioativos quando da evidência de causas de radiação natural ou artificial. Dispensada análise na rede de distribuição quando o parâmetro não for detectado na saída do tratamento e, ou, no manancial, à exceção de substâncias que potencialmente possam ser introduzidas no sistema ao longo da distribuição.
Tabela 7 -
Frequência mínima de amostragem para o controle da qualidade da água de sistema de abastecimento, para fins de análises físicas, químicas e de radioatividade, em função do ponto de amostragem, da população abastecida e do tipo de manancial.
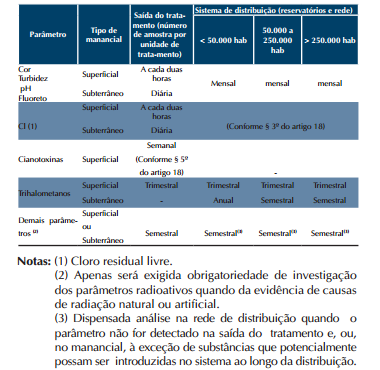
Tabela 8 -
Número mínimo de amostras mensais para o controle da qualidade da água de sistema de abastecimento, para fins de análises microbiológicas, em função da população abastecida.
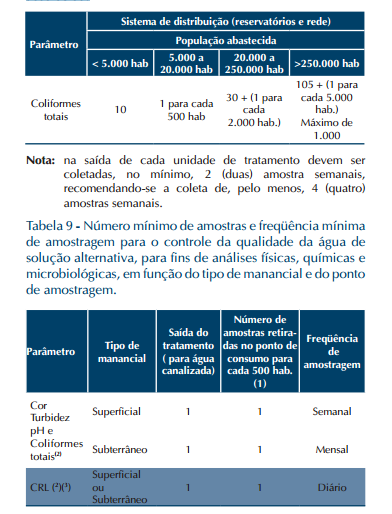
Notas:
Devem ser retiradas amostras em, no mínimo, 3 pontos de consumo de água. Para veículos transportadores de água para consumo humano, deve ser realizada 1 (uma) análise de CRL em cada carga e 1 (uma) análise, na fonte de fornecimento, de cor, turbidez, PH e coliformes totais com frequência mensal, ou outra amostragem determinada pela autoridade de saúde pública. Cloro residual livre.
A amostragem deve obedecer aos seguintes requisitos:
I - distribuição uniforme das coletas ao longo do período; e
II - representatividade dos pontos de coleta no sistema de distribuição (reservatórios e rede), combinando critérios de abrangência espacial e pontos estratégicos, entendidos como aqueles próximos a grande circulação de pessoas terminais rodoviários, terminais ferroviários, etc.) ou edifícios que alberguem grupos populacionais de risco (hospitais, creches, asilos, etc.), aqueles localizados em trechos vulneráveis do sistema de distribuição (pontas de rede, pontos de queda de pressão, locais afetados por manobras, sujeitos à intermitência de abastecimento, reservatórios, etc.) e locais com sistemáticas notificações de agravos à saúde tendo como possíveis causas agentes de veiculação hídrica.
No número mínimo de amostras coletadas na rede de distribuição, previsto na Tabela 8, não se incluem as amostras extras (recoletas). Em todas as amostras coletadas para análises microbiológicas deve ser efetuada, no momento da coleta, medição de cloro residual livre ou de outro composto residual ativo, caso o agente desinfetante utilizado não seja o cloro. Para uma melhor avaliação da qualidade da água distribuída, recomenda-se que, em todas as amostras referidas no deste artigo, seja efetuada a determinação de turbidez. Sempre que o número de cianobactérias na água do manancial, no ponto de captação, exceder 20.000 células/ml (2mm3/l de biovolume), durante o monitoramento que trata o do artigo 19, será exigida a análise semanal de cianotoxinas na água na saída do tratamento e nas entradas (hidrômetros) das clínicas de hemodiálise e indústrias de injetáveis, sendo que esta análise pode ser dispensada quando não houver comprovação de toxicidade na água bruta por meio da realização semanal de bioensaios em camundongos.
Art. 19. Os responsáveis pelo controle da qualidade da água de sistemas e de soluções alternativas de abastecimento supridos por manancial superficial devem coletar amostras semestrais da água bruta, junto do ponto de captação, para análise de acordo com os parâmetros exigidos na legislação vigente de classificação e enquadramento de águas superficiais, avaliando a compatibilidade entre as características da água bruta e o tipo de tratamento existente.
1º O monitoramento de cianobactérias na água do manancial, no ponto de captação, deve obedecer freqüência mensal, quando o número de cianobactérias não exceder 10.000 células/ml (ou 1mm3/l de biovolume), e semanal, quando o número de cianobactérias exceder este valor.
2º É vedado o uso de algicidas para o controle do crescimento de cianobactérias ou qualquer intervenção no manancial que provoque a lise das células desses microrganismos, quando a densidade das cianobactérias exceder 20.000 células/ml (ou 2mm3/l de biovolume), sob pena de comprometimento da avaliação de riscos à saúde associados às cianotoxinas.
Art. 20. A autoridade de saúde pública, no exercício das atividades de vigilância da qualidade da água, deve implementar um plano próprio de amostragem, consoante diretrizes específicas elaboradas no âmbito do Sistema Único de Saúde - SUS.
44 Das exigências aplicáveis aos sistemas e soluções alternativas de abastecimento de água:
Art. 21. O sistema de abastecimento de água deve contar com responsável técnico, profissionalmente habilitado.
Art. 22. Toda água fornecida coletivamente deve ser submetida a processo de desinfecção, concebido e operado de forma a garantir o atendimento ao padrão microbiológico desta Norma.
Art. 23. Toda água para consumo humano suprida por manancial superficial e distribuída por meio de canalização deve incluir tratamento por filtração.
Art. 24. Em todos os momentos e em toda sua extensão, a rede de distribuição de água deve ser operada com pressão superior à atmosférica.
1º Caso esta situação não seja observada, fica o responsável pela operação do serviço de abastecimento de água obrigado a notificar a autoridade de saúde pública e informar à população, identificando períodos e locais de ocorrência de pressão inferior à atmosférica.
2º Excepcionalmente, caso o serviço de abastecimento de água necessite realizar programa de manobras na rede de distribuição, que possa submeter trechos a pressão inferior à atmosférica, o referido programa deve ser previamente comunicado à autoridade de saúde pública.
Art. 25. O responsável pelo fornecimento de água por meio de veículos deve:
I - garantir o uso exclusivo do veículo para este fim;
II - manter registro com dados atualizados sobre o fornecedor e, ou, sobre a fonte de água; e
III - manter registro atualizado das análises de controle da qualidade da água.
A água fornecida para consumo humano por meio de veículos deve conter um teor mínimo de cloro residual livre de 0,5 mg/l.
O veículo utilizado para fornecimento de água deve conter, de forma visível, em sua carroceria, a inscrição: “água potável”.
45 Das penalidades:
Art. 26. Serão aplicadas as sanções administrativas cabíveis, aos responsáveis pela operação dos sistemas ou soluções alternativas de abastecimento de água, que não observarem as determinações constantes desta Portaria.
Art. 27. As Secretarias de Saúde dos Estados, do Distrito Federal e dos municípios estarão sujeitas a suspensão de repasse de recursos do Ministério da Saúde e órgãos ligados, diante da inobservância do contido nesta Portaria.
Art. 28. Cabe ao Ministério da Saúde, por intermédio da SVS/MS, e às autoridades de saúde pública dos Estados, do Distrito Federal e dos Municípios, representadas pelas respectivas Secretarias de Saúde ou órgãos equivalentes, fazer observar o fiel cumprimento desta Norma, nos termos da legislação que regulamenta o Sistema Único de Saúde (SUS).
46 Das disposições finais:
Art. 29. Sempre que forem identificadas situações de risco à saúde, o responsável pela operação do sistema ou solução alternativa de abastecimento de água e as autoridades de saúde pública devem estabelecer entendimentos para a elaboração de um plano de ação e tomada das medidas cabíveis, incluindo a eficaz comunicação à população, sem prejuízo das providências imediatas para a correção da anormalidade.
Art. 30. O responsável pela operação do sistema ou solução alternativa de abastecimento de água pode solicitar à autoridade de saúde pública a alteração na freqüência mínima de amostragem de determinados parâmetros estabelecidos nesta Norma.
Parágrafo único. Após avaliação criteriosa, fundamentada em inspeções sanitárias e, ou, em histórico mínimo de dois anos do controle e da vigilância da qualidade da água, a autoridade de saúde pública decidirá quanto ao deferimento da solicitação, mediante emissão de documento específico.
Art. 31. Em função de características não conformes com o padrão de potabilidade da água ou de outros fatores de risco, a autoridade de saúde pública competente, com fundamento em relatório técnico, determinará ao responsável pela operação do sistema ou solução alternativa de abastecimento de água que amplie o número mínimo de amostras, aumente a freqüência de amostragem ou realize análises laboratoriais de parâmetros adicionais ao estabelecido na presente Norma.
Art. 32. Quando não existir na estrutura administrativa do estado a unidade da Secretaria de Saúde, os deveres e responsabilidades previstos no artigo 6º deste Anexo serão cumpridos pelo órgão equivalente.
47 Apêndice:
No final da elaboração deste manual, já revisado e adaptado para a atual legislação sobre qualidade de água para consumo humano, foram incluídos os procedimentos básicos de coleta de amostras de água para a quantificação das cianobactérias e análise das cianotoxinas em mananciais de abastecimento. A finalidade da inclusão deste tópico é orientar os operadores de ETA’s a se familiarizarem com o procedimento para tomada de posição quando o fato ocorrer ou houver necessidade de atuação. O estudo das cianobactérias, atualmente, tem sido a “coqueluche” do momento. Depois do acidente ocorrido em uma clínica de hemodiálise na cidade de Caruarú-PE, as autoridades sanitárias do país, passaram a dar mais atenção à questão que se tornou um grande problema para a saúde pública, culminando com a sua inclusão na legislação que trata da potabilidade da água, como parâmetro de controle. A Fundação Nacional de Saúde, entidade ligada ao Ministério da Saúde, patrocinou a realização de dois eventos que tratam do estudo das Cianobactérias tóxicas: o primeiro foi realizado na cidade do Rio de Janeiro no ano de 2001 e o segundo durante o 1º Seminário Internacional de Saúde Pública realizado na cidade de Recife-PE em 2002. Neste último evento, foi ministrado um curso sobre “Diagnóstico Preliminar da Ocorrência de Cianobactérias em Mananciais de Água para Consumo Humano” tendo como instrutoras as Professoras Sandra M. F. O. Azevedo e Vera L. M. Huszar, ambas especialistas no assunto. Durante o curso, foram abordados a ocorrência de Cianobactérias em mananciais de abastecimento, os perigos que representam para a saúde dos animais, principalmente do homem, as formas de prevenção das florações, os limites toleráveis, tanto de células quanto de toxinas e os procedimentos de coleta para análise de cianobactérias em água bruta e cianotoxinas em amostras de água bruta e tratada. Com o material fornecido pelas instrutoras, foi possível incluir neste manual os procedimentos de coleta.
Procedimento de coleta de amostras para quantificação de cianobactérias em água bruta:
Material necessário:
Frasco de vidro cor âmbar de 100 ml. Garrafa de van Dorn ou Similar. Solução de lugol (fixador).
Local da coleta:
Ponto de captação (tomada d’água); Amostras de superfície; Amostras de várias profundidades(estratificadas).
Técnica:
Amostra de superfície
Encher o recipiente (frasco de 100 mL) com água da superfície ou do ponto de captação; Adicionar 1 mL da solução de lugol; A amostra preservada dura 10 semanas (aprox. 3 meses).
Amostras de profundidade:
Mergulhar a garrafa de van Dorn até a profundidade desejada; Enchê-la e retornar à superfície; Desconectar a parte superior da mangueira que fica na lateral da garrafa e encher o frasco de 100 ml; Adicionar ao frasco de coleta (100 ml), 1 ml da solução de lugol; A amostra preservada com lugol dura aproximadamente 3 meses.
Identificação das amostras:
Identificar as amostras anotando o local da coleta, as profundidades (se forem coletadas a várias profundidades), a data e hora da coleta, o nome do coletador, etc.
Destino das amostras:
As amostras podem ser analisadas no próprio laboratório da ETA, caso haja condições, ou serem enviadas para laboratórios especializados.
48 Referências bibliográficas:
BATALHA, B.H.L., PARLATORE, A. C. Controle da qualidade da água para o consumo humano; bases conceituais e operacionais. 1ª ed. São Paulo: Cetesb, 1977.
BRASIL. Fundação Nacional de Saúde. Manual técnico de análise de água para consumo humano. Brasília: Funasa, 1999
BRASIL. Ministério da Saúde. Portaria n. 518, de 25.03.04. Dispõe sobre normas e padrões de potabilidade de água para consumo humano. Brasília: SVS, 2004.
COELHO, L. Técnicas de laboratório clínico: guia de coleta e preservação de amostras de água. 1ª ed. São Paulo: Cetesb, 1987.
LIMPEZA de vidraria. Disponível em: http://www.profcupido.ig.com.br/conserv_e_limpeza_vidrarias.htm. Acesso em: marco 2004.
MAIER, F. J. Fluoruracion del agua potable. 1ªed. México:Limusa-Wiley, 1971.
MANUAL de tratamiento de aguas. 4ªed. México: LimusaWiley, 1974.
OPERAÇÃO e manutenção de E.T.A. São Paulo: Cetesb, 1973. V.2.
ORGANIZAÇÃO PAN-AMERICANA DA SAÚDE. Fascículo água: a desinfecção da água. Brasília: OPAS, 1999.
Organizacion Mundial de la Salud. Guias para a calidad del agua potable. 2ªed. Ginebra: OMS, 1995. V.1.
Organizacion Mundial de la Salud. Guias para a calidad del agua potable. 1ªed. Ginebra: OMS, 1998. V.3.
SANTOS FILHO, D. F. Tecnologia de tratamento de água:água para indústria. 1ª ed. Rio de Janeiro: AN, 1976.
SILVA, M.O.S.A. Análises físico-químicas para controle de estações de tratamento de esgotos. 1ª ed. São Paulo: Cetesb, 1977.
STANDARD methods for the examination of water and wastewater. 16th ed. Washington: APHA, 1985.
TÉCNICAS de abastecimento e tratamento de água. 2ªed. São Paulo: Cetesb, 1977. V.2.
TÉCNICAS de análises microbiológicas da água; membrana filtrante, 1ª ed. São Paulo: Cetesb, 1997.