Teoria da Refrigeração - Conceito de Termodinâmica
Instalação e Manutenção de Ar Condicionado SPLIT
1 Princípios térmicos
Propriedades termodinâmicas
A ciência termodinâmica estabelece os conceitos que explicam os fenómenos físicos de transferência de energia térmica, identifica os elementos físicos, as propriedades e as respectivas leis que descrevem os fenómenos térmicos. As principais grandezas e características a saber são:
A temperatura (T), é uma grandeza que indica o estado térmico da substância, que por sua vez caracteriza a capacidade que a substância tem para trocar energia com outra em que esteja em contacto. A pressão (P), é uma força normal (perpendicular a uma superfície) exercida por um fluido por unidade de área, existe também a pressão absoluta quando a pressão da substância é medida juntamente com a pressão atmosférica. A densidade (ρ), específica a massa que ocupa uma unidade de volume, volume específico v, é o que caracteriza o volume de uma unidade de massa da substância.
A densidade e volume específico são recíprocos um relativamente ao outro. O calor específico (c), é a quantidade de energia requerida para elevar a temperatura 1ºC em cada grama de substância. Como a amplitude desta quantidade é influenciada pelo processo realizado, o método como o calor é adicionado ou retirado é também caracterizado pelo calor específico a volume constante (c) e calor específico a pressão constante (c). A entalpia descreve a energia interna total de uma substância, que em determinados processos a sua variação será igual ao calor transferido nesse processo.
A entropia apesar de ser uma propriedade das mais fundamentais e amplamente utilizada na termodinâmica, em sistemas de refrigeração não tem grande relevo, mas está fundamentalmente associada a uma grandeza de desordem interna da substância. Na grande maioria dos sistemas de aquecimento e refrigeração utilizam os estados de fase das substâncias no seu estado líquido ou gasoso para caracterizar o funcionamento dos sistemas.
2 Conceitos básicos da termodinâmica
Equilíbrio térmico, lei zero da termodinâmica, equilíbrio termodinâmico
Empiricamente sabemos que dois corpos com a mesma massa, mas com temperaturas diferentes, T1 e T2, quando entram em contacto, a temperatura dos corpos alteram-se, diminuindo no corpo mais quente e aumentando no corpo mais frio. O equilíbrio térmico é atingido quando a temperatura final dos corpos é uma temperatura intermédia entre duas temperaturas iniciais. Em termos matemáticos, estes resultados podem ser formular-se através da equação Error! Reference source not found.
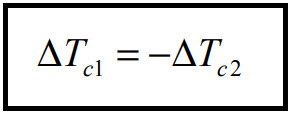
A lei zero da termodinâmica postula que dois sistemas em equilíbrio térmico com um terceiro estão em equilíbrio térmico entre si. Pode haver equilíbrio térmico sem haver equilíbrio termodinâmico, para haver equilíbrio termodinâmico tem que existir as seguintes condições:
• Equilíbrio mecânico ( forças e movimento = 0)
• Equilíbrio químico
• Não haver troca de materiais

Gás ideal, trabalho, 1ª Lei da termodinâmica e entalpia
Habitualmente, utilizam-se o conceito de gás ideal para representar diversos conceitos da termodinâmica. Um gás ideal é um gás hipotético em que as condições de separação entre moléculas são muito maior do que as dimensões das mesmas, inexistência de interação entre as moléculas (excepto durante colisões), bem como a ausência de choques elásticos entre moléculas e entre estas e as paredes do recipiente. Admite-se que as moléculas movem-se aleatoriamente, com a mesma probabilidade em qualquer direção. As suas características macroscópicas, tal como, o volume, a pressão e a temperatura obedecem à equação de estado dos gases ideais em que n representa o número de moles da substância e R é a constante universal dos gases.
Sabe-se que um gás real tem um comportamento próximo de um gás ideal quanto menor for a pressão a que está sujeito e quanto mais afastado se encontrar da sua temperatura do seu ponto de liquefação. A equação de estado de um gás ideal pode ser obtida combinando as leis de Boyle e de Charles. Lei de Boyle-“O volume de uma dada quantidade de gás, a temperatura constante, varia inversamente com a pressão.”