Manual de Métodos de Análise de Solo: Análise Química
Análise de Solos
1 pH (H²0, KCI e CaCI²)/ Carbono Orgânico/ Nitrogênio Total/ Capacidade de Troca de Cátions (CTC) e Bases Trocáveis:
pH (H²0, KCI e CaCI²)
Princípio:
Medição do potencial eletronicamente por meio de eletrodo combinado imerso em suspensão solo:líquido (água, KCl ou CaCl²), 1:2,5
Procedimento:
- Colocar 10ml de solo em copo plástico de 100ml numerado.
- Adicionar 25ml de líquido (água, KCl 1N ou CaCl2 0,01 M).
- Agitar a amostra com bastão de vidro individual e deixar em repouso uma hora.
- Agitar cada amostra com bastão de vidro, mergulhar os eletrodos na suspensão homogeneizada e proceder a leitura do pH.
Reagentes:
Solução de KCl 1N - dissolver 74,5g de KCl em água e elevar a 1L.
Solução padrão de CaCl² M - pesar 147g de CaCl² 2H²O para 1L de solução. Agitar, deixar esfriar e completar o volume.
Solução de CaCl² 0,01 M - diluir 10ml do padrão para cada litro de solução. Medir a C.E. desta solução, que deve ser da ordem de 2,3mS/cm.
Soluções padrão pH 4,00 e pH 7,00 - diluir ampolas padrão.
Equipamento:
- Potenciômetro com eletrodo combinado.
Observação:
Ligar o potenciômetro 30 minutos antes de começar a ser usado.
Aferir o potenciômetro com as soluções padrão pH 4,00 e pH 7,00.
Trabalhando em série, não é necessário lavar os eletrodos entre uma e outra amostra, mas é indispensável antes e depois de aferir o aparelho com as soluções padrão. Para horizonte sulfúrico ou material sulfídrico (Solo Tiomórfico) usar a suspensão, solo:água 1:1.
Carbono Orgânico:
Princípio:
Oxidação da matéria orgânica via úmida com dicromato de potássio em meio sulfúrico, empregando-se como fonte de energia o calor desprendido do ácido sulfúrico e/ou aquecimento. O excesso de dicromato após a oxidação é titulado com solução padrão de sulfato ferroso amoniacal (sal de Mohr).
Procedimento:
- Tomar aproximadamente 20g de solo, triturar em gral e passar em peneira de 80 mesh.
- Pesar 0,5g do solo triturado e colocar em erlenmeyer de 250ml.
- Adicionar 10ml (pipetados) da solução de dicromato de potássio 0,4N. Incluir um branco com 10ml da solução de dicromato de potássio e anotar o volume de sulfato ferroso amoniacal gasto.
- Colocar um tubo de ensaio de 25mm de diâmetro e 250mm de altura cheio de água na boca do erlenmeyer, funcionando este como condensador.
- Aquecer em placa elétrica até a fervura branda, durante 5 minutos.
- Deixar esfriar e juntar 80ml de água destilada, medida com proveta, 2ml de ácido ortofosfórico e 3 gotas do indicador difenilamina.
- Titular com solução de sulfato ferroso amoniacal 0,1N até que a cor azul desapareça, cedendo lugar à verde.
- Anotar o número de mililitros gastos.
Cálculo:

Observação:
Para teores > que 2% de carbono, pipetar quantidades crescentes de dicromato de potássio : 20, 30, 40, ou 50ml até que a coloração da solução permaneça amarela, sem traços de verde. Proceder à fervura e, após esfriar, diluir a solução de 1:5, ou seja, para volumes de 100, 150, 200 e 250 respectivamente. Pipetar 50ml, diluir com água e titular com sulfato ferroso; aplicar a expressão indicada para o cálculo do carbono, uma vez que a alíquota corresponde a 10ml da solução de dicromato de potássio.
Para as amostras em que os 50ml da solução de dicromato de potássio são insuficientes para oxidar toda matéria orgânica, usar 0,25g de solo.
Em caso de solos salinos, adicionar uma pitada de sulfato de prata após adição de dicromato de potássio.
Reagentes:
Solução de K2Cr2O7, 0.4 N em meio ácido - dissolver 39,22g de K2Cr2O7 p.a. (previamente seco em estufa a 130ºC por uma hora), em 500 ml de água contida em balão aferido de 2L. Juntar uma mistura, já fria, de 1.000ml de ácido sulfúrico concentrado e 500ml de água. Agitar bem para dissolver todo o sal, esfriar e completar o volume do balão com água.
Solução de sulfato ferroso amoniacal 0,1 N - dissolver 40g de Fe (NH4)2 (SO4)2.6H2O cristalizado, (sal de Mohr), em 500ml de água contendo 10ml de ácido sulfúrico concentrado. Agitar e completar para 1L.
Difenilamina (indicador) - pesar 1g de difenilamina e dissolver em 100ml de ácido sulfúrico concentrado.
Sulfato de prata ( catalisador)- utilizar o sal puro (Ag2SO4 ).
Ácido ortofosfórico (H3PO4) concentrado (85%) p.a. - usar concentrado.
Equipamento:
- Bureta digital.
- Agitador magnético.
Nitrogênio Total:
Princípio O nitrogênio em solos tropicais está praticamente ligado à matéria orgânica. Neste método, o N é convertido em sulfato de amônio através de oxidação com uma mistura de CuSO4, H2SO4 e Na2SO4 ou K2SO4 (mineralização).
Posteriormente em meio alcalino, o sulfato de amônio convertido da matéria orgânica libera amônia que, em câmara de difusão, é complexada em solução de ácido bórico contendo indicador misto, sendo finalmente determinado por acidimetria (H2SO4 ou HCl).
- Duas técnicas são descritas considerando o mesmo princípio:
- Kjeldahl por câmara de difusão;
- Kjeldahl por destilação a vapor.
Procedimento:
Kjeldahl por câmara de difusão.
- Pesar 0,7g de solo, colocar em balão kjeldahl de 100ml, pesado com aproximação de 0,001g.
- Adicionar 15ml de mistura ácida de sulfatos e proceder a digestão, fervendo o conteúdo durante 1 hora ou mais, até completa destruição da matéria orgânica.
- Deixar esfriar, juntar 25ml de água, agitar para homogeneizar e adicionar 2 gotas de solução xaroposa de cloreto férrico.
- Juntar, gradativamente, solução de NaOH a 30% até que a solução apresente coloração castanho-claro (início da formação dos compostos básicos de ferro).
- Deixar esfriar, colocar o balão na balança, adicionar água até se obter o peso do balão mais 60,35g e misturar bem a solução.
- Preparar a câmara de difusão, colocando sobre a balança o pesafiltro e adicionar, com auxílio de pipeta, 12g da solução parcialmente neutralizada (correspondente a 140mg de solo).
- Colocar 2,5ml da solução de ácido bórico e 4 gotas do indicador misto no recipiente plástico, e este em um tripé de porcelana sobre a câmara de difusão.
- Adicionar ao líquido contido na câmara proveniente do ataque, 2ml da solução de NaOH 30% e fechar imediatamente. Colocar vaselina na tampa da câmara para evitar perdas de amônia formada pela reação .
- Agitar ligeiramente a solução através de movimentos circulares e deixar em repouso durante uma noite.
- Abrir a câmara, retirar o recipiente de plástico contendo o ácido bórico e transferir para bécher de 100ml, lavando com mais ou menos 10ml de água.
- Titular com solução de H2SO4 ou HCl 0,01 N até a mudança da coloração roxa para rósea.
- Utilizar uma prova em branco e calcular a quantidade de N na amostra.
Kjeldahl por destilação a vapor:
- Pesar 0,7g de solo, colocar em balão kjeldahl de 100ml, pesado com aproximação de 0,001g.
- Adicionar 15ml da mistura ácida de sulfatos e proceder a digestão, fervendo o conteúdo durante 1 hora ou mais, até completa destruição da matéria orgânica.
- Deixar esfriar, juntar 25ml de água, agitar para homogeneizar e adicionar 2 gotas de solução xaroposa de cloreto férrico.
- Juntar, gradativamente, solução de NaOH a 30% até que a solução apresente coloração castanho-claro (início da formação dos compostos básicos de ferro).
- Deixar esfriar, colocar o balão na balança, adicionar água até se obter o peso do balão mais 60,35g e misturar bem a solução.
- Transferir 12g (10ml) da solução parcialmente neutralizada (extrato oriundo da mineralização do N) para microdestilador kjeldahl.
- Paralelamente, colocar 25ml de solução de ácido bórico a 4% em erlenmeyer de 125ml, adicionando a esta solução 5 gotas do indicador misto.
- Inserir a extremidade livre do destilador na solução, tendo o cuidado de mantê-la sempre imersa até o final da destilação.
- Adicionar à solução parcialmente neutralizada (extrato oriundo da mineralização do N) 2ml de soda 30% e proceder a destilação da amônia, a vapor, durante 5 minutos.
- Titular o volume destilado, depois de frio, com solução padronizada de H2SO4 0,01 N, até a mudança da cor roxa ou azulada para rósea.
- Finalmente, proceder à prova em branco.
Cálculo:

Observação:
A câmara de difusão é constituída de pesa-filtro de forma baixa, medindo 80 x 30mm, com tampa esmerilhada. O recipiente plástico é formado de tampa de polietileno de 30mm de diâmetro.
Para fins de levantamento de solos, esse resultado é representado como nitrogênio total; entretanto, essa determinação é considerada como nitrogênio orgânico e amoniacal.
Reagentes:
Solução ácida de sulfatos de sódio e de cobre - pesar 180g de Na2SO4 e dissolver em aproximadamente 1 litro de água contida em balão aferido de 2 litros. Adicionar 18g de CuSO4 5H2O e, em seguida, 600ml de H2SO4 concentrado; deixar esfriar e completar o volume.
Solução de hidróxido de sódio a 30% - pesar 300g de NaOH, dissolver em água e completar o volume para 1 litro.
Indicador misto. (verde de bromocresol + vermelho de metila) - dissolver 0,1g de verde de bromocresol e 0,02g de vermelho de metila em álcool etílico e completar o volume para 100ml.
Ácido sulfúrico ou clorídrico 0,01N - preparar a partir da solução N ou 0,1N.
Ácido bórico - pesar 40g do ácido, dissolver em água e elevar a 1 litro.
Equipamento:
- Digestor - tubos de digestão kjeldahl em bloco de aquecimento.
- Bureta digital.
Capacidade de Troca de Cátions (CTC) e Bases Trocáveis:
Princípio:
A CTC do solo é definida como sendo a soma total dos cátions que o solo pode reter na superfície coloidal prontamente disponível à assimilação pelas plantas. Estes cátions adsorvidos são removidos por soluções salinas de amônio, cálcio, bário e soluções de ácidos diluídas e posteriormente determinados por métodos volumétricos, de emissão ou absorção atômica.
Procedimento:
Quatro técnicas de extração são descritas sucessivamente.
Método do KCl N:
Extração:
- Pesar 7,5g de solo, colocar em erlenmeyer de 250ml e adicionar 150ml de solução de KCl N.
- Fechar com rolha de borracha e agitar com movimentos circulares, evitando molhar a rolha; repetir essa operação várias vezes ao dia.
- Depois da última agitação, desfazer o montículo que se forma na parte central do fundo do erlenmeyer e deixar em repouso durante uma noite.
- Pipetar para erlenmeyer de 200ml duas alíquotas de 50ml da parte sobrenadante da solução, para determinação do alumínio extraível, cálcio + magnésio e cálcio trocáveis.
Observação:
Foi preferido um único extrator para cálcio, magnésio e alumínio, a fim de tornar mais verdadeira a relação entre Al+++ e (S + Al+++), uma vez que a soma das bases é, na sua maior parte, composta de Ca++ e Mg++.
A pequena solubilidade dos carbonatos alcalino-terrosos no KCl N, possibilita seu emprego em solos com calcário.
Reagente:
Solução de KCl N normal - pesar 74,6g do sal, previamente seco em estufa, para cada litro de solução a ser preparada.
Método do HCl 0,05 N
Extração:
- Pesar 10g de solo, colocar em erlenmeyer de 200ml e adicionar 100ml da solução de ácido clorídrico 0,05 N.
- Fechar com rolha de borracha e agitar com movimentos circulares, evitando molhar a rolha; repetir esta operação várias vezes ao dia.
- Depois da última agitação, desfazer o montículo que se forma na parte central do fundo do erlenmeyer e deixar em repouso durante uma noite.
- Filtrar e, no filtrado, determinar o sódio e o potássio em fotômetro de chama, diretamente ou em alíquotas diluídas conforme os teores de Na+ e K + existentes na amostra.
Reagente:
Solução de HCl 0,05N - preparar por diluição a partir de produtos concentrados de ótima qualidade.
Método do acetato de cálcio a pH 7,0
Extração:
- Pesar 10g de solo, colocar em erlenmeyer de 200ml e juntar 150ml de solução de acetato de cálcio pH 7,0.
- Fechar com rolha de borracha e agitar com movimentos circulares, evitando molhar a rolha; repetir esta operação várias vezes ao dia.
- Depois da última agitação, desfazer o montículo que fica na parte central do fundo do erlenmeyer e deixar em repouso durante uma noite.
- Utilizar o sobrenadante da solução para a determinação da acidez extraível (H++ Al+++).
Reagente:
Solução de acetato de cálcio N a pH 7,0 - pesar 80g do sal para preparar 1L de solução, dissolvendo em água. Aferir com o potenciômetro para pH 7,0 a 7,1, empregando ácido acético glacial ou hidróxido de cálcio.
Método do acetato de amônio a pH 7,0
Extração
- Pesar 12,5g de solo, colocar em erlenmeyer de 250ml e adicionar 125 ml da solução de acetato de amônio a pH 7,0.
- Fechar com rolha de borracha, agitar com movimentos circulares, evitando molhar a rolha e repetir essa operação várias vezes ao dia.
- Depois da última agitação, desfazer o montículo que se forma na parte central do erlenmeyer e deixar em repouso durante uma noite.
- Pipetar 100ml do líquido sobrenadante e passar para depósito de plástico com tampa, de onde são tiradas as alíquotas para determinação dos íons trocáveis.
Observação:
O Na+ e o K+ são determinados pelo fotômetro de chama e o Ca++ e Mg++ pelo EDTA ou espectrometria de absorção atômica.
Reagentes:
Solução de acetato de amônio N pH 7,0 - transferir 116ml de ácido acético glacial para um bécher de 3 litros contendo aproximadamente 1.600ml de água. Adicionar 140ml de hidróxido de amônio concentrado, preferivelmente por meio de funil de haste longa que mergulha na solução, para evitar a evaporação do hidróxido de amônio. Agitar e adicionar água até próximo dos 2 litros. Levar a solução para um potenciômetro e ajustar, adicionando ácido acético ou hidróxido de amônio, o pH até 7,0. Passar para um balão aferido de 2 litros e completar o volume.
Determinação:
Alumínio trocável:
Princípio:
Extração com solução KCl N e determinação volumétrica com solução diluída de NaOH.
Procedimento:
Em uma das duas alíquotas de 50ml obtidas na extração com KCl N, adicionar 3 gotas do indicador azul de bromotimol e titular com solução de NaOH 0,025 N, até a coloração verde-azulada persistente.
Observação:
O KCl, por ser um sal derivado de ácido e base fortes, dispensa a prova em branco sistemática. O sal sendo de boa procedência, deverá virar o azul de bromotimol após a adição da primeira gota de NaOH. O Ca+++Mg++ são determinados na alíquota após a determinação de Al+++.
No caso de solos ricos em matéria orgânica a determinação espectrofotométrica por absorção atômica é mais indicada, visto que os íons hidrogênio dissociados durante a extração com KCl são também dosados no método volumétrico.
O alumínio pode ser determinado colorimetricamente de acordo com o procedimento descrito no Manual de Métodos de Análise de Solo de 1979, item 2.8.
Cálculo:

Reagentes:
Indicador azul de bromotimol - pesar 0,1g do indicador, colocar em gral de quartzo e adicionar 1,6ml de NaOH 0,1 N. Triturar até a dissolução completa. Caso a cor verde desapareça, adicionar algumas gotas de NaOH. Passar o resíduo para balão de 100ml e completar o volume com água.
Solução de NaOH 0,025 N - pipetar 25ml da solução normal de NaOH para balão aferido de 1 litro, completando o volume com água.
Equipamento:
- Bureta digital.
- EAA.
4.3.2 Cálcio e magnésio trocáveis:
Princípio:
Extração com solução KCl N e determinação complexiométrica em presença dos indicadores eriochrome e murexida ou calcon.
Procedimento:
- No erlenmeyer onde foi feita a titulação do Al+++ trocável, adicionar 1 gota de água de bromo para destruir o azul de bromotimol .
- Adicionar 6,5ml do coquetel tampão e 4 gotas do indicador eriochrome black e titular, imediatamente, com a solução de EDTA 0.0125 N, até viragem da cor vermelho-arroxeada para azul puro ou esverdeada (com esta titulação são determinados conjuntamente (Ca++ e Mg++).
- Anotar o volume de EDTA gasto.
4.3.2.3 Cálculo:

Reagentes:
Coquetel tampão: solução tampão pH 10 - dissolver 67,5g de NH4Cl em 200ml de água e colocar em balão aferido de 1 litro. Adicionar 600ml de NH4OH concentrado, 0,616g de MgSO4 7H2O e 0,930g de EDTA, sal dissódico. Agitar bem até dissolver e completar o volume.
Verificar a “neutralidade” da solução em relação ao EDTA e ao magnésio, colocando 50 ml de água em erlenmeyer de 125 ml, 3 ml da solução tampão e 4 gotas de eriochrome black; a cor avermelhada deverá virar para azul puro pela adição de uma gota do EDTA 0,0125M. Misturar 300 ml da solução tampão pH 10 com 300 ml de trietanolamina e 50 ml de cianeto de potássio a 10%, agitar e guardar em frasco próprio.
Solução de EDTA 0,0125M - pesar 4,653g do EDTA p.a. previamente seco em estufa e dissolver em água contida em balão de 1 litro, completando o volume.
Indicador eriochrome black - dissolver 100mg do indicador em 25ml de álcool metílico contendo 16g de bórax por litro. Esta solução deve ser usada recém-preparada devido à facilidade de se deteriorar.
Murexida - pesar 0,5g do indicador, colocar em gral de porcelana e misturar com 100g de sulfato de potássio seco em pó, triturando bem. Guardar em vidro escuro.
Solução de KCN ou KOH a 10% - pesar 100g, colocar em balão aferido de 1 litro contendo água, dissolver completamente e completar o volume.
Equipamento:
- Bureta digital.
4.3.3 Cálcio trocável:
Princípio:
Extração com solução KCl N e determinação complexiométrica em presença dos indicadores eriochrome e murexida ou calcon.
Procedimento:
- No segundo erlenmeyer, colocar 2ml de trietanolamina a 50%, 2ml de KOH a 10% e uma pitada de murexida (± 50mg). Titular com solução de EDTA 0,0125 M até viragem da cor rósea para roxa.
- Anotar o volume de EDTA gasto, que corresponde ao cálcio existente.
Cálculo:
Calcular a percentagem de cálcio na amostra de solo de acordo com a seguinte expressão:
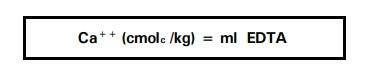
Reagentes:
Ver item 4.3.2.3.
Equipamento:
- Bureta digital.
Magnésio trocável:
Determinação:
Diferença entre os valores de Ca+++Mg++ (ver item 4.3.2) e Ca++ (ver item 4.3.3).
Potássio trocável
Princípio: Extração com solução diluída de ácido clorídrico e posterior determinação por espectrofotometria de chama.
Procedimento:
- Passar o extrato de solo obtido com HCl 0,05N no fotômetro de chama, utilizando o filtro próprio do potássio.
- Fazer a leitura e diluir a solução caso a leitura ultrapasse a do padrão utilizado.
Cálculo:

Observação:
Para obtenção do fator fk, preparar 4 soluções padrão de K+ e Na+ contendo cada uma 0,01 - 0,02 - 0,03 e 0,04 cmolc /L.
4.3.5.3 Reagentes:
Solução padrão de KCl e NaCl (0,1cmolc /l ) - pesar 0,0746g de KCl e 0,0585g da NaCl previamente secos em estufa e dissolver em solução de HCl 0,05 N até completar o volume de 1 litro.
Solução padrão de K+ e Na+ - pipetar para balões aferidos de 500ml as seguintes quantidades da solução anterior: 50, 100, 150 e 200ml. Completar o volume com solução de HCl 0,05 N. Transferir para frascos e anotar no rótulo as concentrações de 0,01 - 0,02 - 0,03 e 0,04 cmolc /L respectivamente.
Passar essas 4 soluções no fotômetro e anotar os valores das leituras sendo recomendável que a leitura do padrão de 0,02 cmolc /L de K + ou Na+ represente exatamente a metade da escala do galvanômetro.
Traçar o gráfico leitura x concentração e determinar o fator fk.
Equipamento:
- Fotômetro de chama.
Sódio trocável:
Princípio:
Extração com solução diluída de ácido clorídrico e posterior determinação com espectrofotometria de chama.
Procedimento:
- Passar o extrato de solo obtido com HCl 0,05N no fotômetro de chama, utilizando o filtro próprio do Na+.
- Proceder a leitura do aparelho; diluir a solução quando a leitura ultrapassar a escala do aparelho.
Cálculo:

Observação:
Para a obtenção do fator fNa, preparar 4 soluções padrão contendo:
0,1 - 0,2 - 0,3 e 0,4 cmolc /l de Na+, conforme item 4.3.5.4, determinar a curva, ou traçar o gráfico leitura x concentração de Na+, para o cálculo do fator fNa.
A solução padrão de sódio pode ser preparada isoladamente; entretanto, como as determinações dos trocáveis envolvem as duas determinações (Na+ e K+), uma só solução torna-se mais prática. Quando se tratar de solos muito ricos em Na+, há necessidade de se proceder várias diluições para poder atingir a escala do aparelho.
Reagente:
Solução padrão de sódio - ver item 4.3.5.4.
Equipamento:
- Fotômetro de chama.
Soma de cátions trocáveis (valor S):
Cálculo:
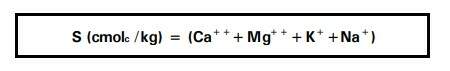
2 Acidez do Solo/ Hidrogênio extraível/ Valor T - CTC (Capacidade de Troca de Cátions)/ Valor V (Percentagem de Saturação de Bases):
Acidez do Solo:
Serão descritos dois métodos diferentes para a determinação da acidez do solo:
Acidez trocável - a acidez (H + Al) liberada pela reação com solução não tamponada de KCl. Pode ser designada como acidez real e é utilizada para determinar o que se denomina CTC efetiva, que é definida como a soma das bases + (H + Al).
Acidez potencial - a acidez obtida pela extração com solução tamponada de acetato de cálcio N pH 7,0. Pode ser denominada como acidez extraível ou acidez titulável e é por vezes referida erroneamente como acidez trocável. É utilizada para calcular a CTC do solo, definida como a soma das bases + acidez potencial.
Acidez trocável:
Princípio:
Soluções não tamponadas de sais neutros como o KCl não produzem acidez por dissociação de radicais carboxílicos (H+), e assim o H+ + Al+++ determinados correspondem às formas trocáveis.
A determinação é feita titulando-se com NaOH em presença de fenolftaleína como indicador.
Procedimento:
Duas técnicas de extração da acidez trocável são descritas sucessivamente.
Método do KCl N:
- Colocar 10g de solo em erlenmeyer de 125ml e adicionar 50ml de KCI N.
- Agitar manualmente algumas vezes e deixar em repouso durante 30 minutos.
- Filtrar em papel de filtro tipo Whatman no 42 de 5,5cm de diâmetro, adicionando duas porções de 10ml de KCl N.
- Adicionar ao filtrado 6 gotas de fenolftaleína a 0,1% e titular com NaOH 0,1N até o aparecimento da cor rosa.
a) Cálculo:

b) Reagentes:
KCl N - dissolver 74,5g do sal em 1 litro de água.
Fenolftaleína (0,1%) - dissolver 0,1g em 100ml de álcool etílico
NaOH 0,1N - dissolver 1 ampola de titrisol conforme instruções. Diluir 100ml para 1l.
c) Equipamento:
- Bureta digital.
Método do BaCl2 0,1M
- Colocar 10g de solo em erlenmeyer de 250ml e adicionar 100ml de BaCl2 0,1M.
- Agitar em agitador mecânico por 1 hora ou manualmente por 1 minuto, deixando a suspensão em equilíbrio por uma noite.
- Pipetar 50ml do sobrenadante.
- Determinar a acidez com NaOH 0,025N, usando 3 gotas de fenolftaleína 1% como indicador.
- Fazer a prova em branco e comparar com o ponto de viragem do indicador.
a) Cálculo:
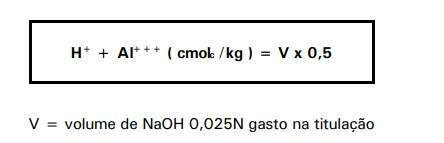
b) Reagentes:
BaCl2.2H2O 0,1 M - pesar 24,4g do sal, colocar em balão volumétrico de 1 litro contendo 700ml de água e completar o volume.
NaOH 0,025 - dissolver uma ampola padrão (titrisol ou fixanal) de NaOH conforme instruções. Colocar 25ml desta solução em balão volumétrico e completar a 1 litro.
c) Equipamento:
- Bureta Digital
Cálculo
A CTC efetiva pode então ser calculada:

Acidez potencial:
Princípio:
Extração da acidez dos solos com acetato de cálcio tamponado a pH 7,0 e determinado volumetricamente com solução de NaOH em presença de fenolftaleína como indicador.
Para solos de clima temperado, o método do cloreto de bário com trietanolamina tamponada a pH 8,2 é o mais utilizado.
Procedimento:
- Pipetar 100ml da solução sobrenadante obtida com acetato de cálcio (ver item 4.2.3.1) e passar para erlenmeyer de 200ml (evitar o arraste de partículas de solo).
- Adicionar 5 gotas da solução de fenolftaleína a 3% e titular com a solução de 0,0606 N de NaOH até o desenvolvimento da cor rósea persistente.
- Para cada série de amostras utilizar uma prova em branco.
Cálculo:
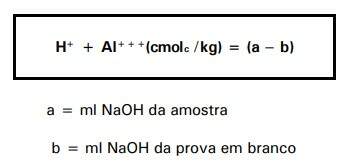
Observação:
O emprego de NaOH 0,0606 N elimina o fator 1,65 usualmente utilizado no cálculo de (H+ + Al+++).
Reagentes:
Indicador fenolftaleína 3% - dissolver 3g do indicador em álcool etílico, completando o volume para 100ml.
Solução de hidróxido de sódio 0,0606 N - preparar a partir de solução padrão de NaOH através de diluições de ampolas (titrisol ou fixanal), conforme instruções.
Equipamento:
- Bureta digital.
Hidrogênio Extraível:
Cálculo:
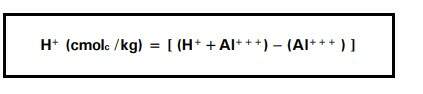
Observação:
Determinado em amostras com pH em água abaixo de 7,0.
Valor T - CTC (Capacidade de Troca de Cátions):
Cálculo:
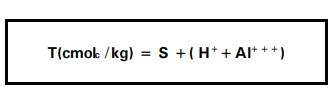
Valor V (Percentagem de Saturação de Bases):
Cálculo:

Observação:
Representa a participação das bases trocáveis em relação ao total de cátions no complexo. Este valor é utilizado para a caracterização de solos eutróficos e distróficos.
3 Percentagem de Saturação com Alumínio/ Percentagem de saturação com sódio/ Troca compulsiva (CTC e CTA)/ Ponto de carga zero (PCZ):
Percentagem de Saturação com Alumínio:
Cálculo:
A percentagem de saturação com alumínio é dada pela seguinte expressão:

Observação:
Esta relação é empregada na separação de classes de solo quanto ao caráter álico.
Percentagem de Saturação Como Sódio:
Cálculo:
A percentagem de saturação com sódio é dada pela seguinte expressão:

Observação:
O valor do Na+ corresponde ao sódio trocável; este valor é utilizado na classificação de solos salinos, sódicos e não salinos.
Troca Compulsiva (CTC e CTA):
Princípio: Troca compulsiva baseada na saturação do solo com solução de BaCl2 e posterior adição de solução padrão de MgSO4. A quantidade de Mg++ retirada do MgSO4 representa a CTC (troca catiônica) e o Cl- retido a CTA (troca aniônica). Estas determinações são feitas ao pH do solo com concentrações eletrolíticas próximas às encontradas no campo.
Procedimento:
- Pesar 1,0g de solo e colocar em tubo de centrífuga de 30ml previamente pesado.
- Adicionar 20ml de BaCl2 0,05M e agitar por 2 horas em agitador mecânico.
- Centrifugar e reter o sobrenadante para posterior determinação dos cátions trocáveis, Ca++, Mg++, Na+ e K+, se for o caso.
- Lavar duas vezes com 20ml de BaCl2 0,002M, agitando 1 hora em cada lavagem. Descartar o sobrenadante.
- Após a segunda lavagem com o BaCl2 diluído, pesar os tubos contendo o solo úmido para determinação do BaCl2 entrante.
- Adicionar 20ml de MgSO4 0,0025M e agitar por 1 hora. Ajustar a condutividade elétrica para 0,3 mS /cm, utilizando água deionizada ou a solução de MgSO4 0,0025M. Agitar por 1 hora ou deixar por uma noite.
- Pesar os tubos para determinar o volume de MgSO4 0,0025M ou água.
- Centrifugar e determinar o Mg++ e o Cl- no sobrenadante.
Observação:
O Mg++ pode ser determinado por complexiometria com EDTA, ou absorção atômica e o Cl- por complexiometria com o Hg(NO3)2 em presença de difenilcarbazona e azul de bromofenol como indicador. A padronização do Hg(NO3)2 0,02 N é recomendada, sendo normalmente feita com solução de NaCl 0,02 N
Cálculos:
CTC
Se o Mg++ foi adicionado para o ajuste da condutividade da solução.

Reagentes:
Solução de BaCl2.2H2O 0,1M - dissolver 24,4g do sal em água e completar o volume a 1l.
Solução de BaCl2 0,002M - preparar a partir de ampolas padronizadas.
Solução de MgSO4 0,0025M - preparar a partir de ampolas padronizadas.
Solução de Hg (NO3 )2 .0,02 N - adicionar em balão volumétrico de 1 litro com ± 700ml de água, 20ml de HNO3 2M e 3,0g de Hg (NO3)2. Agitar até dissolução completa do sal e completar o volume com água.
Difenilcarbazona + verde de bromofenol - dissolver 0,1g de cada indicador em 100ml de etanol. Conservar na geladeira.
NaCl 0,02N - secar em estufa (120°C) por 6 horas uma alíquota do sal P.A. Após resfriar em dessecador, pesar 1,169g, dissolver em balão volumétrico e completar a 1l com água. Usar a solução para padronizar o Hg (NO3)2.
Equipamento:
- Bureta digital.
- EAA.
Ponto de Carga Zero (PCZ):
Princípio:
O PCZ é o ponto de cruzamento entre três ou quatro curvas de titulação potenciométricas em soluções eletrolíticas de sais formados por íons indiferent es (NaCl ou KCl).
Procedimento:
- Colocar 4,0g de solo em 45 bécheres e ordená-los em três filas de 15.
- Adicionar 10ml de NaCl ou KCl 0,2M, 0,02M, 0,002M nos bécheres das filas I, II e III, respectivamente. O bécher mediano (no 8) passa a ser chamado de zero, porque só receberá a solução de NaCl ou KCl.
- Adicionar nos bécheres de nos 1 a 7: 0,25, 0,50, 1,0, 1,5, 2,0, 2,5 e 3ml de HCl 0,1N e nos de nos 9 a 15: 0,25, 0,50, 1,0, 1,5, 2,0, 2,5 e 3,0ml de NaOH 0,1N.
- Adicionar água em cada um dos bécheres para completar o volume de 20ml.
- Deixar em equilíbrio durante 4 dias, agitando ocasionalmente.
- Fazer curva de titulação com ácido e base para cada uma das três concentrações eletrolíticas empregadas. Estas correspondem ao teste em branco.
- Após o repouso de 4 dias, determinar o pH das suspensões e calcular as adsorções de H + e OH- adicionados, subtraindo-se dos valores determinados nos brancos correspondentes.
- Plotar as concentrações de H+ e OH- adsorvidos contra os pH de cada concentração eletrolítica empregada, de forma a se obter um gráfico. As concentrações finais das três curvas serão respectivamente: 10-¹mol dm-³ , 10-²mol dm-³ e 10-³ mol dm-³.
- O ponto de cruzamento comum as três curvas de titulação potenciométricas correspondem às adsorções iguais de H+ e OH- e, portanto, o PCZ desejado.
Observação:
No caso de determinação de PCZ obtido pelo cruzamento de apenas três curvas de titulação potenciométricas, sugere-se a eliminação de curva de concentração molar.
Reagentes:
Solução de NaCl ou KCl 0,2M - pesar 11,7g de NaCl ou 14,9g de KCl, colocar em balão volumétrico de 1 litro contendo 500ml de água e completar o volume.
Soluções de NaCl ou KCl 0,02M e 0,002M - são preparadas a partir das respectivas soluções 0,2M.
Solução de HCl 0,1N - preparada através de ampola padronizada, tipo titrisol ou fixanal.
Solução de NaOH 0,1N - preparada através de ampola padronizada tipo titrisol ou fixanal.
Equipamento:
- Potenciômetro digital, de precisão centesimal
4 Ataque Sulfúrico/ Sílica/ Ferro no extrato sulfúrico/ Alumínio no extrato sulfúrico/ Titânio no extrato sulfúrico:
Ataque Sulfúrico:
Princípio:
A solubilização de amostras de solo com H2SO4 1:1, visando a determinação de relações moleculares (Ki e Kr), permite a avaliação de estágios de intemperização de solos.
Procedimento:
- Pesar 1g de solo e colocar em erlenmeyer de 500ml (previamente testado quanto à qualidade do vidro) ou em recipiente de teflon.
- Adicionar 20ml de ácido sulfúrico diluído de 1:1 e ferver durante meia hora, usando condensador de refluxo para evitar evaporação.
- Deixar esfriar, adicionar 50ml de água e filtrar para balão aferido de 250ml, lavando o resíduo com água até completar o volume.
- Utilizar o filtrado para as determinações de ferro, alumínio, titânio, manganês e fósforo total, e o resíduo, para a determinação da sílica.
Observação:
O extrato sulfúrico produzido com essa força iônica pressupõe que somente minerais secundários (argilo-minerais) são dissolvidos e assim os percentuais de Fe, Al, Si, Ti são próximos aos da fração coloidal do solo.
Reagente:
Ácido sulfúrico diluído de 1:1 - medir 500ml de H2S04 concentrado d=1,84 e colocar, vagarosamente, em bécher de 2 litros contendo 500 ml de água. Deixar esfriar e colocar em vidro próprio.
Equipamento:
- Placa aquecedora.
Sílica:
Princípio:
Solubilização da sílica proveniente do ataque sulfúrico com solução de NaOH e posterior desenvolvimento da cor azul do complexo sílico-molíbdico através da redução do molibdato com ácido ascórbico.
Procedimento:
- Passar o resíduo retido no papel de filtro (método 13) com auxílio de pisseta com água (usar aproximadamente 150ml), para o mesmo erlenmeyer onde foi feito o ataque sulfúrico. Esta operação é facilitada colocando-se o papel de filtro aberto em funil grande, preso em suporte, e aplicando-se um jato fino e forte de água.
- Adicionar 4ml de solução de NaOH a 30% e colocar o erlenmeyer em placa elétrica até início de fervura, usando sistema de refrigeração.
- Deixar esfriar e transferir tudo para balão aferido de 200ml (ou acertar a 201,2g), com auxílio de pisseta; completar o volume com água.
- Filtrar e receber o filtrado límpido em frasco de polietileno (desprezar os dois primeiros).
- Pipetar 0,2ml do filtrado com micropipeta (pipeta Seligson, USA) em copo plástico de 150ml.
- Adicionar aproximadamente 50ml de água, e, com controle de tempo da aplicação dos reagentes, adicionar 2,5ml da solução de molibdato de amônio. Após 10 minutos, juntar 2,5ml de solução de ácido tartárico 28% e, decorridos ± 5 minutos, 30mg de ácido ascórbico, como redutor.
- Passar o conteúdo para balão aferido de 100ml e completar o volume com água.
- Deixar o balão em repouso para desenvolvimento da cor. Após 12 horas, nunca depois de 24 horas, medir a absorvância a 695 mµ e anotar a leitura.
- Para obtenção da percentagem de sílica na amostra, preparar 3 padrões (em duplicata), de solução contendo 6 a 6,5% de SiO2, proveniente de amostras de solo O teor de sílica é controlado trimestralmente pelo processo gravimétrico.
- Pipetar 0,1, 0,2 e 0,4ml deste extrato e proceder da mesma forma descrita para a amostra; determinar os valores das leituras no espectrofotômetro correspondentes a cada solução, e empregar o valor médio para o cálculo do fator de conversão da leitura em percentagem de sílica.
Cálculo:
Quando a leitura da amostra não ultrapassar a leitura do padrão de 0,2ml:

Observação:
A leitura das amostras deverá ficar entre 100 e 300 mu para a alíquota de 0,2ml. Diluir ou tomar alíquotas maiores que 0,2ml, se necessário.
Reagentes:
Solução ácida de molibdato de amônio - dissolver 89g do sal em ± 600ml de água e adicionar, lenta e continuamente, 62ml de H2SO4 (concentrado previamente diluído a 100ml com água), agitando constantemente. Esfriar e transferir para balão aferido de 1 litro. Completar o volume com água.
Ácido ascórbico - usar sal puro p.a. (± 30mg), ou solução recém preparada.
Ácido tartárico - 28%.
Equipamento:
- EAM
Ferro no Extrato Sulfúrico:
Princípio:
Determinação por complexiometria com EDTA ou por espectrofotometria de absorção atômica no extrato sulfúrico.
Procedimento:
- Pipetar 20ml do extrato sulfúrico (método 13) e colocar em bécher de 300ml de forma alta.
- Adicionar 2,5ml da solução de HCl + HNO3 e ferver por alguns minutos, até completa destruição da matéria orgânica (desaparecimento da cor escura).
- Repetir a operação quando a destruição não for completa.
- Adicionar 25 a 30ml de água e ajustar o pH da solução para 1,5, em potenciômetro, empregando solução de HCl 1:1 e NH4OH concentrado, quando for o caso.
- Adicionar, em seguida, 1ml da solução de ácido sulfossalicílico como indicador e aquecer até temperatura aproximada de 60ºC.
- Titular com solução de EDTA 0,01M, passando a coloração de vermelho para amarelo (observar que a reação é lenta).
- Após a titulação separar o bécher com a solução, para ser empregada na determinação de Al2O3.
Cálculo:

Observação:
O ferro pode ser determinado com o EDTA a pH 2,0 a 2,2; entretanto, quando se usa a mesma alíquota para a determinação do alumínio, é recomendável baixar esse pH a 1,5, a fim de tornar a determinação do ferro mais seletiva.
Reagentes:
Ácido clorídrico 1:1 - adicionar 500ml de água em proveta de 1 litro e juntar 500ml de HCl concentrado.
Ácido clorídrico + ácido nítrico 1:4 - colocar 50ml de HNO3 concentrado em proveta de 250ml e adicionar, vagarosamente, 200ml de HCL 1:1. Agitar, homogeneizar e guardar em vidro escuro.
Ácido sulfossalicílico 5% - pesar 50g do produto e dissolver em água, contida em balão de 1 litro. Agitar até dissolver e completar o volume.
EDTA 0,01 M - pesar, exatamente, 3,7224g do sal (etileno-diaminotetra-acetato de sódio) e dissolver em água contida em balão aferido de 1 litro. Agitar até completa dissolução e completar o volume. Guardar em recipiente de polietileno e padronizar com solução de cloreto de cálcio 0,01 M.
Cloreto de cálcio 0,01 M - pesar 1g de CaCO3 puro p.a. e colocar em bécher de 250ml. Umedecer e em seguida aplicar, gota a gota, ácido clorídrico concentrado, até total dissolução do sal. Aquecer caso seja necessário. Transferir para balão aferido de 1 litro, lavar bem o bécher e completar o volume.
Equipamento:
- Bureta digital.
- EAA.
Alumínio no Extrato Sulfúrico:
Princípio:
Determinação por complexometria com CDTA ou por espectrofotometria de absorção atômica no extrato sulfúrico.
Procedimento:
- Após a dosagem de Fe2O3 pelo EDTA, adicionar 10ml da solução de CDTA (aguardar mais ou menos 1 hora), 10ml da solução tampão de acetato de amônio pH 4,5 (esperar 10 minutos), 50ml de álcool etílico e 2ml de solução de ditizona (recém-preparada).
- Titular o excesso de CDTA com solução de sulfato de zinco, até viragem de cor verde-acinzentada para cor rosa forte, sendo esta mudança nítida e instantânea.
- Paralelamente, empregar uma prova em branco e determinar o volume de sulfato de zinco necessário para reagir com 10ml do CDTA.
Cálculo:

Observação:
Este método determina conjuntamente o alumínio e o titânio, sendo necessário descontar o TiO2 obtido pelo método para ter o resultado só de Al2O3. Em caso de solos com alto teor de TiO2 (Latossolo Roxo, por exemplo) é conveniente recorrer à separação prévia do titânio e ferro por precipitação, para em seguida proceder à determinação do Al2O3 pelo mesmo método.
Reagentes:
Solução do CDTA 0,031M - pesar exatamente 11,30g do ácido 1,2 ciclo-hexilenodinitrilo - tetracético. Colocar em bécher de 250ml e adicionar 100ml de solução de NaOH 2,5%, recém-preparada. Agitar bem com bastão de vidro até dissolver; transferir para balão aferido de 1 litro, adicionando água até completar o volume. Guardar a solução em depósito de polietileno.
Acetato de amônio de pH 4,5 - colocar 6ml do ácido acético (C2O2H4) glacial em balão aferido de 50ml, contendo 40ml de água. Homogeneizar e completar o volume. Transferir a solução para erlenmeyer de 125ml, adicionar 2 gotas de azul de bromotimol e titular com NH4OH concentrado até viragem do azul para o verde, anotando o volume gasto. Preparar a solução tampão, colocando 120ml do ácido acético em balão aferido de 1 litro contendo 500ml de água e adicionar, pouco a pouco, agitando, a quantidade de NH4OH gasto na titulação ant erior multiplicada por 10. Agitar e completar o volume.
Álcool etílico absoluto - utilizar o produto comercial.
Solução de ditizona a 0,025% - pesar 0,025g de ditizona (difeniltiocarbazona) e dissolver em 100ml de álcool etílico p.a. Esta solução é instável, podendo ser usada no máximo por 2 a 3 dias se colocada em geladeira.
Solução de sulfato de zinco 0,0156M - pesar 4,5190g de ZnSO4.7H2O, colocar em balão aferido de 1 litro contendo água, agitar, homogeneizar e completar o volume.
Equipamento:
- Bureta digital.
- EAA.
Titânio no Extrato Sulfúrico:
Princípio:
Peroxidação do sulfato de titânio a persulfato com H2O2 concentrada e determinação espectrofotométrica por absorção molecular ou diretamente no extrato sulfúrico por absorção atômica. O teor de TiO2 no solo serve como indicativo de solo desenvolvido a partir de rocha básica.
Procedimento:
- Pipetar 25ml do extrato sulfúrico (método 13), colocar em balão aferido de 50ml e adicionar 4ml de ácido sulfúrico 1:1.
- Adicionar, gota a gota, solução de permanganato de potássio até persistência de coloração violeta, e aquecer até próximo à fervura (80 a 90oC), durante 5 minutos; caso a coloração desapareça, adicionar mais algumas gotas de permanganato.
- Juntar, gota a gota, solução de ácido oxálico a 10%, até completo descoloramento, evitando excesso deste redutor.
- Deixar esfriar, juntar 1 ml de ácido fosfórico concentrado, e 7 gotas de H2O2. Agitar e completar o balão com água.
- Colocar 0,5, 1 e 2ml da solução padrão de TiO2 (1 g/litro) em balão aferido de 50ml, adicionar ± 20ml de água, 6 ml de H2SO4 1:1, 1ml de H3PO4 a 50% e 7 gotas de perhidrol. Completar o volume.
- Depois de algumas horas (a coloração é estável durante alguns dias) medir a absorvância a 430 mµ e anotar a leitura.
- Medir em absorvância. Anotar a leitura correspondente a cada padrão.
Cálculo:
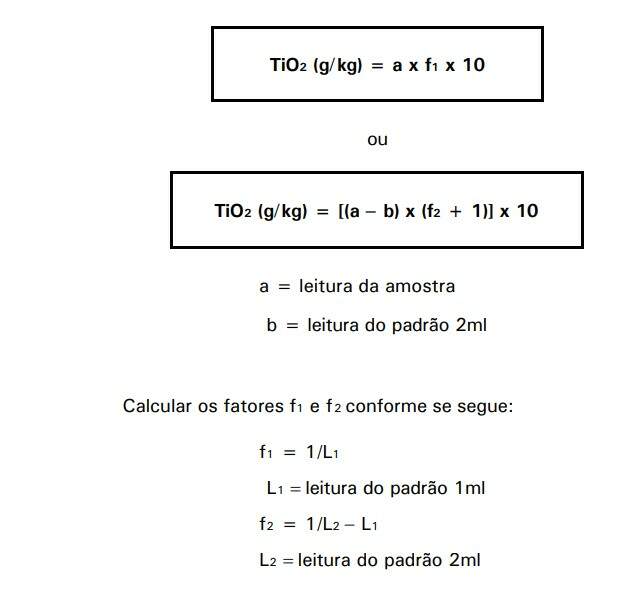
Observação:
Usar o fator f2 quando a leitura da amostra > a leitura do padrão 2ml.
Os numeradores das expressões relativas aos fatores f1 e f2 são obtidos relacionando-se amostra e padrão.
Os resultados deverão ser multiplicados por 2.
Reagentes:
Ácido sulfúrico 1:1 - adicionar 500ml de H2SO4 concentrado a idêntico volume de água, contida em proveta de 1 litro.
Permanganato de potássio - empregar solução concentrada de KMnO4.
Ácido oxálico a 10% - dissolver 100g do produto p.a. em 600ml de água contida em proveta de 1 litro, agitar e completar o volume.
Perhidrol ou água oxigenada - utilizar o produto p.a.
Solução padrão de TiO2 (1 g/litro).
- Pesar 1g de TiO2 p.a., colocar em bécher de 400ml e adicionar 50ml de solução de H2SO4 1:1.
- Aquecer no banho de areia em capela, até o desprendimento de SO3 Adicionar 250ml de água, agitando continuamente com bastão de vidro para evitar hidrólise e ferver durante alguns minutos.
- Deixar esfriar, transferir para balão aferido de 1 litro e completar o volume (filtrar se necessário).
- Pipetar 100ml, colocar em bécher de 250ml, aquecer e adicionar, gota a gota, a solução de hidróxido de amônio 1:1 até ligeiro excesso, usando azul de bromotimol como indicador.
- Ferver durante 5 minutos, filtrar em papel de filtro sem cinzas e lavar o precipitado com água quente, até que uma pequena porção do filtrado não apresente reação de sulfatos pelo cloreto de bário a 10%.
- Colocar o papel de filtro em cadinho de porcelana na estufa, durante 1 a 2 horas, e depois em mufla, para calcinar até 800 - 900oC, deixando nessa faixa de temperatura durante 1 a 2 horas.
- Esfriar em dissecador e pesar com aproximação de 0,0001g.
- Efetuar esta determinação em duplicata e determinar a concentração exata da solução de TiO2 em função do peso do resíduo depois de calcinado, de acordo com a seguinte expressão:

Equipamento:
- EAM.
- EAA.
5 Manganês no Extrato Sulfúrico/ Fósforo no Extrato Sulfúrico/ Relações Moleculares Ki e Kr/ Relação Molecular AL²O³ / Fe²O³:
Manganês no Extrato Sulfúrico:
Princípio:
Peroxidação do manganês com periodato de potássio e leitura espectrofotométrica por absorção molecular ou diretamente do extrato sulfúrico por absorção atômica.
Procedimento:
- Pipetar alíquota de 20ml do extrato sulfúrico para bécher de 100ml, adicionar 1ml de ácido nítrico concentrado e aquecer até destruição da matéria orgânica.
- Adicionar 1ml de ácido fosfórico concentrado e 0,2 a 0,3g (1 pitada) de periodato de potássio.
- Acrescentar 10ml de água e ferver por cinco minutos.
- Deixar esfriar, transferir para balão de 100ml e completar com água.
- Pipetar 0,1, 0,2, 0,5 e 1ml de solução padrão (fixanal) 0,1 N de permanganato de potássio para balão de 100ml.
- Adicionar a cada um dos padrões a mesma quantidade de ácido nítrico, fosfórico e periodato de potássio que foi adicionada às amostras.
- Completar o volume dos balões a 100ml com água e deixar em repouso.
- Proceder à leitura em absorvância, após 1 hora, em espectrofotômetro a 550mm.
Cálculo:
Calcular a percentagem do MnO pela seguinte expressão:
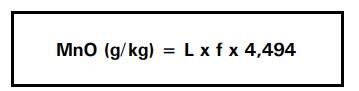
Determinar os fatores de conversão de leituras para teores de KMnO4 na amostra em função dos padrões do KMnO4, conforme descrito abaixo.

Os numeradores das expressões relativas aos fatores f1 e f2 são obtidos relacionando-se amostra e padrão.
Equipamento:
EAM
EAA.
Fósforo no Extrato Sulfúrico:
Princípio:
Solubilização das formas fosfatadas minerais e orgânicas pelo H2SO4 1:1. O fósforo contido no extrato sulfúrico representa a concentração total deste elemento.
Procedimento:
- Pipetar 10ml do extrato sulfúrico para balão de 50ml.
- Adicionar 10ml de solução de P total concentrado.
- Juntar água até aproximadamente 35ml e uma “pitada” (15mg) de ácido ascórbico.
- Agitar até completa dissolução do ácido ascórbico e completar o volume.
- Pipetar 0,5 - 1 - 2ml de solução padrão de fósforo contendo 50mg/l para balões aferidos de 50ml. Juntar um pouco de água e 10ml do reagente concentrado do fósforo assimilável (compensação de acidez com as amostras provenientes do ataque sulfúrico) e uma “pitada” (15mg) de ácido ascórbico. Agitar e completar o volume com água.
- Determinar as leituras em espectrofotômetro a 660 mu.
Cálculo:

Observação: 0,125 g de P2O5 foi obtido relacionando-se amostra e padrão.
Reagentes:
Solução de molibdato de amônio - em balão de 1 litro, vidro Pyrex, contendo ± 500ml de água, juntar 2g de subcarbonato de bismuto e, rapidamente, 100ml de H2SO4 concentrado. Com o calor desenvolvido, o sal de bismuto se dissolve. Esfriar, adicionar a esta solução outra de 20g de molibdato de amônio em 200ml de água. Completar o volume.
Solução padrão de P2O5 contendo 50 mg de P2O5 por litro - dissolver 0,0958g de KH2PO4 em água destilada, juntar 3ml de H2SO4 concentrado e completar a 1 litro.
Equipamento:
- EAM
Relações Moleculares Ki e Kr:
Cálculo:
O Ki é calculado em função dos valores expressos em % de SiO2 e Al2O3, divididos pelos seus respectivos pesos moleculares. Os resultados obtidos nos itens 14.3 e 16.3 devem ser divididos por 10.

Relação Molecular AL²O³ / Fe²O³:
Cálculo:
Obtida em função dos valores expressos em percentagens de Al2O3 e Fe2O3, divididos pelos seus respectivos pesos moleculares, pela seguinte expressão simplificada:
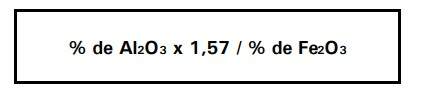
6 Ferro, Alumínio, Manganês e Sílica Extraíveis/ Sais Solúveis/ Equivalente de Carbonato de Cálcio
Ferro, Alumínio, Manganês e Sílica Extraíveis
Estas análises compreendem:
- compostos de ferro, alumínio e manganês livres no solo extraídos por solução de citrato-ditionito-bicarbonato;
- compostos de ferro, alumínio e sílica amorfos extraídos por solução de oxalato ácido de amônio;
- ferro e alumínio de ligações orgânicas extraídas por solução de pirofosfato.
Método do citrato-ditionito-bicarbonato (CBD)
A amostra é aquecida em uma solução complexante tamponada de citrato/bicarbonato, a qual é adicionada ditionito de sódio em pó como agente redutor. O ferro, alumínio e manganês são determinados no extrato pelo AAS.
Procedimento:
- Pesar 1 a 2g de solo e colocar em tubo de centrífuga de 100ml. Tem-se como critério pesar 1g para amostras com teores de Fe2O3 total (ferro do ataque sulfúrico) acima de 5% e 2g para abaixo de 5%.
- Adicionar 40 ml da solução de citrato tribásico de sódio biidratado 0,3M e 5 ml de solução de bicarbonato de sódio M.
- Aquecer em banho-maria à temperatura entre 75oC e 80oC. Precaução: a temperatura não deve exceder a 80oC (precipitação do enxofre).
- Juntar 1g de ditionito de sódio em pó, agitar constantemente por 1 minuto e ocasionalmente por 5 minutos. Uma segunda porção de 1g de ditionito é adicionada agitando-se posteriormente. Uma terceira porção de 1g é adicionada com agitação ao final do segundo período de 5 minutos.
- Adicionar 10ml de solução saturada de NaCl e manter o aquecimento em banho-maria por algum tempo.
- Deixar esfriar e centrifugar durante 10 minutos a 2.000 rpm.
- Transferir o líquido sobrenadante para balão de 250ml e repetir a operação até se obter um líquido sobrenadante claro. Completar o volume com água.
Cálculo:

Reagentes:
Solução de citrato de sódio 0,3M - dissolver 88,23g de citrato de sódio bihidratado em 1 litro de água.
Solução de bicarbonato de sódio 1M - dissolver 84,01g em 1 litro de água. Ditionito de sódio - pó.
Soluções padrão de Fe, Al, e Mn - diluir ampolas padronizadas conforme instruções.
Equipamento:
- Banho-maria.
- Centrífuga.
- EAA.
Método do oxalato ácido de amônio:
Baseia-se na afinidade do oxalato em meio ácido para formação de complexos coloidais após a dissolução dos óxidos e oxi-hidróxidos amorfos do solo (Fe, Al, Si), permanecendo inatacados os argilo-minerais cristalinos. O Fe, Al e Si são determinados no extrato pelo EAA por espectrofotometria de absorção atômica.
Procedimento:
- Pesar 0,5g de solo para tubo de centrífuga.
- Adicionar 20ml de oxalato ácido de amônio 0,2M pH 3,0.
- Agitar por 4 horas no escuro.
- Centrifugar por 15 minutos a 2.000 rpm.
- Cuidadosamente, passar o líquido sobrenadante para vidro escuro de 100ml e reservar para as determinações de Fe, Al e Si.
Cálculo:


Reagentes :
Oxalato ácido de amônio 0,2 M pH=3 - dissolver 28,4g do oxalato de amônio e 12,6g do ácido oxálico em 1 litro de água. Misturar 700ml do sal com 530ml do ácido. Ajustar o pH=3 com ácido oxálico ou NH4OH.
Equipamentos:
- Agitador mecânico.
- EAA.
Método do pirofosfato de sódio:
Princípio:
Os complexos de ferro e alumínio com a matéria orgânica são extraídos com pirofosfato de sódio, permanecendo inatacáveis as formas inorgânicas amorfas e cristalinas.
Procedimento:
- Triturar 5g de amostra no gral e passar por tamiz de 100 mesh.
- Pesar 0,3g de amostra (100 mesh) em tubos de centrífuga (1g p/amostra com pouco Fe e Al).
- Adicionar 30ml de solução de pirofosfato de sódio 0,1 M. Vedar e agitar por uma noite ou agitar por 2h, deixar em repouso por uma noite e agitar novamente por 2 horas.
- Centrifugar a 20.000 rpm por 10 minutos. Se não dispuser de supercentrífuga, adicionar 0,5ml de solução super floc 0,1%, e centrifugar por 15 minutos a aproximadamente 3.500 rpm.
- Decantar o sobrenadante claro em um frasco e armazenar em “freezer” para futuras análises.
- A determinação dos elementos é feita por absorção atômica.
Cálculo:


Reagentes:
Pirofosfato de sódio 0,1 M - dissolver 44,6g de Na4P2O7.10H2O em água e elevar a 1 litro.
Super floc (N - 100).
Equipamento:
- Supercentrífuga.
Sais Solúveis:
Princípio:
Determinação dos sais solúveis nos solos pela medição de cátions e ânions no extrato aquoso. O procedimento descrito é o do extrato obtido na pasta de saturação. A salinidade do solo é estimada pela condutividade elétrica do extrato.
Preparação do extrato de saturação:
Procedimento:
- Pesar 100 a 200g de solo e colocar em bécher de plástico de 400ml.
- Adicionar água contida em proveta de 50ml, em quantidade inicial de 25ml para solos arenosos e 50ml para os demais.
- Amassar a amostra com espátula de aço inoxidável e continuar a adição de água, pouco a pouco, de preferência por meio de bureta de 50ml.
- Dar como concluída essa operação quando a massa do solo apresentar aspecto brilhante ou espelhante, ou quando uma pequena quantidade de água adicionada já não é mais absorvida pela massa do solo, ou ainda, quando a pasta deslizar suavemente na espátula.
- Anotar a quantidade de água utilizada e deixar a amostra em repouso durante 4 horas ou uma noite.
- Decorrido esse tempo, verificar se a massa do solo apresenta excesso ou falta de água; no primeiro caso adicionar mais 50g de terra fina e repetir a operação de saturação; no segundo caso adicionar mais água até completar a saturação. Determina-se então a percentagem de saturação:

- Transferir a pasta saturada para um funil de Buckner contendo papel de filtro e adaptado a um kitasato de 500ml.
- Aplicar a sucção e coletar o filtrado.
- Transferir o extrato para depósito de plástico com tampa e anotar o número da amostra.
Observação:
Adicionar 1 gota de solução de hexametafosfato de sódio a 1% para cada 25ml de extrato, quando se vai determinar os íons carbonatos e bicarbonatos, para evitar a precipitação do carbonato de cálcio durante o repouso da amostra. A quantidade de solo a ser usada depende das determinações a serem feitas, entretanto, para solos de textura média, 250g são suficientes para se obter uma quantidade de extrato razoável. A pasta não deve acumular água na superfície, perder seu brilho ou endurecer durante o repouso; especial cuidado se deve ter quando se trata de Solos Orgânicos, muito argilosos ou sódicos.
Equipamento:
- Funil buckner.
- Bomba a vácuo.
Condutividade elétrica:
Procedimento:
- Utilizar o extrato de saturação obtido (ver item 23.2.1) e um condutivímetro de leitura direta.
- Medir a temperatura do extrato e ajustar o aparelho para essa temperatura; ligar o aparelho com certa antecedência e aferir a leitura do mesmo com solução de KCl 0,01 N (condutividade de 1,4 mS/cm ).
- Lavar a célula de condutividade com água 2 a 3 vezes e encher a mesma com o extrato de saturação.
- Fazer a leitura direta de mS/cm.
Observação:
Lavar bem a célula com água destilada depois de cada determinação para evitar interferência nos resultados.
Quando necessário (solos com predominância de argilo-expansivos), recorrer ao seguinte procedimento indireto utilizando o solo e o extrato aquoso de 1:1 por filtração simples:
- pesar 50g de solo para erlenmeyer de 100ml e adicionar 50ml de água;
- agitar esporadicamente e deixar em repouso durante uma noite;
- filtrar em papel de filtro comum;
- utilizar o filtrado, mesmo sendo turvo e medir a condutividade elétrica expressa em mS/cm;
- a percentagem de água na pasta saturada é obtida conforme especificado no item 23.2.1.
Reagente:
Solução de cloreto de potássio 0,01 N - pesar 0,7456g do sal previamente seco em estufa a 110oC, dissolver em água e completar o volume para 1 litro. A CE dessa solução é de 1,4 mS/cm.
Equipamento:
- Condutivímetro digital.
Cátions solúveis:
Princípio:
O cálcio e magnésio solúveis são determinados pelo AAS e o sódio e potássio pelo fotômetro de chama nos extratos diluídos. Interferências nas determinações pelo AAS são eliminadas pela adição de lantânio.
Procedimento:
Ca e Mg solúveis:
- Diluir uma solução padrão de Ca 1.000mg/l para 250mg/l; pipetar 50ml para balão volumétrico de 200ml e completar o volume com água.
- Diluir uma solução padrão de Mg 1.000mg/l para 25mg/l; pipetar 25 ml para balão volumétrico de 1l e completar o volume com água.
- Pipetar uma série de 0-5-10-15-20-25ml para balão volumétrico de 250 ml das soluções de Ca 250mg/l e Mg 25mg/l respectivamente.
- Em cada amostra adicionar 2.5ml da solução de lantânio a 1%. Completar o volume com água.
Na solúvel:
- Passar o extrato de saturação no fotômetro de chama.
- Proceder à leitura, diluindo o extrato quando a leitura ultrapassar a escala do aparelho.
K solúvel:
- Passar o extrato de saturação no fotômetro de chama.
- Proceder à leitura e diluir o extrato quando a leitura ultrapassar a escala do aparelho.
Cálculos:
O sal solúvel no solo é expresso de duas formas: - concentração de cátions no extrato, expresso em cmolc /l; - concentração de cátions no solo, expresso em cmolc /kg. A concentração do Ca e Mg no extrato é obtido por:

Observação:
Obter o fator f para o Na+ em função dos valores obtidos com os padrões de 0,01 - 0,02 - 0,03 e 0,04 cmolc /l Na+ na mesma forma indicada no item 4.3.6, adaptando-o para cmolc /l. Geralmente é necessário proceder a várias diluições para tornar possível a leitura no aparelho.
O fator f para o potássio é obtido da mesma maneira indicada no item 4.3.5; usualmente as diluições para o potássio são bem menores do que para o sódio.
O teor de cátions no solo é obtido por:


Reagentes:
Solução padrão de KCl e NaCl (0,1 cmolc /l ) - pesar 0,0746g de KCl e 0,0585g de NaCl previamente secos em estufa e dissolver em solução de HCl 0,05 N até completar o volume de 1 litro.
Solução padrão de K+ e Na+ - pipetar para balões aferidos de 500ml as seguintes quantidades da solução anterior: 50, 100, 150 e 200ml; completar o volume com solução de HCl 0,05 N; transferir para frascos e anotar no rótulo as concentrações de 0,01 - 0,02 - 0,03 e 0,04 cmolc /l respectivamente.
Passar essas 4 soluções no fotômetro e anotar os valores das leituras, sendo recomendável que a leitura do padrão de 0,02cmolc /l de K + ou Na+ represente exatamente a metade da escala do galvanômetro.
Traçar o gráfico leitura x concentração e determinar o fator fk.
Solução padrão de sódio - ver item 4.3.5.4.
Equipamento:
- Espectrofotômetro de absorção atômica.
- Fotômetro de chama.
Relação de adsorção de sódio (RAS)
Calculado em função dos teores de Na, Ca e Mg+no extrato de saturação:

Ânions solúveis
Determinações dos carbonatos, bicarbonatos, cloretos e sulfatos.
Carbonatos:
Princípio:
Determinação por acidimetria com H2SO4 em presença da fenolftaleína como indicador.
Procedimento:
- Pipetar alíquota de 10 a 25ml do extrato de saturação e colocar em erlenmeyer de 125ml.
- Adicionar 3 gotas de fenolftaleína e titular com solução de H2SO4 0,025 N, preferivelmente contida em microbureta de 10ml.
- Anotar o número de ml gastos; caso a extração não apresente coloração vermelha com a fenolftaleína, o valor de CO3 - - é nulo
Observação:
A titulação deve ser feita em local bem iluminado (luz fluorescente), sendo o erlenmeyer colocado sobre azulejo branco; uma mesma quantidade de água deve ser colocada em um erlenmeyer, assim como o mesmo número de gotas do indicador, para comparação com a amostra; esta mesma alíquota é usada para determinação dos bicarbonatos.
Cálculo:

Reagentes:
Solução de fenolftaleína a 1% - dissolver 1g de fenolftaleína em 100ml de álcool etílico a 60%.
Ácido sulfúrico 0,025 N - preparar a partir de solução normal ou decinormal de H2SO4.
Bicarbonatos:
Princípio
Determinação por acidimetria com H2SO4 no extrato após determinação do carbonato em presença de vermelho de metila como indicador.
Procedimento:
- Após a titulação dos carbonatos, adicionar 3 gotas do indicador metil-orange e continuar a adição do ácido sulfúrico 0,025 N contido na bureta, até viragem da cor rósea para alaranjada.
- Utilizar uma prova em branco, ou seja, o total usado com a fenolftaleína e com o metil-orange.
Cálculo:

Observação:
Esta mesma alíquota pode ser usada para determinação dos cloretos.
Reagentes:
Indicador metil-orange 0,01% - pesar 0,01g do indicador, dissolver em água destilada e completar o volume para 100ml.
Solução de H2SO4 0,025 N - preparada a partir de solução normal ou decinormal do ácido.
Cloretos:
Princípio:
Determinação volumétrica com AgNO3 em presença de K2Cr2O4 como indicador.
Procedimento:
- Pipetar alíquota de 1 a 25ml, do extrato de saturação; dependendo do teor salino da amostra, colocar em cápsula de porcelana de 150ml e diluir para volume de 25ml.
- Adicionar 5 gotas de cromato de potássio e agitar bem com bastão de vidro.
- Titular com solução de AgNO3 0,05 N até a formação de coloração vermelha persistente.
Cálculo:

Observação:
Empregar microbureta âmbar de 10ml. A titulação não deve ir além dos 12ml de AgNO3, sendo feitas as diluições necessárias para que fique numa faixa de 2 a 8ml. Paralelamente deve ser feita uma prova em branco com o cromato de potássio para verificação de viragem e do volume de AgNO3 gasto, o qual participará do cálculo.
Para determinação de cloretos em baixas ou altas concentrações, o método complexiométrico do nitrato mercúrico em meio ácido através da formação do complexo azul/violeta Hg-difenilcarbazona é considerado excelente.
Reagentes:
Solução de cromato de potássio 5% - pesar 5g do K2CrO4 e dissolver em 50ml de água destilada; adicionar gota a gota solução de AgNO3 0,05N, até formação de precipitado permanente; filtrar e diluir para 100ml.
Solução de nitrato de prata 0,05 N - pesar exatamente 8,495g de AgNO3 puro e dissolver em água destilada contida em balão aferido de 1 litro, agitar e completar o volume; guardar em vidro escuro.
Sulfatos:
Princípio:
Precipitação do sulfato com BaCl2 e determinação gravimétrica.
Procedimento:
- Pipetar alíquota de 25ml do extrato de saturação, colocar em bécher de 250ml e adicionar 100ml de água.
- Juntar 3 gotas de metil-orange e 1ml de ácido clorídrico concentrado.
- Colocar em placa elétrica e, quando se iniciar a ebulição, adicionar a solução de cloreto de bário até ligeiro excesso, agitando com bastão de vidro, energicamente, para formação do precipitado.
- Colocar em banho-maria até reduzir o volume para aproximadamente 50ml.
- Deixar esfriar e filtrar em papel de filtro sem cinzas, lavando com água quente até que uma pequena porção do filtrado não apresente reação pelo nitrato de prata.
- Colocar o papel de filtro, dobrado, em cadinho de porcelana recém pesado, levar para forno mufla de calcinar até temperatura de 750°C.
- Deixar esfriar em dessecador e pesar com aproximação de 0,0001g.
Cálculo:

Observação:
Outros métodos podem ser empregados para determinação dos sulfatos, especialmente quando os teores destes íons são baixos, entretanto este método é considerado como o mais preciso.
Reagentes:
Solução de BaCl2 a 10% - pesar 100g de BaCl2 2H2O, dissolver em água e completar o volume para 1 litro. Indicador metil-orange 0,1% - dissolver 0,1g do indicador em 100ml de água.
Equivalente de Carbonato de Cálcio:
Princípio:
Ataque da amostra com excesso de solução padrão de HCl e titulação do excesso de ácido com solução de NaOH padrão. A diferença entre os cmolc /l adicionados e os titulados representa o percentual de CaCO3 na amostra.
Procedimento:
- Pesar 5 a 25g de solo, colocar em cápsula de porcelana de 200ml e adicionar 50ml de HCl 0,5 N por meio de pipeta.
- Aquecer por 5 minutos ou colocar em banho-maria durante 15 minutos.
- Deixar esfriar, adicionar um pouco de água e 3 gotas de fenolftaleína.
- Titular com solução de NaOH 0,25 N.
Observação:
A quantidade de amostra a pesar é definida em função do grau de efervescência que a amostra apresenta quando é umedecida com HCl 30%. A reação pode ser fraca, moderada ou forte.
Caso haja dificuldade na titulação da solução com a amostra de solo, filtrar, lavar e proceder à titulação no total ou numa alíquota. Esta determinação inclui também outros carbonatos.
Cálculo:
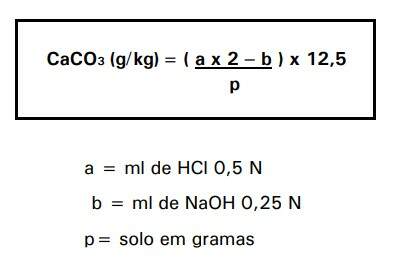
Reagentes:
Solução de HCl 0,5 N (padronizada) - preparar a partir de solução normal do ácido.
Solução de NaOH 0,25 N - preparar a partir de solução normal de NaOH e determinar sua normalidade exata com o ácido.
Fenolftaleína 1% - dissolver 1g do indicador em 100ml de álcool etílico 95%. 24.5
Equipamento:
- Bureta digital.
7 Necessidade de Gesso/ Enxofre/ Microelementos/ Fósforo Assimilável/ Ataque Triácido:
Necessidade de Gesso
Princípio:
Quantidade de gesso necessária para proporcionar condições adequadas de recuperação e uso de solos salinos. Determina-se dosando-se o Ca++ + Mg++ no extrato resultante do equilíbrio do solo com solução saturada de CaSO4, subtraindo-se esse valor do valor de Ca++ titulados na solução de CaSO4.
Procedimento:
- Colocar 5g de solo em erlenmeyer de 150ml e adicionar, com auxílio de pipeta, 100ml de solução saturada de sulfato de cálcio.
- Fechar o erlenmeyer e agitar várias vezes ou utilizar agitador circular durante 5 minutos.
- Filtrar e pipetar alíquota do filtrado claro e dosar o Ca++ e o Mg++ pelo EAA. · Calcular a concentração do Ca++ e do Mg++ em cmolc /l.
Cálculo:

Reagente:
Solução saturada de sulfato de cálcio - pesar 5g do CaSO42H2O, colocar em garrafa contendo um litro de água. Agitar várias vezes ou utilizar agitador circular durante 10 minutos. Filtrar e pipetar 5 ml do filtrado límpido; dosar o cálcio nessa alíquota e calcular a concentração desse íon em cmolc /l, que deve ser da ordem de 28 cmolc /l Ca++.
Equipamento:
- Agitador mecânico circular.
- Bureta digital.
Enxofre:
Princípio:
Ataque da amostra com HCl 1:1, precipitação com BaCl2, calcinação do BaSO4 e determinação gravimétrica do precipitado. Esta determinação aliada ao baixo pH serve de referência para a caracterização de solos tiomórficos.
Procedimento:
- Pesar 10g de solo e colocar em erlenmeyer de 500ml.
- Adicionar 50ml de HCl 1:1 e ferver durante meia hora, usando condensador de refluxo para evitar evaporação.
- Deixar esfriar, adicionar 50ml de água destilada e filtrar para balão aferido de 250ml, completando o volume.
- Pipetar 50ml do extrato obtido para bécher de 250ml e adicionar 10 gotas de HNO3 concentrado.
- Aquecer o extrato até início de ebulição, adicionando em seguida, gota a gota, 10ml de solução de BaCl2 10%, agitando com bastão de vidro até completa precipitação do sulfato (SO4 - - ).
- Filtrar em papel de filtro isento de cinzas, lavando com água quente até que uma pequena porção do filtrado não apresente reação com AgNO3 5%. · Colocar o precipitado retido no papel de filtro, bem dobrado, em cadinho de platina ou porcelana recém-tratado, levar para forno mufla e calcinar até temperatura de 750°C (rubro).
- Deixar esfriar em dessecador contendo sílica-gel ou CaCl2 sólido e pesar com aproximação de 0,0001g.
Observação:
O ataque clorídrico 1:1 é empregado no Laboratório de Química do CNPS em lugar da fusão do solo com Na2CO3 por se tratar de método mais simples e equivalente a este.
Cálculo:

Reagentes:
Solução de HCl 1:1 - medir 500ml de HCl concentrado em proveta graduada e completar o volume a 1l com água.
Solução de BaCl2 10% - pesar 100g do sal e dissolver em 1l de água.
Solução de AgNO3 5% - pesar 5g do sal e dissolver em 100ml de água.
Equipamento:
Forno mufla com termostato e regulagem de temperatura até 1.200ºC.
Microelementos:
Princípio:
Extração dos microelementos através de solução quelante (DTPA) ou solução mista de ácidos. A determinação dos elementos é feita por espectrofotometria de absorção atômica.
Procedimento:
Duas técnicas de extração são descritas sucessivamente.
Método DTPA:
- Pesar 10g de solo e colocar em erlenmeyer de 125ml.
- Adicionar 20ml da solução extratora DTPA.
- Agitar por 2h em agitador mecânico e filtrar imediatamente a suspensão. No filtrado determinar os micronutrientes por espectrofotometria de absorção atômica.
Método de Mehlich modificado:
- Pesar 10g de solo e colocar em erlenmeyer de 125ml.
- Adicionar 50ml de solução extratora de Mehlich.
- Agitar por 5 minutos em agitador mecânico e filtrar imediatamente a suspensão. No filtrado determinar os micronutrientes por espectrofotometria de absorção atômica.
Reagentes:
Solução extratora DTPA - pesar 14,92g de TEA, 1,967g de DTPA e 1,47g de CaCl2.2H2O P.A. Colocar em balão volumétrico de 1 litro, contendo 900ml de água. Dissolver, ajustar o pH até 3 com HCl 1M e completar.
Soluções padrão Cu, Zn, Fe, Mn - diluir ampolas padronizadas conforme instruções, preparando padrões apropriados para cada elemento.
Solução extratora mista: HCl 0,05 N + H2SO4 0,025 N - colocar em balão volumétrico de 1 litro contendo 500 ml de água, 4.0ml de HCl p.a (d = 1.19) e 0,7ml de H2SO4 p.a (d = 1,84). Completar o volume.
Equipamento:
- EAA.
Fósforo Assimilável:
Princípio:
Fração do teor total de fósforo no solo, correspondente ao teor utilizado pelas plantas. Formação de complexo fósforo-molíbdico de cor azul obtido após redução do molibdato com ácido ascórbico e determinação por EAM.
Procedimento:
- Colocar 5g de solo em erlenmeyer de 125ml. Adicionar 50ml de solução extratora (HCl 0,05 N e H2SO4 0,025 N).
- Agitar durante 5 minutos em agitador circular horizontal..
- Deixar decantar durante uma noite, tendo antes o cuidado de desfazer os montículos que se formam no fundo dos erlenmeyers. · Pipetar, sem filtrar, 25ml do extrato e passar para recipiente plástico.
- Pipetar 5ml desse extrato e colocar em erlenmeyer de 125ml; deixar o restante para determinação de K+ e Na+.
- Adicionar 10ml de solução ácida de molibdato de amônio diluída e aproximadamente 30mg de ácido ascórbico em pó, como redutor.
- Agitar durante 1 a 2 minutos no agitador circular horizontal.
- Deixar desenvolver a cor durante uma hora. Em seguida, fazer a leitura da densidade ótica no fotocolorímetro, usando filtro vermelho (comprimento de onda de 660 mµ)
Observação:
No caso de a amostra possuir elevada concentração de fósforo, diluir a solução até que seja possível a leitura no aparelho; para maior facilidade operacional, essa diluição pode ser feita adicionando-se quantidades iguais a 15ml de água, ou seus múltiplos.
Cálculo:

Determinação do fator Fp:
- colocar 10ml de cada solução padrão diluída em erlenmeyers de 125ml. Adicionar 20ml da solução ácida de molibdato de amônio diluída e uma “pitada” de ácido ascórbico. Proceder da mesma forma indicada para a determinação do fósforo no extrato de solo; anotar as leituras (em absorvância) correspondentes a cada padrão. O fator Fp é o coeficiente angular da reta que se obtém, cruzando-se os valores de concentração de fósforo (mg/kg) dos padrões no eixo das abcissas e as respectivas leituras no eixo das ordenadas.
- para a obtenção direta da concentração de P (mg/kg) no solo, o fator Fp deve ser multiplicado por 10, considerando que a concentração de fósforo na amostra sofreu diluição de 1:10 na extração.
Reagentes:
Soluções extratoras - HCl 0,05 N e H2SO4 0,025 N - adicionar 40ml de ácido clorídrico p.a. (d = 1,19) e 7,6ml de ácido sulfúrico p.a. (d = 1,84) em aproximadamente 5 litros de água, contidos em balão aferido de 10 litros; agitar e completar o volume com água. Pode-se usar baldes plásticos previamente aferidos.
Solução ácida de molibdato de amônio (concentrada) - colocar 2g de subcarbonato de bismuto em aproximadamente 250ml de água contida em balão aferido de 1 litro; juntar, rapidamente, 150ml de ácido sulfúrico concentrado p.a. Verificar se todo o sal de bismuto foi dissolvido. Deixar Solução ácida de molibdato de amônio (concentrada) - colocar 2g de subcarbonato de bismuto em aproximadamente 250ml de água contida em balão aferido de 1 litro; juntar, rapidamente, 150ml de ácido sulfúrico concentrado p.a. Verificar se todo o sal de bismuto foi dissolvido.
Deixar esfriar e adicionar solução recém-preparada de molibdato de amônio (20g para 200ml de água). Agitar e completar o volume com água.
Solução ácida de molibdato de amônio (diluída) - colocar 300ml de solução concentrada em balão aferido de 1 litro e adicionar água até completar o volume. Homogeneizar e guardar em frasco escuro.
Solução padrão de fósforo (50 mg/l de P) - pesar 0,2195g de KH2PO4 p.a., previamente seco em estufa a 105oC e dissolver em 3ml de H2SO4 concentrado e completar o volume com água.
Soluções padrão de fósforo (diluídas) - pipetar 10, 20, 30 e 40ml de solução padrão de 25 mg/l para balões aferidos de 250ml e completar o volume com a solução extratora; as quatro soluções possuem concentrações de 0,5 1 e 2mg/l de P; guardar em frascos tampados, com indicação das concentrações nos rótulos.
Equipamento:
- EAM.
Ataque Triácido:
Princípio:
Minerais e compostos orgânicos componentes do solo são totalmente solubilizados através da digestão com uma mistura ternária de ácidos fortes e concentrados (HNO3+HF+HClO4), liberando seus elementos constituintes posteriormente determinados por métodos complexiométricos ou espectrofotométricos (EAA, EAM).
Procedimento:
- Pesar 1g de solo e adicionar 2ml de HNO3 e 2ml de HClO4. Usar bécher de teflon ou cadinho de Pt em banho de areia. Aquecer até evaporação completa. Deixar e esfriar.
- Adicionar 3ml de HClO4 e 5ml de HF. Deixar em contato durante a noite; aquecer até evaporação completa, deixar esfriar.
- Repetir item acima.
- Adicionar 3ml de HClO4. Aquecer até evaporação completa. Deixar esfriar.
- Dissolver e suspender o resíduo com 8ml de água e 3ml de HCl. Aquecer até que a solução fique límpida. Transferir para balões de 50ml e colocar em estufa (70oC) durante a noite. Deixar esfriar e completar o volume.
- Determinar o Fe, Al e outros elementos por espectrofotometria de absorção atômica, preparando padrões apropriados para cada elemento.
Reagentes:
HClO4 concentrado.
HNO3 concentrado.
HCl concentrado.
HF concentrado.
Equipamento:
- EAA.
8 Expressão dos Resultados: