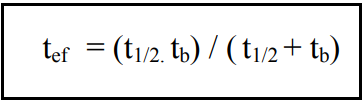Princípios Básicos de Segurança e Proteção Radiológica
Noções Básicas em Auxiliar de Radiologia
1 ESTRUTURA DA MATÉRIA:
A questão da estrutura da matéria vem recebendo atenção de filósofos e cientistas desde os primórdios da civilização. Sob o ponto de vista de proteção radiológica, a matéria pode ser considerada como constituída de partículas fundamentais cujas propriedades de interesse são a massa e a carga elétrica. Neste contexto, as três partículas importantes para a compreensão da estrutura e propriedades da matéria são os elétrons (e), os prótons (p) e os nêutrons (n). A estas, pode ser acrescentado o fóton, tipo especial de partícula associada à radiação eletromagnética. Partículas mais elementares como léptons e quarks fogem ao escopo desta publicação. O elétron já era conhecido desde o século dezenove como a unidade de carga elétrica, tendo sua carga negativa o mesmo valor numérico que a do próton, ou seja, 1,6021.10-19 C. O nêutron não possui carga elétrica e tem uma massa aproximadamente igual à do próton. Assim, o núcleo possui uma carga elétrica positiva cujo tamanho depende do número de prótons nele contidos.
Átomo e Estrutura do Átomo:
O átomo é a menor partícula de um elemento que conserva suas propriedades químicas, sendo constituído por partículas fundamentais (prótons, elétrons e nêutrons). Os prótons e os nêutrons encontram-se aglomerados numa região central muito pequena, chamada núcleo, que se mantêm unida mediante forças nucleares fortes, que têm caráter atrativo e são muitas ordens de grandeza superiores à força de repulsão eletrostática existente entre os prótons, a qual tenderia a expulsá-los do interior do núcleo.
A densidade do núcleo é muito elevada, sendo da ordem de milhões de toneladas por centímetro cúbico. Segundo o modelo atômico de Bohr, os elétrons, partículas de massa insignificante frente à massa do núcleo (me ≅ mp/1840) e carga elétrica negativa, movem-se em torno do núcleo, numa região denominada coroa, cujo raio é cerca de dez mil vezes maior que o raio do núcleo.
Como a massa dos elétrons que orbitam em torno do núcleo é muito pequena, é correto considerar o núcleo como um ponto minúsculo no centro do átomo onde está concentrada a maior parte de sua massa. O átomo de um elemento possui uma massa bem definida, cujo valor exato é determinado em relação à massa de um elemento tomado como padrão. Em 1961, por um acordo internacional entre físicos e químicos, foi estabelecida uma escala unificada, tendo sido atribuído o valor exato de 12,000000 para a massa atômica do carbono-12, Assim, nessa escala, uma unidade de massa atômica é igual a 1/12 da massa do átomo de carbono-12, ou seja:

O próton possui uma massa de 1,00759 u.m.a., valor muito semelhante à massa do átomo de hidrogênio, e uma carga positiva igual a 1,6021.10-19 C. O nêutron possui uma massa de 1,00898 u.m.a., valor muito próximo ao da massa do próton, sendo eletricamente neutro. As propriedades químicas dos átomos são definidas pelo número atômico Z (número de unidades de carga positiva existente no átomo), sendo esta a característica que diferencia um elemento de outro. Normalmente, o número de unidades de carga positiva é igual ao da negativa, tornando o átomo eletricamente neutro. Átomos de um elemento podem se combinar com átomos de outro elemento formando moléculas. Por exemplo, quatro átomos de hidrogênio podem se combinar com um átomo de carbono para formar uma molécula de metano, CH4.
Número Atômico, Número de Massa, Massa Atômica e Átomo-Grama:
Número atômico: é o número de prótons que um átomo possui em seu núcleo e que determina suas propriedades químicas, sendo representado pelo símbolo Z. Átomos do mesmo elemento químico possuem o mesmo número atômico, mas não necessariamente a mesma massa, já que podem diferir pelo número de nêutrons.
Número de massa: é o número total de núcleons, ou seja, prótons (Z) + nêutrons (N) existentes em um átomo, sendo simbolizado pela letra A (A=N+Z).
Massa atômica: também conhecida impropriamente por Peso Atômico: é a razão ente a massa média dos átomos do elemento em sua composição isotópica natural e 1/12 da massa do carbono-12. Átomo-grama: é a massa atômica de um elemento, expressa em gramas, e que contêm 6.02 x 1023 átomos desse elemento.
Nuclídeo:
Chama-se nuclídeo qualquer espécie nuclear (núcleo de um dado átomo) definida por seu número atômico (Z), número de massa (A) e estado energético. O símbolo utilizado neste texto para representar os nuclídeos consiste no símbolo químico do elemento (por exemplo, Fe), com o número atômico (Z=26) como subíndice à direita, abaixo e o número de massa (A=57) como supra-índice, à esquerda e acima. Generalizando:
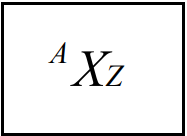
Normalmente, omite-se o número atômico como subíndice, uma vez que o símbolo químico é suficiente para identificar o elemento, por exemplo:
57Fe, 4He, 198Au.
Isótopos:
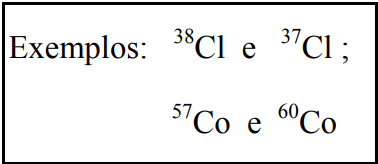
Isótopos são nuclídeos que possuem o mesmo número atômico Z mas massas atômicas (A) diferentes, isto é, os isótopos têm o mesmo número de prótons, porém diferente número de nêutrons (N) e, como conseqüência, diferente número de massa A. O fato dos isótopos possuírem o mesmo número atômico faz com que se comportem quimicamente de forma idêntica.
Isóbaros:
São nuclídeos que possuem o mesmo número de massa e diferentes números atômicos. Tendo números atômicos distintos, comportam-se quimicamente de forma diferente.
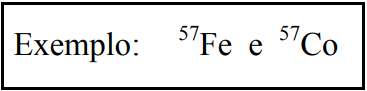
Isótonos:
São nuclídeos que possuem o mesmo número de nêutrons (N).
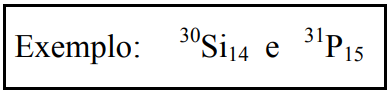
2 Elemento:
Elemento (X) é uma substância que não pode ser decomposta, por ação química normal, em substâncias mais simples . A definição de elemento engloba sua mistura natural de isótopos, uma vez que a maioria dos elementos é formada por vários isótopos. Por exemplo, o estanho natural é formado pela mistura de dez isótopos. Desde os primórdios da Química, tentou-se classificar os elementos conforme as analogias ou diferenças de suas propriedades. Atualmente, a pouco mais de centena de elementos conhecidos está classificada no sistema periódico de Niels Bohr, aprimorado a partir da classificação original proposta por Mendeleiev (1834- 1907). Assim, os elementos são dispostos em fileiras ou períodos e colunas ou grupos, atendendo á estrutura eletrônica de seus átomos, de que dependem as respectivas propriedades, e em ordem crescente de seus números atômicos.
Equivalência entre Massa e Energia:
A unidade de energia conveniente para o estudo dos fenômenos de interação da radiação com a matéria em proteção radiológica é o elétronvolt (simbolizado eV), que corresponde à energia adquirida por um elétron ao atravessar um campo elétrico de 1 volt. Esta unidade expressa um valor muito pequeno e sua relação com unidades macroscópicas e a seguinte:
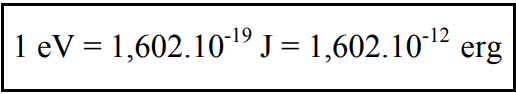
Em 1909, como parte de sua teoria da relatividade especial, Albert Einstein enunciou que o conteúdo total de energia E de um sistema de massa m é dado pela relação:
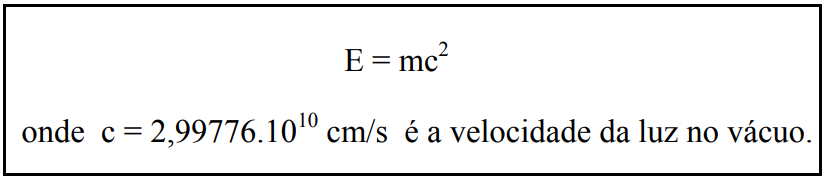
Em quase toda reação nuclear, uma pequena quantidade de massa é transformada em energia, ou vice versa, como por exemplo:

Energia de Ligação dos Núcleos:
As partículas que constituem um núcleo estável são mantidas juntas por forças de atração fortes e, portanto, para separá-las, é necessário realizar trabalho até que elas se mantenham afastadas por uma grande distância. Ou seja, energia deve ser fornecida ao núcleo para separá-lo em seus constituintes individuais, de tal forma que a energia total dos constituintes, quando suficientemente separados é maior do que aquela que têm quando formam o núcleo. Verifica-se que a massa real de um núcleo é sempre menor que a soma das massas dos núcleons que os constituem. Esta diferença de massa, conhecida por defeito de massa, quando convertida em energia, corresponde à energia de ligação do núcleo Tomando, por exemplo, o átomo de 4 He, tem-se:
- massa do núcleo do hélio = 4,00150 u.m.a.
- massa do próton = 1,00728 u.m.a.
- massa do nêutron = 1,00867 u.m.a.
- massa total: 2p + 2n = 4,03190 u.m.a.
Pode ser observado que a diferença entre o valor da soma das massas dos constituintes do núcleo e a massa do núcleo é de 0,03040 u.m.a. Como 1 u.m.a. é equivalente a 931 MeV, temos que a diferença das massas eqüivale a 28,3 MeV, que representa a energia de ligação do núcleo do átomo de Hélio.
Estabilidade Nuclear:
Os nuclídeos podem ser estáveis ou instáveis. Estáveis são aqueles que preservam sua identidade de elemento químico indefinidamente. Instáveis são aqueles que podem sofrer um processo espontâneo de transformação (desintegração) e se converter em um outro nuclídeo. Neste processo, pode haver a emissão de radiação. A energia de ligação é, também uma medida da estabilidade de um núcleo uma vez que pode ser demonstrado que um núcleo não se fragmenta em partículas menores quando sua massa é menor que a soma das massas dos fragmentos.
Números Quânticos:
As características de cada elétron são definidas por quatro números, denominados números quânticos. Os elétrons estão distribuídos em camadas ou níveis energéticos, sendo que, para cada nível, a energia total dos elétrons que o ocupam é exatamente a mesma. O número quântico principal ou fundamental indica, ainda, o número máximo de elétrons possíveis numa camada, sendo que a cada nível energético principal é atribuído um número inteiro (1, 2, 3, 4, 5, 6 ou 7) ou uma letra ( K, L, M, N, O, P ou Q ).
Os níveis de energia das camadas K, L e M para o átomo de tungstênio, por exemplo, são respectivamente 70 keV, 11 keV e 2,5 keV. Estes valores correspondem às energias de ligação dos elétrons em cada um desses níveis. Isto significa ser necessário, no mínimo, 70 keV para remover um elétron localizado na camada K para fora do átomo. À medida que aumenta o número atômico, aumenta o número de elétrons em torno do núcleo. Os novos elétrons irão ocupar as camadas disponíveis, seguindo uma ordem bem estabelecida. Cada camada tem uma capacidade máxima de receber elétrons.
Assim, o nível energético K pode comportar até dois elétrons; o L, oito; o M, dezoito; o N e o O comportam o número máximo de trinta e dois elétrons cada. A camada K é a mais próxima do núcleo e corresponde ao nível energético mais baixo do átomo. Os elétrons em níveis energéticos mais altos têm probabilidade maior de situarem-se em regiões mais afastadas do núcleo do átomo. Os elétrons localizados em órbitas próximas do núcleo, como a órbita K, têm uma certa probabilidade de penetrar na região do núcleo. Este fato faz com que esses elétrons possam participar de certos processos nucleares.
Se uma quantidade de energia for fornecida ao átomo de forma que seus elétrons mais internos sejam removidos para órbitas mais externas ou mesmo arrancados do átomo, um dos elétrons das camadas mais externas irá ocupar a vaga deixada e, nessa transição, o átomo emitirá fótons de energia, conhecidos por radiação característica. Cada nível energético principal subdivide-se em subníveis, que dependem do segundo número quântico, chamado número quântico secundário. O elétron pode se encontrar em qualquer lugar em torno do núcleo, exceto neste. No entanto, há algumas regiões do espaço onde é muito mais provável encontrá-lo que outras.
Chama-se orbital à região do espaço em volta do núcleo onde é mais provável encontrar o elétron ou onde a densidade eletrônica é maior. O número quântico secundário pode ter n valores, começando por 0, sendo o valor máximo n-1, onde n = no quântico principal, e indicam a forma e o tamanho dos orbitais, sendo seu valor representado, também, pelas letras s, p, d, f.... Os orbitais s, por exemplo, têm a forma esférica e seu raio aumenta com o nível energético principal. Uma vez que o elétron é uma partícula carregada e em movimento, ela cria um campo magnético e se constitui em pequeno ímã, razão pela qual se orienta em qualquer campo magnético externo.
As diferentes orientações que um elétron pode tomar vêm definidas pelo terceiro número quântico, o número quântico magnético, cujo valor também é inteiro, positivo, negativo ou nulo. Os elétrons têm um movimento de rotação sobre si mesmos, conhecido por “spin”, que é definido pelo quarto número quântico, o número quântico rotacional ou de spin, que toma os valores –½ e + ½, conforme o sentido de rotação seja horário ou o contrário.
De acordo com o Princípio de exclusão de Pauli, dois elétrons de um mesmo átomo não podem ter os quatro números quânticos iguais; diferirão, pelo menos em um deles. Assim é que dois elétrons no mesmo orbital têm, necessariamente, spins opostos.
3 RADIAÇÃO ELETROMAGNÉTICA:
Os gregos da antiguidade já haviam reconhecido a natureza única da luz, empregando o termo fóton para definir o ‘átomo de luz’, ou seja, a menor quantidade de qualquer radiação eletromagnética que possui a velocidade da luz. O fóton pode ser retratado como um pequeno pacote de energia, também chamado quantum, que se move através do espaço com a velocidade da luz. Embora fótons não possuam massa, eles possuem campos elétricos e magnéticos que se movem continuamente sob a forma de ondas senoidais. As propriedades importantes do modelo senoidal são a freqüência (f) e o comprimento de ondas (λ), sendo a equação da onda expressa simplesmente por:
v = f .λ
No caso de radiação eletromagnética, o produto da frequência pelo comprimento de onda é constante e igual à velocidade da luz. Assim, sempre que a frequência aumenta, o comprimento de onda diminui e vice-versa. Outra propriedade importante da radiação eletromagnética emitida por uma fonte é expressa pela lei do quadrado das distâncias, ou seja, a intensidade (I) diminui rapidamente com a distância da fonte (d), conforme se segue:
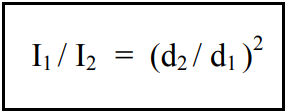
A razão para esse rápido decréscimo na intensidade da radiação é o fato que, quando se aumenta cada vez mais a distância da fonte pontual, a energia emitida é espalhada por áreas cada vez maiores. Como regra geral, a lei do quadrado da distância pode ser aplicada sempre que a distância da fonte for, pelo menos, sete vezes maior que a maior dimensão da fonte não pontual. O espectro eletromagnético está compreendido na faixa de freqüência de 10 a 1024 Hz e o comprimento de onda dos respectivos fótons encontram-se na faixa de 107 a 10-16 metros.
4 RADIOATIVIDADE:
Descoberta da Radioatividade:
Após o descobrimento dos raios-X por William Röentgen em 1895, o físico francês Henri Becquerel, associando a existência desses raios até então desconhecidos aos materiais fosforescentes e fluorescentes, testou uma série de substâncias com essas características. Assim, em 1896, verificou que sais de urânio emitiam radiações capazes de velar chapas fotográficas, mesmo quando envoltas em papel preto. Observou ainda, que a quantidade de radiação emitida era proporcional à concentração de urânio e era independente das condições de pressão, temperatura ou estado químico da amostra, além de permanecer inalterada mesmo sob a ação de campos elétricos ou magnéticos.
Posteriormente, o casal Pierre e Marie Curie aprofundou estas pesquisas, chegando, em 1898, à descoberta de dois novos elementos radioativos, quais sejam, o polônio e o rádio, tendo empregado o termo radioatividade para descrever a energia por eles emitida. Ernest Rutherford, em 1899, por meio de uma experiência simples, contribuiu para elucidar a natureza da radioatividade. Uma amostra do material radioativo foi colocada dentro de um recipiente de chumbo contendo um orifício. A radiação produzia um ponto brilhante em uma placa de sulfeto de zinco, colocada diante do orifício. Sob a ação de um campo magnético, o feixe de radiação repartia-se em três, que foram denominadas radiação alfa, beta e gama.
Em 1909, Rutherford e Soddy demonstraram que a radiação α era constituída por núcleos de hélio, com dois prótons e dois nêutrons, apresentando, portanto, duas cargas positivas. A radiação β foi, posteriormente, identificada como sendo constituída por elétrons. Tanto as partículas α como as partículas β eram emitidas com altas velocidades, demonstrando que uma grande quantidade de energia estava armazenada no átomo. Foi observado, também, que a radiação gama (γ) não era desviada de sua trajetória sob a ação do campo magnético e apresentava as mesmas características dos raios-X, ou seja, uma onda eletromagnética de alta energia.
Esses trabalhos de pesquisa científica permitiram concluir que a radioatividade é a transformação espontânea de um núcleo atômico, convertendo um nuclídeo em outro. A natureza das radiações emitidas é característica das propriedades nucleares do nuclídeo que está se desintegrando, denominado nuclídeo pai. O nuclídeo pai, ao se desintegrar, dá origem ao nuclídeo filho. Em alguns casos, o nuclídeo filho também é radiativo, formando, assim, uma cadeia radioativa.
Um nuclídeo radioativo é denominado radionuclídeo.
Tipos de Desintegração Radioativa:
Desintegração Alfa (α):
As partículas alfa são núcleos de hélio, constituídos por dois prótons e dois nêutrons, tendo duas cargas positivas. A reação de desintegração alfa pode ser assim esquematizada:

Desintegração Beta:
A desintegração beta tanto pode ser negativa (emissão de elétrons), quando o núcleo está com excesso de nêutrons, como positiva (emissão de pósitrons), ou seja, partículas com massa igual à do elétron, mas com carga positiva, quando o núcleo está com excesso de prótons, conforme descrito a seguir.
Desintegração Beta Negativa ( β- ):
Quando o núcleo possui um nêutron em excesso, este é convertido em um próton e uma partícula beta negativa.

A partícula beta negativa possui as mesmas características dos elétrons atômicos, porém tem origem no núcleo. A emissão de partícula β- é diferente das emissões α uma vez que as partículas β- são emitidas em um espectro contínuo de energia, variando de zero até um valor máximo, característico do núcleo pai. Esta energia máxima está na faixa de 0,05 - 3,5 MeV, para os nuclídeos mais comuns. Como o núcleo possui níveis de energias discretos, a emissão de uma partícula com espectro contínuo de energia é explicada pela emissão de uma segunda partícula, neste caso o antineutrino. O antineutrino transporta a diferença de energia existente entre a energia da partícula beta negativa e a energia disponível, dada pela diferença de massa entre o núcleo pai e os produtos da desintegração (Q).
Desintegração Beta Positiva ( β+):
Quando o núcleo possui um próton em excesso, este é convertido em um nêutron e uma partícula beta positiva (pósitron).
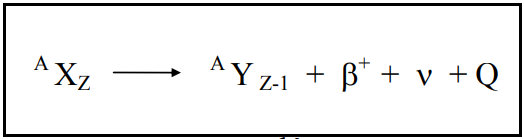
O pósitron possui a mesma massa do elétron e sua carga tem valor absoluto igual à do elétron, porém com sinal positivo. De maneira análoga às partículas beta negativas, as partículas beta positivas são emitidas em um espectro contínuo de energia. Neste caso, a energia máxima está na faixa de 0,3 - 1,4 MeV, para os nuclídeos mais comuns.
Desintegração por Captura Eletrônica:
O processo de captura eletrônica compete com o de desintegração beta positiva, isto é, também ocorre quando o núcleo possui um excesso de prótons. Em certos casos, a probabilidade do mesmo núcleo se desintegrar por qualquer um desses dois processos é comparável. Assim, o núcleo, ao invés de emitir um pósitron, captura um elétron de seu próprio átomo, convertendo um de seus prótons em nêutron e liberando um neutrino monoenergético, o qual transporta a energia disponível no processo.
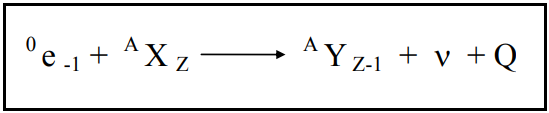
O elétron da camada K é o que tem maior probabilidade de ser capturado, em razão da sua maior proximidade do núcleo. Entretanto, este processo pode ocorrer também com elétrons de camadas mais externas. Após a captura do elétron, este deixará uma vaga no seu nível orbital, que será preenchida por outro elétron de camadas mais externas, dando origem à emissão de raios-X (chamados de característicos).
Conversão Interna e Elétron Auger:
A captura de elétrons orbitais pelo núcleo atômico pode vir acompanhada, algumas vezes, pela emissão de elétrons atômicos denominados elétrons Auger. Isto ocorre quando um dos raios-X emitidos colide com um dos elétrons que permaneceram nos orbitais atômicos e cede energia a esse elétron, deslocando-o de seu orbital.
Desintegração com Emissão Gama (γ):
Em muitos casos, após ocorrer um dos tipos de desintegração descritos anteriormente, o processo radioativo se completa. Em outros, o núcleo filho é formado em um de seus estados excitados, contendo, ainda, um excesso temporário de energia. Quando isto ocorre, o núcleo filho emite essa energia armazenada sob a forma de raios gama (γ). A radiação gama pertence a uma classe conhecida como radiação eletromagnética. Este tipo de radiação consiste de pacotes de energia (quanta) transmitidos em forma de movimento ondulatório. A radiação eletromagnética é uma modalidade de propagação de energia através do espaço, sem necessidade de um meio material.
Outros membros bem conhecidos desta classe são: ondas de rádio, raios-X e, inclusive, a luz visível. A diferença essencial entre a radiação γ e a radiação X está na sua origem. Enquanto os raios γ resultam de mudanças no núcleo, os raios-X são emitidos quando os elétrons atômicos sofrem uma mudança de orbital. Os raios γ são emitidos dos núcleos radioativos com energias bem definidas, correspondentes à diferença entre os níveis de energia de transição do núcleo que se desexcita. A transição pode ocorrer entre dois níveis excitados ou entre um nível excitado e o nível fundamental. Deste modo, pode haver a emissão de um ou mais raios γ em cada desintegração. Por exemplo, o Cobalto-60, após desintegração beta, tem como resultado o segundo nível de excitação do Níquel-60 que, como conseqüência, emite dois gamas, um de 1,17 MeV e outro de 1,33 MeV. A energia dos raios gamas emitidos pelos diferentes nuclídeos está, aproximadamente, na faixa de 0,03 – 3 MeV.
Interação da Radiação com a Matéria:
As radiações são processos de transferência de energia sob a forma de ondas eletromagnéticas e, ao interagir com a matéria, resulta na transferência de energia para os átomos e moléculas que estejam em sua trajetória. Sob ponto de vista da física, as radiações, ao interagirem com um meio material, podem provocar ionização, excitação, ativação do núcleo ou emissão de radiação de frenamento, conforme descrito a seguir.
- Ionização: processo de formação de átomos eletricamente carregados, ou seja, íons, pela remoção ou acréscimo de um ou mais elétrons.
- Excitação: adição de energia a um átomo, elevando-o do estado fundamental de energia ao estado de excitação. Os elétrons são deslocados de seus orbitais de equilíbrio e, ao retornarem, emitem a energia excedente sob a forma de radiação (luz ou raios-X característicos).
- Ativação do Núcleo: interação de radiações com energia superior à energia de ligação dos núcleons e que provoca reações nucleares, resultando num núcleo residual e na emissão de radiação.
- Radiação de Frenamento: (Bremsstrahlung) radiação, em particular raios-X, emitida em decorrência da perda de energia cinética de elétrons que interagem com o campo elétrico de núcleos de átomos-alvo, átomos estes com elevado número atômico, ou mesmo que interagem com a eletrosfera.
Em decorrência das diferenças existentes entre as partículas e radiações, em suas cargas e suas massas, cada um deles interage de modo diferente com a matéria. O conhecimento das propriedades das radiações e de seus efeitos sobre a matéria são de grande importância, destacando-se:
- A detecção de substâncias radioativas, uma vez que se baseia, sempre, em alguns dos efeitos produzidos pela radiação na parte sensível do equipamento de medida;
- A maior facilidade na interpretação das diversas aplicações dos materiais radioativos;
- A adoção das medidas preventivas mais apropriadas, de modo a proteger o corpo humano dos efeitos nocivos da radiação.
Quando as partículas carregadas ou a radiação eletromagnética atravessam a matéria, o mecanismo que mais contribui para a perda de energia é a interação com os elétrons. Isto se justifica pelo fato do raio do núcleo ser da ordem de 10.000 vezes menor que o raio do átomo. Assim, é de se esperar que o número de interações com elétrons seja muito maior que com núcleos, uma vez que o número de interações é proporcional à área projetada, ou seja, ao raio elevado ao quadrado.
Para o caso específico de partículas carregadas, este fenômeno é facilmente evidenciado a partir da dispersão que elas experimentam ao interagir com a matéria. As partículas mais pesadas são pouco desviadas de sua direção original quando interagem, perdendo energia. As partículas beta, por serem menos pesadas, são desviadas com ângulos muito maiores ao interagirem com o meio. As perdas de energia resultante de colisões com núcleos resultam ser várias ordens de grandeza menores que na interação com elétrons.
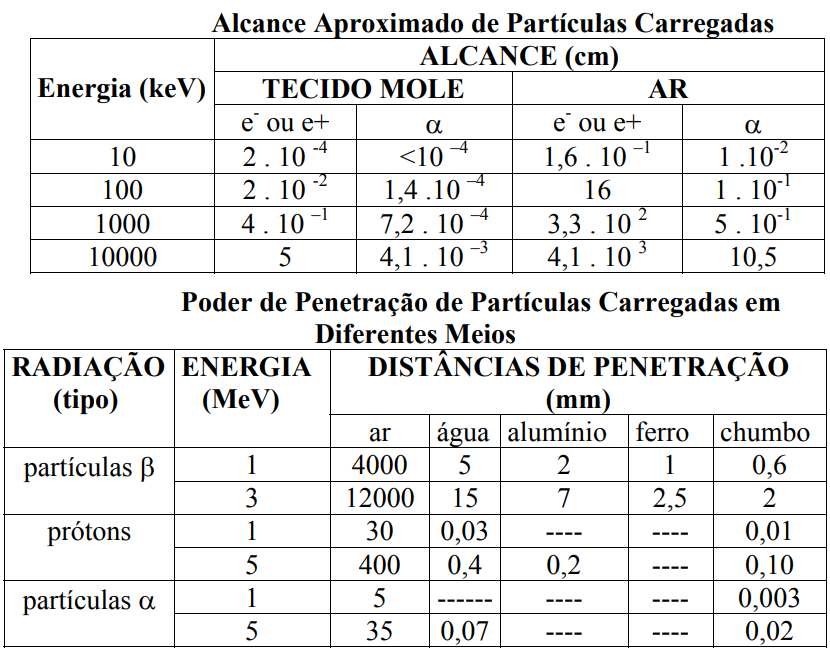
Interação de Partículas Carregadas (10 keV a 10 MeV):
Uma partícula carregada, ao passar através de uma substância (alvo) pode interagir com elétrons carregados negativamente e núcleos de átomos ou moléculas carregados positivamente. Devido à força Coulombiana, a partícula, em função de sua carga, tenta atrair ou repelir os elétrons ou núcleos próximos de sua trajetória, perdendo parte de sua energia, esta tomada pelos átomos alvo próximos a sua trajetória. Essas partículas, à medida que penetram na matéria, sofrem colisões e interações com perda de energia até que, a uma dada espessura do material, toda energia é dissipada e a partícula, portanto, para de se deslocar. Denomina-se alcance a distância média percorrida por uma partícula carregada, em uma dada direção, distância essa que depende de vários fatores. Quatro dos mais importantes são descritos a seguir:
- Energia: O alcance de uma dada partícula é ampliado com o aumento da energia inicial.
- Massa: Partículas mais leves tem alcance maior que partículas mais pesadas de mesma energia e carga. A dependência do alcance em relação à massa é, algumas vezes, expressa como função da velocidade da partícula.
- Carga: Uma partícula com menos carga possui alcance maior que uma partícula com mais carga.
- Densidade do Meio: Quanto mais alta a densidade do meio, menor é o alcance da partícula, sendo este muito maior em gases do que em líquidos ou sólidos.
As partículas α, por exemplo, pelo fato de serem pesadas e possuírem carga +2, interagem muito intensamente com a matéria. Seu poder de ionização é muito alto, perdendo toda a energia em poucos micrometros de material sólido ou em alguns centímetros de ar. Isso significa que o poder de penetração das partículas alfa é muito pequeno, sendo a espessura de uma folha de papel suficiente para blindar todas as partículas emitidas por uma fonte alfa. Já as partículas β, pelo fato de possuírem massa muito menor do que a das partículas α e, ainda, uma carga menor, também apresentam poder de ionização mais baixo. Isto significa que seu poder de penetração é maior do que o das partículas α e, portanto, é necessária uma espessura maior de material para que ocorra a perda de toda sua energia.
Interação da Radiação Eletromagnética Ionizante com a Matéria:
No processo de interação de partículas carregadas com a matéria, a energia é perdida em decorrência de um grande número de colisões, a maioria com elétrons orbitais, processo esse que não ocorre na interação da radiação gama ou X com a matéria. Nesta, em princípio, os fótons são absorvidos ou desviados de sua trajetória original por meio de uma única interação. O fóton, quando produz ionização, o faz em uma única vez, sendo que o elétron pode ser arrancado de um átomo por diversos mecanismos. Este elétron liberado, denominado elétron secundário, pode possuir quase tanta energia quanto um fóton inicial e, por sua vez, produzir novas ionizações até consumir toda sua energia. Em outras palavras, pode-se considerar que a ionização da matéria, quando atravessada por fótons, é conseqüência de elétrons secundários, já que cada fóton, em princípio, produz muito pouca ou, às vezes, só uma ionização. Os principais efeitos decorrentes da interação das radiações γ e X com a matéria são:
Efeito Fotoelétrico: caracterizado pela transferência total de energia de um fóton (radiação X ou gama), que desaparece, a um único elétron orbital, o qual é expelido com uma energia cinética bem definida, T, qual seja:

Como T expressa a energia do fóton, a menos de um valor constante Be, a transferência dessa energia para o material de um detetor pode ser utilizada como mecanismo de identificação do fóton e respectiva energia. O fato da transferência de energia do elétron de ionização para o material produzir uma ionização secundária proporcional, faz com que a amplitude do pulso de tensão ou intensidade de corrente proveniente da coleta dos elétrons, ou íons, no final do processo expressem a energia da radiação incidente. A direção de saída do fotoelétron, com relação à de incidência do fóton, varia com a energia.
Para altas energias (acima de 3 MeV), a probabilidade de ser ejetado para frente é bastante grande. Para baixas energias (abaixo de 20 keV) a probabilidade de sair para o lado é máxima para um ângulo de 70 graus. O efeito fotoelétrico é predominante para baixas energias e para elementos químicos de elevado número atômico Z, decrescendo rapidamente com o aumento de energia. No caso do chumbo, por exemplo, o efeito fotoelétrico é maior para energias menores que 0,6 MeV e, no caso do alumínio, para energias menores do que 0,06 MeV.
Efeito Comptom: onde o fóton interage com um elétron periférico do átomo, mas cede apenas parte de sua energia, resultando na emissão de um fóton com energia menor e que continua sua trajetória dentro do material e em outra direção. Como a transferência de energia depende da direção do elétron emergente e sendo esta aleatória, de um fóton de energia fixa podem resultar elétrons com energia variando de zero até um valor máximo. Assim, a informação associada ao elétron emergente é desinteressante, sob ponto de vista da detecção da energia do fóton incidente. Quando a energia de ligação dos elétrons orbitais se torna desprezível face à energia do fóton incidente, a probabilidade de ocorrência de espalhamento Compton aumenta consideravelmente. O efeito Compton é predominante para energias intermediárias (100keV - 1MeV).
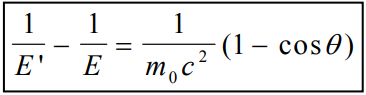
Formação de Pares: uma das formas predominantes de absorção da radiação eletromagnética de alta energia, também chamada de formação de par elétron-pósitron, ocorre quando fótons de energia superior a 1,02 MeV passam próximos a núcleos de elevado número atômico, interagindo com o forte campo elétrico nuclear. Nesta interação, a radiação desaparece e dá origem a um par elétron-pósitron, por meio da reação:
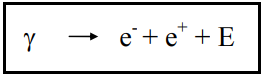
5 Decaimento Radioativo:
Quando um núcleo é instável por excesso de núcleons (prótons e nêutrons) ou quando a razão A/Z (número de massa/número atômico) é muito grande, ele se desintegra, por emissão alfa ou beta, conforme exemplificado a seguir:
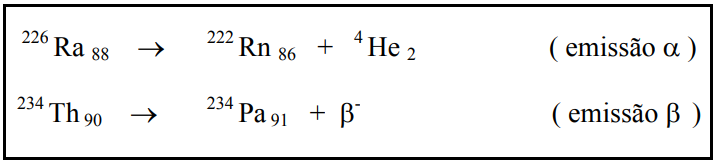
No interior do núcleo, os prótons e os nêutrons interagem intensamente, resultando numa força chamada nuclear, de curto alcance, de tal forma que somente núcleons muito próximos interagem entre si. Existe, também, no núcleo, uma interação entre prótons, dando origem a forças elétricas mais fracas, porém com alcance maior. Assim, quando prótons e nêutrons estão no núcleo, existe competição entre essas duas forças: as forças nucleares de curto alcance tendem a manter os núcleons bem próximos e a força elétrica tende a separar os prótons.
Para átomos com um número elevado de prótons e nêutrons, a força elétrica de repulsão continua atuando, mas a força nuclear de curto alcance não abrange todos os núcleons, resultando em núcleo instável. Assim, em busca da estabilidade, ou seja, para se transformar em núcleo com núcleons mais fortemente ligados, são emitidas energia e partículas α ou β, o que leva à formação de núcleo de elemento químico distinto do original. Muitos fatores afetam a estabilidade nuclear sendo, talvez, o mais importante o número de nêutrons. Quando um núcleo possui nêutrons a mais (em relação ao número de prótons), ou a menos, o átomo pode se desintegrar em busca de uma configuração estável.
Velocidade de Desintegração A emissão de radiação por uma população de átomos de um dado isótopo radioativo não ocorre simultaneamente em todos os seus núcleos. Assim, o número de átomos que se desintegram transcorrido um intervalo de tempo (t – t0) será dado pela diferença entre o número de átomos de um isótopo radioativo no instante inicial (N0) e o número de átomos ainda não desintegrados (N) do mesmo isótopo, no tempo t > t0. Logo, a velocidade média de desintegração, Vm, será dada pela relação:
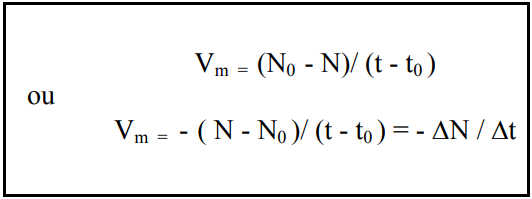
A velocidade instantânea de desintegração num intervalo de tempo infinitésimo dt, ou seja, quando ∆t tende a zero, é dada pela derivada de N em relação a t, dN/dt , com o sinal negativo. A variação do número de desintegrações nucleares espontâneas (dN) em um intervalo de tempo dt é chamada atividade, A, ou seja:
A = dN/dt
A primeira unidade estabelecida para atividade foi o Curie, originalmente definido como a taxa de desintegração do gás radônio (222Rn), em equilíbrio com um grama de rádio (226Ra). Posteriormente, o Curie foi definido mais precisamente pelo valor abaixo, que é bem próximo do medido originalmente.

Constante de Desintegração e Meia-Vida:
A velocidade de desintegração varia muito entre os isótopos radioativos, existindo uma probabilidade para cada um emitir um certo tipo de radiação, ou se desintegrar, característica desse isótopo. Esta probabilidade é chamada Constante de Desintegração ou Constante Radioativa, sendo representada pelo símbolo λ. A velocidade de desintegração depende não só do número de átomos do isótopo radioativo presente na amostra (quanto maior N, maior o número de radiações emitidas), como também da constante radioativa λ, ou seja:
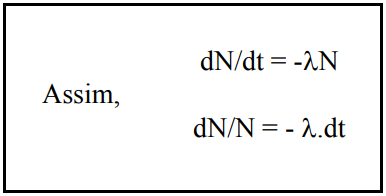
Integrando-se o primeiro termo dessa igualdade no intervalo de variação do número de átomos não desintegrados, ou seja, entre N0 (início da contagem do tempo, t = 0) e N (número de átomos do radioisótopo, presentes decorrido o tempo t) e integrando-se o segundo termo entre zero e t, tem-se que:
N = N0 exp (- λ.t )
sendo esta a expressão da Lei da Desintegração Radioativa, que mostra que o número de átomos de um radionuclídeo diminui exponencialmente com o tempo.
De maneira similar, a atividade de uma fonte radioativa, no tempo t, é expressa por:
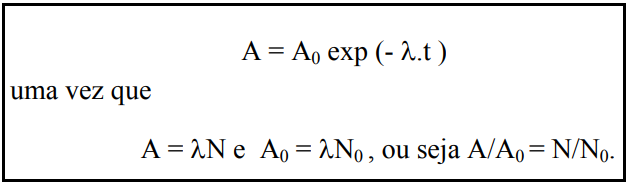
A meia-vida de um isótopo radioativo, t1/2, é o tempo necessário para que metade dos átomos contidos numa amostra desse isótopo sofra desintegração, ou seja, é o tempo necessário para que N seja igual a N0/2. A relação matemática existente entre λ e t1/2 pode ser obtida substituindo-se, na equação anterior, N por N0/2 e t por t1/2.
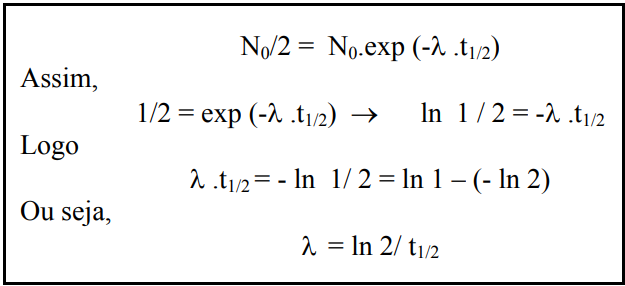
Portanto, a meia-vida de um radioisótopo pode ser calculada a partir da constante de desintegração e vice-versa. O intervalo de tempo necessário para que o organismo elimine metade de uma substância ingerida ou inalada é chamado meia-vida biológica, tb . Quando a meia-vida física e a meia-vida biológica devem ser levadas em consideração, determina-se a meia-vida efetiva, tef, por meio da seguinte expressão: