Como deve ser coletado e transportado o sangue para a quantificação de subpopulações de linfócitos CD4?
O sangue para o teste de quantificação de linfócitos CD4 deve ser coletado em tubo contendo solução de EDTA e transportado em temperatura ambiente, não excedendo a 37°C. A amostra deve chegar ao laboratório, onde será processada para o exame, no máximo 18 horas após a coleta.
Atenção:
No teste de CD4 é utilizado o sangue total, que nunca deve ser colocado em geladeira ou congelador.
Como coletar, separar e transportar a amostra usada para o teste de quantificação da carga viral para o HIV?
O sangue deve ser coletado em tubo contendo solução de EDTA. O plasma deve ser separado por centrifugação, a 1.500 rpm por 10 minutos. Deve ser armazenado a -70°C e transportado congelado.
Obs:
O plasma deve chegar e permanecer congelado no laboratório até a realização do teste.
Para cuidar de sua segurança, da segurança de seus colegas de trabalho e do meio ambiente, obedeça aos procedimentos básicos de biossegurança em laboratórios:
Todo cuidado é pouco na manipulação de materiais biológicos, tais como soro, sangue ou secreções, fluidos orgânicos, tecidos etc. Redobre suas precauções, pois esses materiais são potencialmente infectantes e muitas vezes estão contaminados com agentes etiológicos diferentes do que se está pesquisando, ou ainda desconhecidos. Nunca pipete com a boca e jamais cheire placas de cultura. A inativação do soro em banho-maria a 56°C por 30 minutos não elimina o potencial infectante da amostra.
Lembre-se de que, com a automação, aumentou muito o número de amostras processadas em laboratório e, consequentemente, aumentou também o risco de contaminação. Como você sabe, é difícil afirmar que um profissional se contaminou, de fato, em serviço. Isso faz com que as doenças infecto-contagiosas causadas por acidentes de trabalho não sejam devidamente notificadas; em conseqüência, as medidas de segurança envolvendo o biorisco acabam não sendo implementadas.
Use sempre equipamento de Proteção Individual (EPI): avental ou jaleco longo de mangas compridas e punho retrátil, luvas descartáveis, óculos de proteção, pipetadores manuais ou automáticos e, quando for o caso, protetor facial. Os EPI são regulamentados pelo Ministério do Trabalho e seu uso visa a minimizar a exposição do técnico aos riscos e evitar possíveis acidentes nos laboratórios.
Note que, às vezes, os profissionais de laboratório precisam de um tempo para se adaptar ao uso dos equipamentos na sua rotina. O importante é que você se adapte e incorpore a utilização dos EPI à sua prática profissional. O uso indevido dos EPI, ao invés de proteger, poderá ocasionar acidentes.
Evite a formação e dispersão de aerossóis. Aerossóis são micropartículas sólidas e líquidas com dimensões aproximadas entre 0,1 e 50 micra que podem, caso contenham micro-organismos, permanecer em suspensão e plenamente viáveis por várias horas. A pipetagem, flambagem de alças, abertura de frascos e ampolas, manipulação de seringas, agulhas, lancetas, lâminas e outros assemelhados podem gerar e propagar aerossóis. Abertura de frascos, ampolas, tubos e garrafas de cultura requer cuidados especiais.
Envolva a parte a ser aberta com um pedaço de gaze. Utilize um pedaço de gaze para cada material, prevenindo assim a contaminação cruzada. Descarte-a imediatamente em hipoclorito de sódio a 2 %. Centrífugas, agitadores e maceradores, quando manipulados sem as precauções e abertos antes da total parada ou término da operação, igualmente podem contaminar o ambiente laboratorial.
Jamais reencape agulhas. Esse procedimento é uma das principais causas da contaminação de profissionais de saúde por micro-organismos, existentes no sangue e em outros fluidos orgânicos, como por exemplo, o vírus da hepatite B e o HIV. Após a coleta, você deve descartar esse material diretamente em recipiente de paredes rígidas com tampa, contendo hipoclorito de sódio a 2% em volume superior a metade do recipiente.
Lembre-se: Cada mililitro de sangue contaminado com o vírus da hepatite B contém 100.000.000 de partículas virais, que podem permanecer viáveis por até uma semana. Basta (01) uma dessas partículas para contaminar a pessoa.
Reduza ao máximo o manuseio de resíduos, em especial os perfurocortantes. Descarte o rejeito perfurocortante diretamente em recipiente de paredes rígidas, contendo hipoclorito de sódio a 2%. Deixe em imersão total no mínimo por 24 horas e, em seguida, faça a autoclavação desse material. Esta é uma regra básica para diminuir os riscos de acidente nos laboratórios. É fundamental que os materiais perfurocortantes sejam autoclavados depois da imersão em hipoclorito de sódio a 2%. Só então esses materiais devem ser encaminhados ao lixo hospitalar.
O acondicionamento dos resíduos de laboratório deve seguir a Norma Brasileira (NBR) 9190 da Associação Brasileira de Normas Técnicas- ABNT, que recomenda sacos brancos leitosos para os resíduos potencialmente infectantes e hospitalares e escuros para o lixo comum. Os profissionais responsáveis pela limpeza e conservação devem ser bem orientados e usar equipamentos de proteção. Todos os recipientes para descarte devem estar identificados.
Lembre-se de que, pela legislação brasileira, quem gera o resíduo é o responsável pela sua eliminação e controle. No caso dos materiais reutilizáveis, como vidraria e utensílios, deposite-os em recipiente contendo o desinfetante próprio, pelo tempo de contato recomendado e, em seguida, faça a autoclavagem. Depois, lave normalmente esses materiais e guarde-os para uso posterior.
Identifique e sinalize os principais riscos presentes em seu laboratório. Produtos e áreas que oferecem risco devem ser marcados com os devidos símbolos internacionais em etiquetas auto-adesivas padrão.
Veja, a seguir, os principais símbolos associados aos riscos em laboratórios.
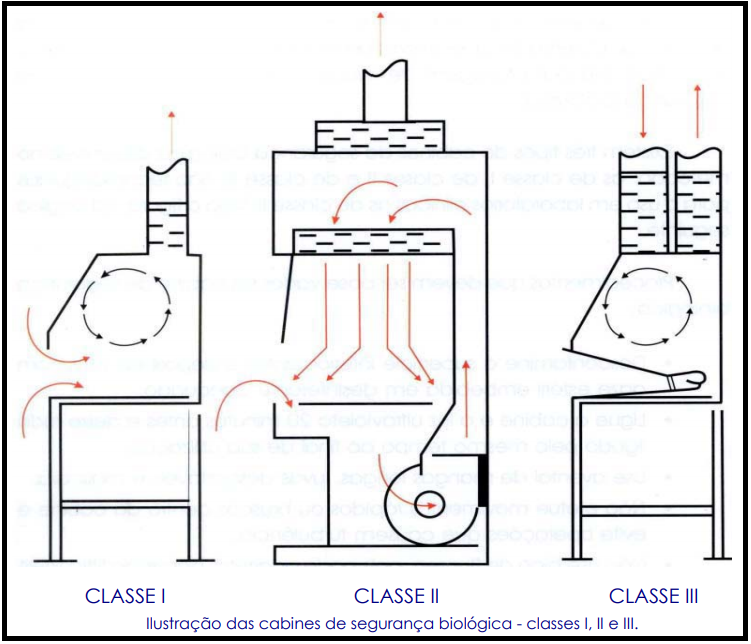
Verifique sempre as condições de funcionamento dos equipamentos de Proteção Coletiva (EPC): extintores de incêndio, chuveiros de segurança, lava-olhos, pia para lavagem de mãos, caixa de areia e cabine de segurança biológica. Existem três tipos de cabines de segurança biológica disponíveis no mercado: as de classe I, de classe II e de classe III. São recomendadas para o uso em laboratórios clínicos as de classe II. Veja a figura, na página seguinte. Procedimentos que devem ser observados na cabine de segurança biológica:
- Descontamine a superfície interior, antes e depois do uso, com gaze estéril embebida em desinfetante adequado;
- Ligue a cabine e a luz ultravioleta 20 minutos antes e deixe tudo
ligado pelo mesmo tempo ao final de sua utilização;
- Use avental de mangas longas, luvas descartáveis e máscara;
- Não efetue movimentos rápidos ou bruscos dentro da cabine e
evite operações que causem turbulência;
- Não use bico de Bunsen, pois pode acarretar a anos ao filtro HEPA e causar desequilíbrio do fluxo de ar. Se necessário, use incinerador elétrico ou micro queimador automático; e
- Mantenha as grelhas anteriores e posteriores da cabine desobstruídas. A cabine não é um depósito. Evite guardar equipamentos ou quaisquer outros objetos no seu interior.
As cabines de classe I e II são consideradas como barreira de proteção parcial e a de classe III é uma barreira de proteção total.