Introdução ao estudo dos processos químicos industriais-relacionamento com a engenharia química
Inicialização em Técnico de Química Industrial
1 Processo químico:
Definição de processo químico:
Define-se processo químico como qualquer operação ou conjunto de operações coordenadas que provocam transformações químicas e/ou físicas num material ou numa mistura de materiais.
Objetivo dos processos químicos:
O objetivo dos processos químicos é a obtenção de produtos de interesse a partir de matérias-primas selecionadas ou disponíveis para tal.
Por exemplo, pode-se obter etanol a partir de diferentes fontes de carbono:


Exemplos de processos químicos
Shreve e Brink jr. (1980) detalham vários processos químicos, entre eles tem-se:
- Tratamento de água;
- Produtos carboquímicos;
- Indústria de cerâmica;
- Indústria do açúcar e do amido.
Fluxograma da produção de açúcar (C12H22O11):
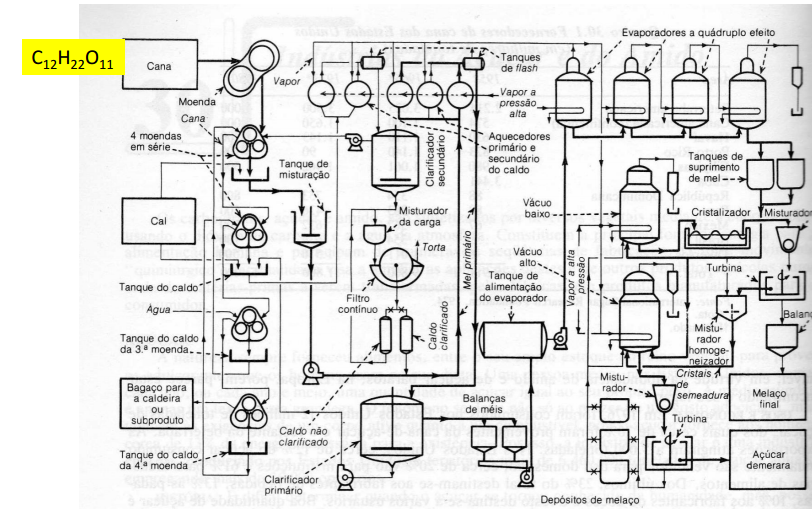
Fluxograma da produção de álcool (C2H5OH)
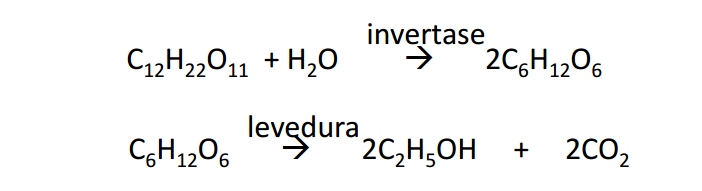
2 Análise de processos químicos:
De acordo com os processos apresentados, as matérias-primas são transformadas em produtos através de uma sequência de etapas.
Essas etapas são denominadas operações unitárias da indústria química e são realizadas em equipamentos específicos, tais como moendas, evaporadores, centrífugas, secadores e colunas de destilação.




Qual é o objetivo da análise de processos químicos:
A análise dos processos químicos tem como objetivo a obtenção das quantidades e propriedades das correntes de produtos a partir de quantidades apropriadas das correntes de alimentação, e vice-versa, nas etapas do processo.
Assim, deve-se conhecer as principais variáveis envolvidas nos processos, tendo como base a lei de conservação de massa e energia.
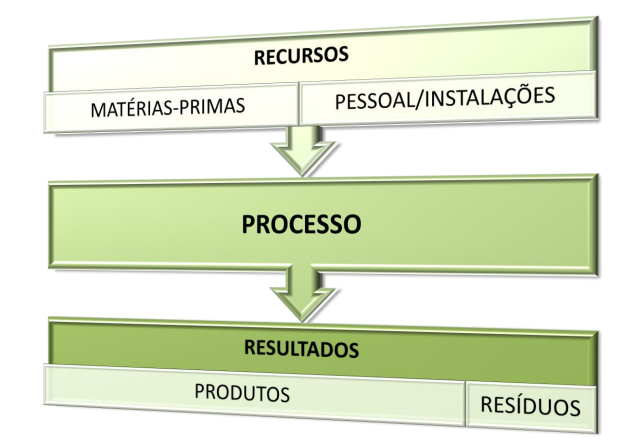
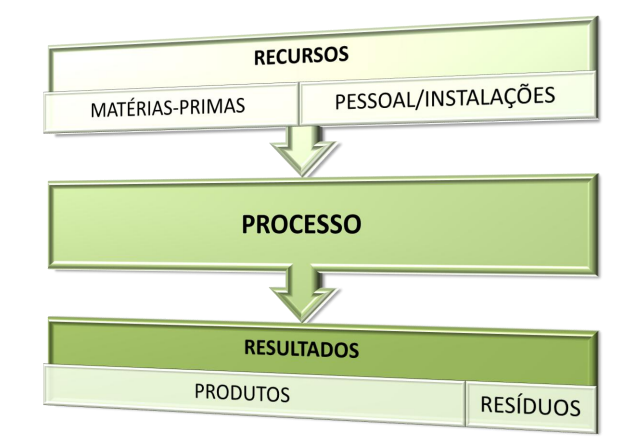
3 Recursos:
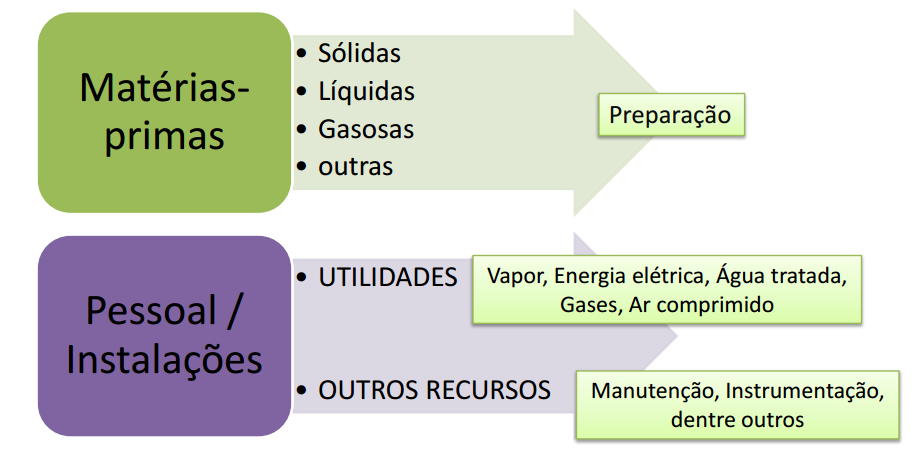
Resíduos:
• Sub-produtos
• Resíduos poluentes
• Resíduos sólidos recicláveis
• Resíduos sólidos tratáveis
• Resíduos sólidos incineráveis
• Resíduos sólidos para aterros
• Efluentes (líquidos, sólidos e gasosos)
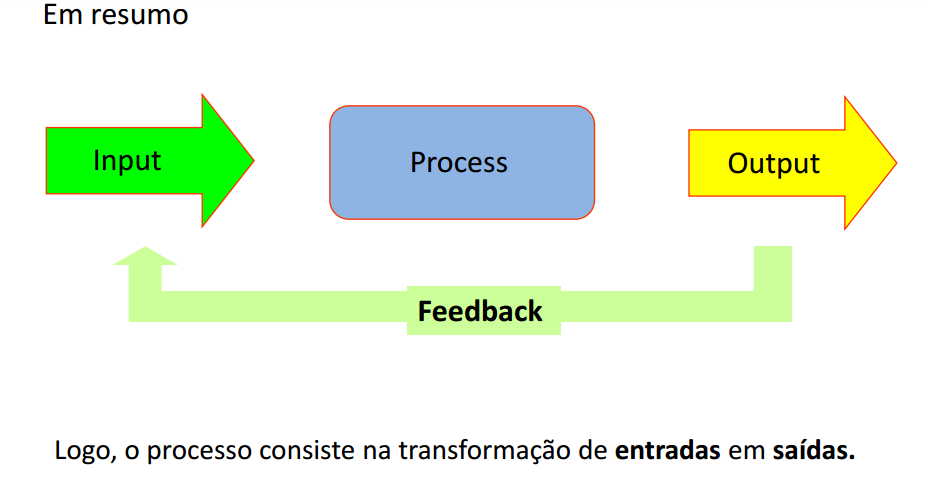
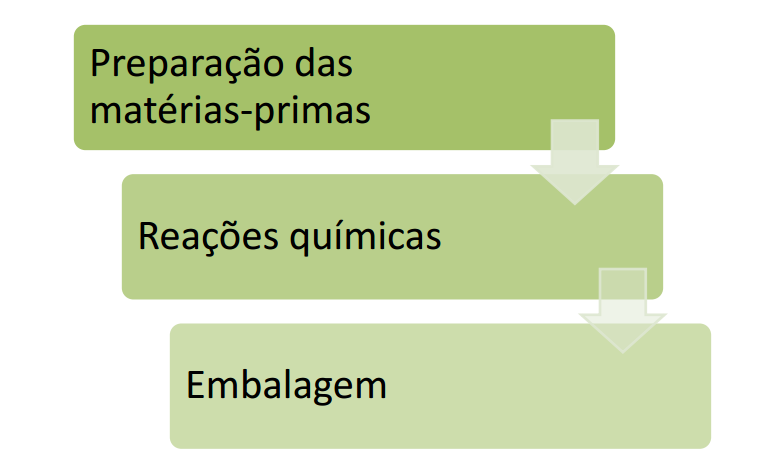
O processo químico compreende várias etapas:
OPERAÇÃO:
É a ação direta do homem e equipamentos sobre a matéria-prima e seus produtos (funções que devem ser executadas).
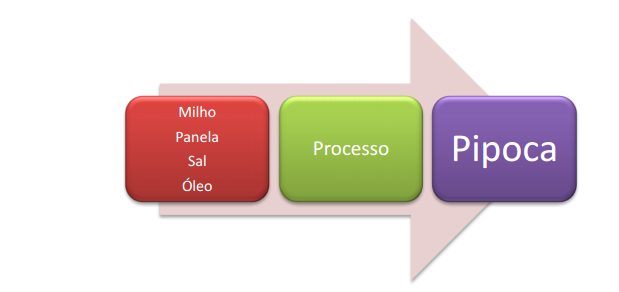
PROCESSO:
É um conjunto de operações físicas e transformações químicas que visam obter produtos finais a partir de matérias-primas.
4 Operações unitárias:
Segundo Cremasco, Operações Unitárias constituem-se etapas individuais, visando ao tratamento e/ou separação e/ou transporte físico de matéria e/ou energia, presentes em um processo (bio) químico.
O que vale ressaltar é que em uma operação unitária existe uma alteração física ou uma separação sem ocorrer reação química.
Operações unitárias:
- Bombeamento de fluidos
- Troca de calor
- Transporte de sólidos
- Redução de tamanho
- Peneiração
- Filtração
- Misturação
- Destilação
- Evaporação
- Absorção de gás
- Extração
- Processos de separação
- Secagem
5 Processo Químico Industrial:
Mas, o que é um PROCESSO QUÍMICO INDUSTRIAL?
É a aplicação dos princípios da química, da física e da físico-química (quando necessário, apoiadas por outras ciências) para a transformação da(s) matéria(s)- prima(s) em produtos.



RENDIMENTO E CONVERSÃO:


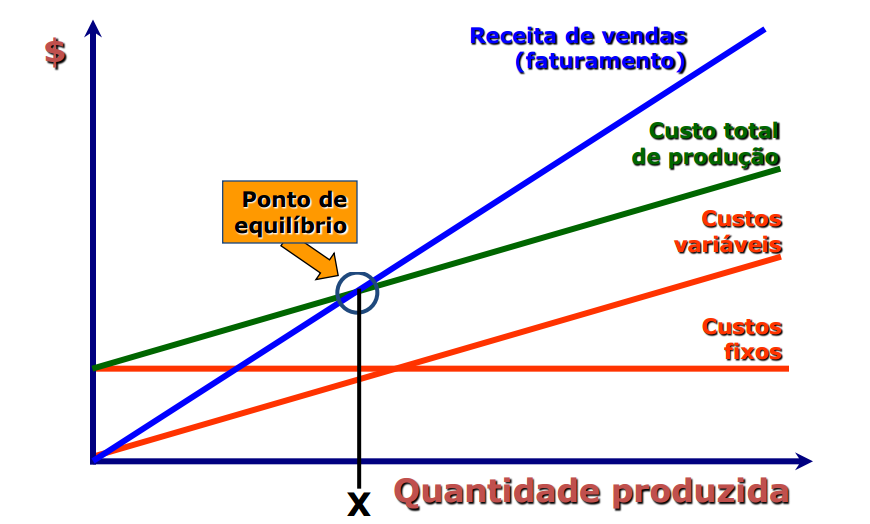
6 Custos de produção:




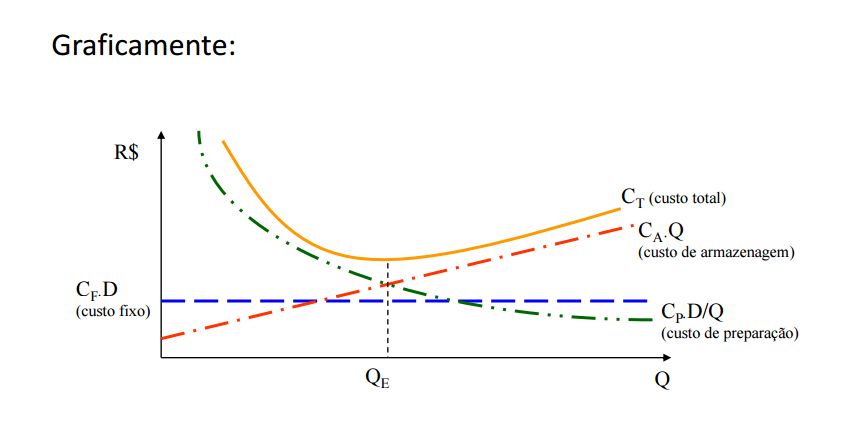
Aplicação:
A Indústria de alimentos MF Ltda está planejando as rodadas de produção para sua linha de iogurtes. Em média, estima-se que o custo de preparação de máquinas esteja em torno de R$ 200,00; havendo pouca diferenciação de um sabor e outro. O custo unitário médio de fabricação foi calculado em R$ 300,00, sobre o qual, para efeito de armazenagem, incidirá uma taxa total de 60% entre juros e armazenagem. Estima-se que, para 2014, a demanda para linha de iogurte light situar-se-á em torno de 5.000 caixas.
Determinar:
a) Quantas caixas devem ser produzidas de cada vez;
b) Qual o custo total;

c) Custo total e custo total em estoque

7 Classificação dos processos:
Os processos químicos são classificados de acordo com o procedimento de entrada e saída de matéria do volume de controle em:
- Processos em batelada;
- Processos contínuos;
- Processos semicontínuos.
Processo Descontínuo (por batelada):
Um equipamento é carregado com as matérias-primas, a operação ou a conversão ocorrem após um tempo determinado, quando então o produto é descarregado.
Exemplos:
Polimerização, fabricação de produtos farmacêuticos, de especialidades químicas.

O processo descontínuo é utilizado quando o volume de produção é pequeno, quando o custo de produção é mais favorável que o do processo contínuo ou quando condições de segurança são fundamentais.
Processos contínuos:
Diferentemente dos processos em batelada, as entradas e saídas fluem continuamente ao longo do tempo total de processo.
Exemplo:

Processos contínuos:
O processo contínuo exige uma instrumentação de processo mais complexa, que não somente registre, mas também controle as variáveis do processo (temperatura, vazão, pressão...).
É necessário controlar os desvios e corrigi-los rapidamente.
Controle informatizado do processo.
Custos são altos para pequenas produções mas se diluem para grandes produções.
Processos semicontínuos:
É qualquer processo que não se enquadre nas duas definições anteriores.
Exemplos:


8 Tipos de fluxogramas:
Os três principais tipos de diagramas usados para descrever os fluxos de correntes químicas através de um processo são:
– Fluxogramas de blocos (block flow diagrams – BFD)
– Fluxograma do processo (process flow diagram – PFD)
– Fluxogramas de tubulação e instrumentação (piping and instrumentation diagram – P&ID):
Fluxogramas de blocos:
Permite a rápida visualização do processo.
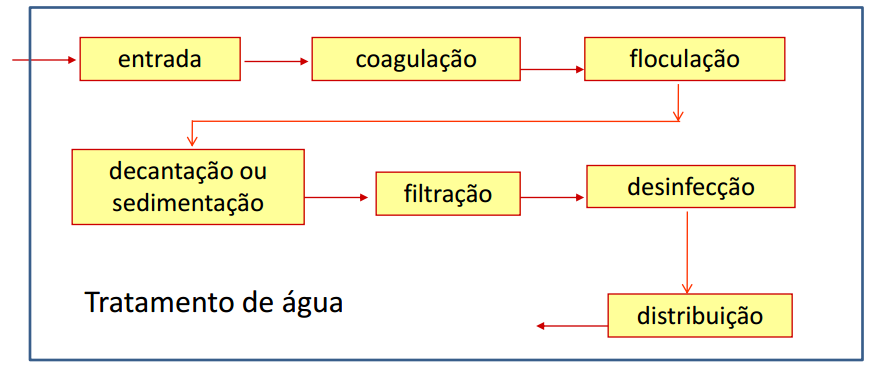
Cada bloco ou retângulo representa uma operação unitária ou processo unitário.
Para fazer fluxogramas de blocos claros e objetivos:
– Correntes de entrada e saída são representadas por linhas retas que podem ser horizontais ou verticais;
– A direção do fluxo deve ser claramente indicada por setas;
– As correntes de fluxo devem ser numeradas em uma ordem lógica;
– As operações unitárias (i.e blocos) devem ser rotulados;
– Quando possível, o diagrama deve ser arrumado de modo que o fluxo material ocorra da esquerda para a direita, com unidades a montante, à esquerda, e unidades a jusante, à direita.
Fluxograma do processo:
Contém as informações necessárias para os balanços material e energético do processo.
O fluxograma de processo apresenta as relações entre os principais componentes no sistema, bem como tabula os valores projetados para o processo para os componentes nos diferentes modos de operação: mínimo, normal e máximo.
Um fluxograma de processo inclui:
– tubulação do sistema;
– símbolos dos principais equipamentos, nomes e números de identificação;
– Controles e válvulas que afetam a operação do sistema;
– interconexões com outros sistemas;
– principais rotas de by-pass e recirculação;
– taxas do sistemas e valores operacionais como temperatura e pressão para fluxos mínimo, normal e máximo;
– composição dos fluidos.
Exemplo:
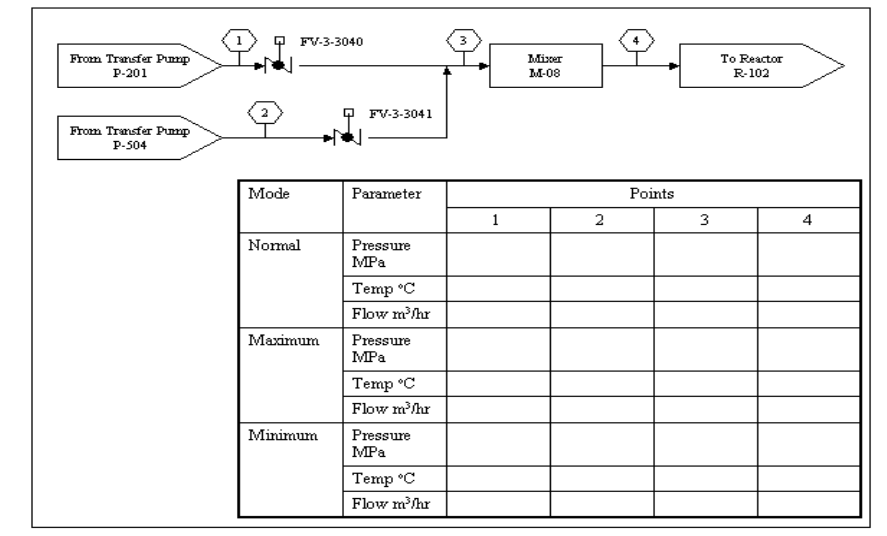
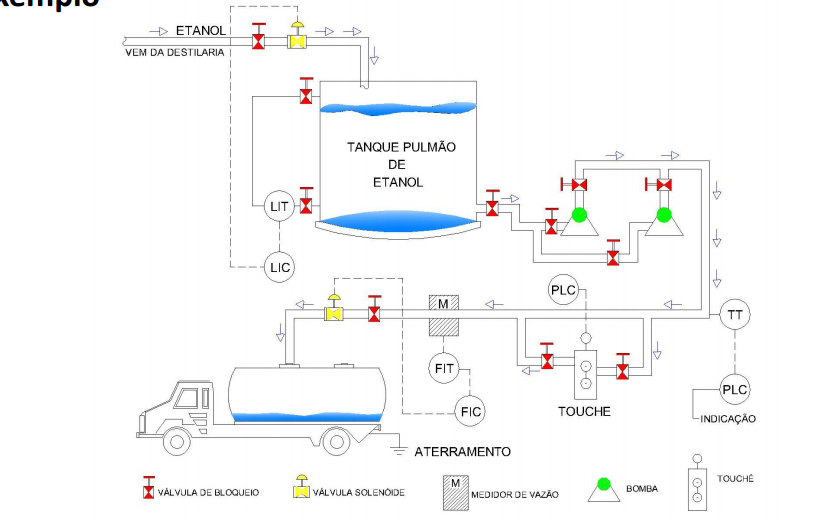
Fluxogramas de tubulação e instrumentação:
Deve conter toda informação do processo necessária para a construção da planta.
• Mostram toda a tubulação incluindo a sequência física de ramificações, redutores, válvulas, equipamentos, instrumentação e controles intertravados;
• São usados para operar o processo de produção;
• Devem apresentar todos os detalhes pertinentes ao processo.
Exemplo:
9 Reações químicas realizadas em condições industriais:
Industrialmente, os reatores químicos podem ser de vários materiais, formatos e dimensões, dependendo das condições em que a conversão química se realiza.
Os reagentes em excesso podem ou não retornar ao processo, formando o reciclo; pode haver catalisador ou não; o catalisador pode estar em leito fixo ou em leito fluido.
Para melhorar o rendimento nas reações químicas realizadas em condições industriais, geralmente, é desejável que um ou mais reagentes estejam em excesso (em relação às quantidades teóricas previstas pelas equações químicas).
Exemplo: Processos de nitração
As quantidades máximas dos produtos formados serão determinadas pela quantidade do reagentelimitante , que é aquele que não se encontra em excesso; o qual servirá de base para o cálculo do excesso dos de mais.
10 Equação química e estequiometria:
A equação química fornece informações quali- e quantitativas essenciais para o cálculo das massas dos materiais envolvidos em um processo químico, como por exemplo:
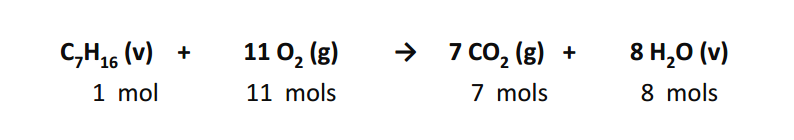
A equação química nos fornece, em termos de mols, as razões entre reagentes e produtos (chamadas razões estequiométricas).
A Estequiometria lida com as massas dos elementos e compostos que se combinam.